1、选择题 下列叙述正确的是
[? ]
A.在醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a b
b
B.在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH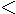 7
7
C.1.0×10-3mol/L盐酸pH=3,1.0×10-8mol/L盐酸的 pH=8
D.若1mLpH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7则NaOH溶液的pH=11
2、选择题 已知一种c(H+)=1×10-3?mol/L的一元酸溶液和一种c(OH-)=1×10-3?mol/L的一元碱溶液等体积混合后溶液呈碱性,则生成的盐是
[? ]
A.强酸强碱盐?
B.强酸弱碱盐
C.强碱弱酸盐?
D.上述三种盐均可能
3、选择题 若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能
[? ]
A.生成一种强酸弱碱盐
B.弱酸溶液和强碱溶液
C.强酸与弱碱溶液反应
D.一元强酸溶液与一元强碱溶液反应
4、填空题 现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
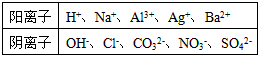
已知:
①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是___________________(用离子方程式表示)。
(2)写出E溶液与过量的B溶液反应的离子方程式______________________。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H=-a kJ・mol-1。请写出相同条件下B与C的稀溶液反应的热化学方程式______________________。
(4)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子浓度______
倍。
(5)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或-1)浓度由大到小的顺序为:______________________。
5、选择题 下列说法正确的是
[? ]
A.t ℃ 时,某溶液pH=6,则该溶液一定为酸性
B.常温下,将pH=11的氨水稀释后,溶液中所有离子的浓度均降低
C.常温下,将pH=11的NaOH溶液和pH=3的HCl溶液等体积混合后,溶液pH=7
D.常温下,物质的量浓度和体积相同的Na2CO3、Na2SO4、HCl 溶液混合后,pH<7