| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《有关氧化还原反应的计算》练习题(六)
参考答案:C 本题解析:A.该浓硝酸的物质的量浓度是C= 本题难度:一般 2、选择题 已知2MOyx-+5S2-+16H+=2M2++5S↓+8H2O,则MOyx-中的x的值为( ) |
参考答案:A
本题解析:根据电子的得失守恒可知5×2=2×n,解得n=5,即MOyx-在反应中得到5个电子,所以化合价是+7价。根据原子守恒可知,y=4,所以x=1,答案选A。
本题难度:一般
3、选择题 下列化学用语表示正确的是
A.CO2分子的比例模型示意图: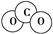
B.三氟化氮的电子式: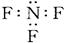
C.二氧化硅的分子式:SiO2
D.含有10个中子的氧原子: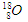
参考答案:D
本题解析:CO2分子的比例模型为 。三氟化氮中每个氟原子还有3对电
。三氟化氮中每个氟原子还有3对电
子对没有参与成键,正确的为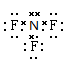 。在二氧化硅中不存在分子,SiO2代表化学式。所以正
。在二氧化硅中不存在分子,SiO2代表化学式。所以正
确的答案是D。
本题难度:简单
4、选择题 一定条件下,等物质的量的下列物质分别与足量的浓盐酸反应,产生Cl2的物质的量最多的是
A.MnO2
B.KClO3
C.KMnO4
D.Ca(ClO)2
参考答案:B
本题解析:4种物质与足量浓盐酸反应的离子方程式分别为2Cl- + 4H+ + MnO2 Mn2+ + Cl2↑+ 2H2O、ClO3-+6H++5Cl-
Mn2+ + Cl2↑+ 2H2O、ClO3-+6H++5Cl- 3Cl2↑+3H2O、2MnO4-+16H++10Cl-
3Cl2↑+3H2O、2MnO4-+16H++10Cl- 2Mn2++5Cl2↑+8H2O、ClO-+2H++Cl-
2Mn2++5Cl2↑+8H2O、ClO-+2H++Cl- Cl2↑+H2O。1molMnO2、KClO3、KMnO4、Ca(ClO)2与足量的浓盐酸反应,产生Cl2的物质的量分别为1mol、3mol、2.5mol和2mol,最多的是KClO3,选B。
Cl2↑+H2O。1molMnO2、KClO3、KMnO4、Ca(ClO)2与足量的浓盐酸反应,产生Cl2的物质的量分别为1mol、3mol、2.5mol和2mol,最多的是KClO3,选B。
考点:考查氧化还原反应的相关计算。
本题难度:一般
5、选择题 金属铜与人体分泌物中的盐酸以及子宫内的空气反应可生成超氧酸:Cu+HCl+O2=Cu Cl+HO2? HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
Cl+HO2? HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A. 氧化剂
氧化剂 是O2
是O2
B.HO2在碱中能稳定存在
C.氧化产物是HO2
D.1 mol Cu参加反应有2 mol电子发生转移
参考答案:A
本题解析:略
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《电解质溶液.. | |