1������� Ϊ�ⶨ�ò�Ѫ����Ʒ[��Ҫ�ɷ��������������壨FeSO4?7H2O��]����Ԫ�صĺ�����ij��ѧ��ȤС�����������ʵ�鷽����
����һ��������KMnO4��Һ�ζ��ⶨ��Ԫ�صĺ���
��1��д���ζ���Ӧ�����ӷ���ʽ______��
��2�����еζ���ʽ�У����������______���гֲ�����ȥ��������ĸ��ţ���
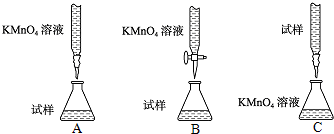
��3��ʵ��ǰ������Ҫȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mL������ʱ��Ҫ����������ƽ�����������ձ�����ͷ�ι��⣬����______�����������ƣ���
��4��ijͬѧ�����ԭ��ص���ʽʵ��Fe2+��Fe3+��ת�����������ҺΪϡ���ᣬ��д�������ĵ缫��Ӧʽ______
������?��FeSO4ת��ΪFe2O3���ⶨ�����仯�����������£�
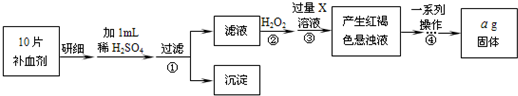
��3��������г���H2O2�����ʹ�õ�������______��
��5��������Ƿ����ʡ��______��������______��
��6���������һϵ�в��������ǣ����ˡ�ϴ�ӡ�______����ȴ��������
��7������ʵ������ģ���ÿƬ��Ѫ������Ԫ�ص�����______g���ú�a�Ĵ���ʽ��ʾ����
�ο��𰸣�����һ����1�����Ը�����ؾ���ǿ�����ԣ���Fe2+����ΪFe3+������ԭΪMn2+��ͬʱ����ˮ����Ӧ���ӷ���ʽΪ5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��
�ʴ�Ϊ��5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��
��2�����Ը�����ؾ���ǿ�����ԣ����Է�����Ƥ�ܣ�Ӧʢ������ʽ�ζ����ڣ�����������Һ�����ԣ�Ӧʢ������ʽ�ζ����ڣ���B����ʣ�
�ʴ�Ϊ��B��
��3����ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250mL������ʱ��Ҫ����������ƽ��ҩ�ס��������ձ�����ͷ�ιܡ�250mL����ƿ��
�ʴ�Ϊ��250mL����ƿ��
��4��ԭ��ظ�����Ӧ������Ӧ��Fe2+�ڸ����ŵ�����Fe3+�������缫��ӦʽΪFe2+-e-�TFe3+��
�ʴ�Ϊ��Fe2+-e-�TFe3+��
��������
��3������ڼ�����ǿ�������Լ����ܽ�Fe2+ȫ������ΪFe3+������H2O2�����ʹ����ˮ�ȣ�
�ʴ�Ϊ����ˮ��
��5��Fe2+��Ӧ���ܱ�֤Fe2+ȫ��ת��ΪFe3+�����Ȳ��ܵõ�������Fe2O3������ȷ����Fe�ĺ������ʲ���ڲ���ʡ�ԣ�
�ʴ�Ϊ�����ܣ�Fe2+��Ӧ���ܱ�֤Fe2+ȫ��ת��ΪFe3+�����Ȳ��ܵõ�������Fe2O3������ȷ����Fe�ĺ�����
��6���������һϵ�д�������������������Һ����ת��Ϊ����������Ҫ���ˡ�ϴ�ӵ�����������Ȼ��������������������ȴ�������������������
�ʴ�Ϊ�����գ�
��7��ag����������Ԫ�ص�������Ϊ10Ƭ��Ѫ������������������ÿƬ��Ѫ������Ԫ�ص�����ag��11216010=0.07ag��
�ʴ�Ϊ��0.07a��
���������
�����Ѷȣ�һ��
2��ѡ���� Ϊ�˳�ȥ����ͭ��Һ�к��е�Fe2+���ʣ��ȼ�����ʵ�������ʹFe2+����ΪFe3+���������������ѡ��
[? ]
A��H2O2��Һ
B��KMnO4��Һ
C��Cl2ˮ
D��HNO3��Һ
�ο��𰸣�A
���������
�����Ѷȣ���
3������� ij�����Ĺ�ҵ��ˮ�к���Fe3+��Cu2+��SO42-�����ӣ�Ϊ�˼�����Ⱦ�����Ϊ���������ƻ��Ӹ÷�ˮ�л��ս���ͭ���õ�����������������������ͼ��ʾ�������Լ���Ϊ��������
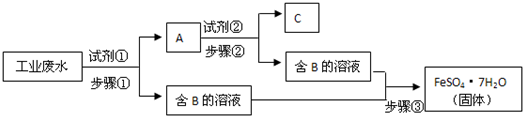
��ش�
��1���Լ���Ӧ����______��A�к��е�������______��������з�����Ӧ�����ӷ���ʽΪ______��
��2������١��ڡ����й�ͬ�ķ����ᴿ������______��������л���Ҫ�ķ����ᴿ������______��
��3��ijͬѧΪ����֤���ڷ��õ�FeSO4?7H2O�����Ƿ���ʣ�ȡ�����ù������Թ��У�������������ˮ���ٵ��뼸��______��Һ�����۲쵽______����֤���ù����Ѿ����ʣ�
�ο��𰸣���1���ӷ�ˮ�л��ս���ͭ���õ������������ۣ���� Ӧ�ü����������������ԭ�����������������������ù������Fe�� Cu������������Ӧ����2Fe3++Fe�T3 Fe2+��Cu2++Fe�TFe2++Cu��
�ʴ�Ϊ�����ۡ�Fe�� Cu��2Fe3++Fe�T3 Fe2+��Cu2++Fe�TFe2++Cu��
��2������١��ڡ����ж��Ǵ���Һ�з�����壬���Թ�ͬ�ķ����ᴿ�����ǹ��ˣ�������Ǵ���Һ����ȡ���ʣ���Ҫ�������ܼ���
�ʴ�Ϊ�����ˡ�������
��3��FeSO4?7H2O������ʻ���Fe3+���ɣ�����Fe3+ �ķ����Ǽ�KSCN��Һ����Һ��죬֤����Fe3+����֤���ù����Ѿ����ʣ�
�ʴ�Ϊ��KSCN����Һ��죮
���������
�����Ѷȣ�һ��
4��ѡ���� X��Y��Z��W����ͼ��ʾ��ת����ϵ����X��Y������
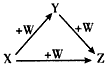
[? ]
��C��CO ��AlCl3��Al(OH)3 ��Fe��FeCl3 ��Na2CO3��NaHCO3
A��ֻ�Т٢�
B��ֻ�Тۢ�
C��ֻ�Т٢ڢ�
D���٢ڢۢ�
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ���з�Ӧ����������ɫ����ɫ�����ɫ������ɫ����ɫ˳�����е���
[? ]
�ٽ������ڴ�����ȼ�ա���FeSO4��Һ�е���NaOH��Һ�����ڿ����з���һ��ʱ�䡡
��FeCl3��Һ�е���KSCN��Һ ����ˮ����ͭ����ҽ�þƾ���
A���ڢۢ٢�?
B���ۢڢ٢�
C���ۢ٢ڢ�?
D���٢ڢۢ�
�ο��𰸣�B
���������
�����Ѷȣ���