1、简答题 A、B、C、D、E为原子序数依次增大的五种短周期元素.E元素最高正价与最低负价的代数和为6,C单质既可与盐酸反应又可与NaOH溶液反应,C、E属同一周期,且能形成1:3型化合物;B原子的最外层电子数比次外层电子数多3;A、D原子序数相差8;若用A、B、D三种元素最高价氧化物分别与足量NaOH溶液反应,在得到的溶液中加入过量稀盐酸,只有一种溶液中能析出白色沉淀Y.
(1)写出E元素和钾元素形成的化合物的化学式______.
(2)C的氧化物与氢氧化钠溶液反应的离子方程式为______.
(3)将红热的A单质投入到B的最高价氧化物对应水化物浓溶液中发生反应的化学方程式为______.
(4)生成白色沉淀Y的离子方程式为______.
(5)在1molD的最高价氧化物形成的晶体中,含有共价键______mol.
参考答案:C单质既可与盐酸反应又可与NaOH溶液反应,应为Al元素,C、E属同一周期,且能形成1:3型化合物,E元素最高正价与最低负价的代数和为6,应为Cl元素,B原子的最外层电子数比次外层电子数多3,应为N元素,A、D原子序数相差8,可为同主族元素,结合原子序数关系可知A为C元素,D为Si元素符合,A、B、D三种元素最高价氧化物分别为CO2、N2O5以及SiO2,与足量NaOH溶液反应,在得到的溶液中加入过量稀盐酸,只有一种溶液中能析出白色沉淀Y,
该沉淀为H2SiO3或H4SiO4,
(1)由以上分析可知E为Cl元素,可与K元素化合生成KCl,故答案为:KCl;
(2)C的氧化物为Al2O3,为两性氧化为,可与碱反应,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)A为C元素,B为N元素,对应的最高价氧化物对应水化物浓溶液为浓硝酸,具有强氧化性,可与C发生反应,反应的化学方程式为C+4HNO3(浓)?△?.?CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)?△?.?CO2↑+4NO2↑+2H2O;
(4)Y为H2SiO3或H4SiO4,反应的离子方程式为SiO32-+2H+=H2SiO3↓或(H2O+SiO32-+2H+=H4SiO4↓),
故答案为:SiO32-+2H+=H2SiO3↓或(H2O+SiO32-+2H+=H4SiO4↓);
(5)D为Si元素,对应的氧化物中,Si原子可与4个O原子形成共价键,则在1molD的最高价氧化物形成的晶体中,含有4mol共价键,故答案为:4.
本题解析:
本题难度:一般
2、简答题 A、B、C为单质,其中一种是金属,通常状况下,A为固体.B为液体(且主要从海水中提取),C为气体,其余均为化合物,X是一种具有挥发性的无氧强酸,E为黑色固体,H为无色液体,它们之间的转化关系如图(其中某些反应条件和产物已略去)
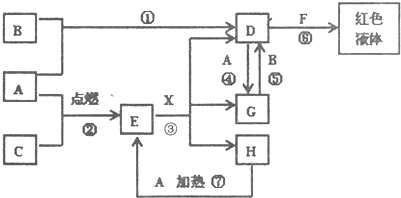
(1)写出:A的化学式______,F的化学式______,H的电子式______.
(2)在反应①-⑦中,不属于氧化还原反应的是______?(填序号).
(3)完成E和X反应的离子方程式:______.
(4)与B同族的元素中最高价氧化物的水化物其酸性最强的是______?(填化学式)
(5)完成H和某种化合物快速制C的化学方程式______,每生成0.15 mol C电子转移______mol.
(6)B蒸气与过量氨气混合有白烟及另一种气体单质产生,该反应的化学方程式为:______.
参考答案:依据转化关系的特征和物质性质分析判断,单质A和H反应生成E为黑色晶体,E黑色固体和X酸反应生成D、G、H,其中DG之间可以实现相互转化,说明A为变价金属Fe,和C在点燃条件下生成黑色固体E为Fe3O4,C为O2,依据D+A=G说明D为含三价铁离子的化合物,F为含硫氰酸根离子的化合物,G为含Fe2+离子的化合物,H为H2O;依据G+B=D分析判断B是强氧化剂,常温下为液体的氧化剂单质判断为:Br2,所以推断D为FeBr3,得到G为FeBr2;X为HBr;
(1)通过以上分析知,A是Fe,F是KSCN,H是H2O,其电子式为:

,故答案为:Fe,KSCN,

;
(2)③⑥的反应中各元素的化合价不变,所以不属于氧化还原反应,故选③⑥;
(3)E是四氧化三铁,X是氢溴酸,四氧化三铁和氢溴酸反应生成溴化铁、溴化亚铁和水,离子反应方程式为:Fe3O4+8H+=Fe2++2Fe3++4H2O,
故答案为:Fe3O4+8H+=Fe2++2Fe3++4H2O;
(4)非金属的非金属性越强,其最高价含氧酸的酸性越强,与B同族的元素中F元素最高价含氧酸,所以最高价氧化物的水化物其酸性最强的是HClO4,故答案为:HClO4;
(5)水和过氧化钠反应生成氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,每生成0.15 mol氧气转移电子的物质的量=2mol1mol×0.15mol=0.3mol,
故答案为:2Na2O2+2H2O=4NaOH+O2↑,0.3;
(6)溴和氨气反应生成溴化铵和氮气,反应方程式为:3Br2+8NH3=6NH4Br+N2,故答案为:3Br2+8NH3=6NH4Br+N2.
本题解析:
本题难度:一般
3、填空题 如图转化关系中A-H为中学常见化合物,甲、乙、丙、丁为常见单质,其中甲、丁常温为气体.已知单质乙、化合物A为黄色(或淡黄色)固体.乙经过连续与甲反应后,再与水化合,是工业上制H的反应过程.B、F两种气体都能使澄清石灰水变浑浊.(部分反应物或产物略去)
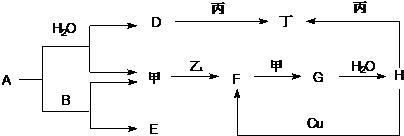
(1)写出下列反应的化学方程式:
A与B______,甲与F______
(2)工业制H时,甲与F反应发生在______(设备名称)
(3)写出丙与D溶液反应的离子方程式______
(4)常温时H的浓溶液与丙物质并不能看到明显的反应现象,原因是______.
参考答案:本题关键是从化合物A是淡黄色固体、单质乙是黄色固体,推断出A为Na2O2,乙为S,判断甲为O2,D为NaOH,F为二氧化硫SO2,G为SO3,H为H2SO4;B、F两种气体都能使澄清石灰水变浑浊,所以推断出B为二氧化碳CO2;E为Na2CO3;丙单质和氢氧化钠反应,也可以和硫酸反应,说明单质为铝;综合分析判断,结合反应,写出个步反应为:
A(Na2O2)+H2O→甲(O2)+D(NaOH);A(Na2O2)+B(CO2)→甲(O2)+E(Na2CO3);甲(O2)+乙(S)→F(SO2)→G(SO3)→H(H2SO4);D(NaOH)+丙(Al)→丁(NaAlO2),H(H2SO4)+丙(Al)→丁(NaAlO2),;所以拍得出的物质分别为:A、Na2O2;B、CO2;D、NaOH;E、Na2CO3;F、SO2;G、SO3;H、H2SO4;甲、O2;乙、S;丙、Al;
(1)A与B发生反应生成碳酸钠和氧气,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;甲与F发生反应生成三氧化硫,化学方程式为:2SO2+O2催化剂.△2SO3
故答案为:2Na2O2+2CO2=2Na2CO3+O2;2SO2+O2催化剂.△2SO3
(2)工业制硫酸时,二氧化硫的催化氧化反应在接触室内完成反应,所以设备名称为接触室,故答案为:接触室;
(3)丙与D溶液反应是金属铝和氢氧化钠反应生成偏铝酸钠和氢气,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)常温下金属铝在浓硫酸中 发生钝化现象,不再继续反应,故答案为:铝在浓硫酸中表面形成致密的氧化膜,阻止内部金属的反应(或铝在浓硫酸中发生钝化);
本题解析:
本题难度:一般
4、填空题 物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,

请按要求回答下列问题。
⑴组成金属A的元素在周期表的位置是_____________,
D的化学式是__________________
⑵写出反应“C→F”的离子方程式?;
⑶写出反应“ I→J”的离子方程式?;
⑷写出金属 H与水蒸气在高温下反应的化学方程式?。
参考答案:(1)第三周期ⅢA族、 HCl
(2)Al3++3NH3・H2O=Al(OH)3+3NH4+
(3)2Fe2++Cl2=2Fe3++2Cl-
(4)3Fe+4H2O=Fe3O4+4H2
本题解析:本题无机框图题,关键是找准突破点。红褐色沉淀K,所以K是氢氧化铁。黄绿色气体E,说明E是氯气,则B是氯化氢,H是铁,I是氯化亚铁,J是氯化铁。A是铝,C是氯化铝,F是氢氧化铝,G是偏铝酸钠。
本题难度:一般
5、选择题 已知甲、乙、丙、X是4种中化学中常见的物质,其转化关系符合如图。则甲和X不可能的是?
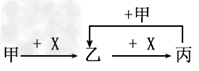
[? ]
A.C和O2?
B.Cl2和Fe?
C.AlO2-?溶液和CO2?
D.SO2和NaOH溶液
参考答案:C
本题解析:
本题难度:一般