1������� ��1���������������������£��о��ı���ʼ�������ʵ�������n��H2����ʾ�ݶ�N2(g)��3H2(g) 2NH3(g)��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ����ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������
2NH3(g)��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ����ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������
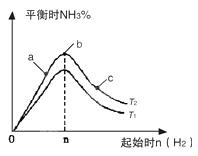
�ٱȽ���a��b��c����������ƽ��״̬�У���Ӧ��N2��ת������ߵ���__________��
���������ݻ�Ϊ1L��n��3mol����Ӧ�ﵽƽ��ʱN2��H2��ת���ʾ�Ϊ60%��������ʼʱ��ϵ�м���N2�����ʵ���Ϊ__________mol���������£�T2������Ӧ��ƽ�ⳣ��K��_________�����¶�����ʱ��ƽ�ⳣ����__________��
��ͼ����T2��T1�Ĺ�ϵ��__________��������ڡ��������ڡ��������ڡ�������ȷ��������
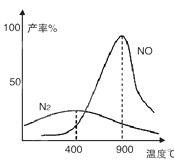
��2��������������145��Ϳ�ʼ��Ӧ���ڲ�ͬ�¶Ⱥʹ������������ɲ�ͬ�����ͼ����
4NH3��5O2 4NO��6H2O ��4NH3��3O2
4NO��6H2O ��4NH3��3O2 2N2��6H2O
2N2��6H2O
�¶Ƚϵ�ʱ������__________Ϊ�����¶ȸ���900��ʱ��NO�����½���ԭ����___________________
�ο��𰸣���14�֣���1����c?��1��K=25/12��2.08����С�۵���?����2�֣�
��2��N2��������������NO�ķ�Ӧ�Ƿ��ȷ�Ӧ�������¶�ת�����½�?����2�֣�
�����������1��������ʱ�¶���ͬ��������Խ������ת����Խ����c���ת������ߣ��ʴ�Ϊ��c��
��N2��g��+3H2��g�� 2NH3��g��
2NH3��g��
��ʼ x? 3? 0
ת��0.6 ?1.8? 1.2
ƽ��x-0.6? 1.2? 1.2
N2��ת����Ϊ60%����
0.6mol/x��100%=60%�����x=1mol��
��Ӧ��ƽ�ⳣ��K=(1.2mol��L��1)2/0.4mol��L��1��(1.2mol��L��1)3=2.08��mol��L��1���D2��
��ͼ��֪���¶ȵͰ����ĺ�����������ӦΪ���ȷ�Ӧ���������¶���ƽ�ⳣ����С��
�ʴ�Ϊ��1��2.08��mol��L��1���D2����С��
����ͼ��֪������������ͬʱ��T1�ȴﵽƽ����ƽ��ʱ������Ũ��С����T2����T1���ʴ�Ϊ�����ڣ�
��2������ͼ���֪�¶ȵ�ʱ���ɵ������¶ȸ�ʱ����NO�����÷�ӦΪ���ȷ�Ӧ�����¶ȸ���900��ʱ��NO�����½����ʴ�Ϊ��N2��������������NO�ķ�Ӧ�Ƿ��ȷ�Ӧ�������¶�ת�����½���
�����Ѷȣ�һ��
2������� �������ʵ�����A��B�����2L���ܱ������з�����Ӧ3A��g��+B��g���TxC��g��+2D��g������5min���D��Ũ��Ϊ0.5mol?L-1��c��A����c��B��=3��5��C��ƽ����Ӧ������0.1mol/��L?min������
��1����ʱ��A�����ʵ���Ũ��Ϊ______��
��2����Ӧ��ʼǰ������A��B�����ʵ���Ϊ______��
��3��B��ƽ����Ӧ����Ϊ______��
��4��x��ֵΪ______��
�ο��𰸣�D��Ũ��Ϊ0.5mol/L������D�����ʵ���Ϊ1mol��
��A��B�����ʵ���Ϊnmol��
3A��g��+B��g��=xC��g��+2D��g����
��ʼ n mol n mol 0 0
��Ӧ 1.5mol 0.5mol1mol
5min ��n-1.5��mol�� n-0.5��mol 1mol
ͬһ�����У�c��A����c��B��=n��A����n��B��=n-1.5n-0.5=35��n=3mol��
��1��A��5minĩ�����ʵ���Ϊ����n-1��5��mol=1.5mol�������ʵ���Ũ��Ϊ0.75mol/L���ʴ�Ϊ��0.75mol/L��
��2���ɼ����֪n=3mol���ʴ�Ϊ��3mol��
��3��C�ķ�Ӧ������0.1mol/��L?min��������ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�����B�ķ�Ӧ������0.05mol/��L?min����
�ʴ�Ϊ��0.05mol/��L?min����
��4��D��Ũ��Ϊ0.5mol/L����Ӧʱ��Ϊ5min��D�ķ�Ӧ����Ϊ0.1mol/��L?min����C�ķ�Ӧ������0.1mol/��L?min��������ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�����x=2���ʴ�Ϊ��2��
���������
�����Ѷȣ���
3��ѡ���� ����ͬ�¶Ⱥ�ѹǿ�£��Է�ӦCO2(g)��H2(g)  CO(g)��H2O(g)���мס��ҡ�����������ʵ�飬ʵ����ʼʱ���������ڸ���ֵ����ʵ������±���
CO(g)��H2O(g)���мס��ҡ�����������ʵ�飬ʵ����ʼʱ���������ڸ���ֵ����ʵ������±���

������������ﵽƽ���n(CO)�Ĵ�С˳����(����)
A���ң����������ס���������
B���ң������ף���
C�������ң�������
D�����������ң���
�ο��𰸣�A
������������ݷ�Ӧ����ʽ��
CO2(g)��H2(g)  CO(g)��H2O(g)
CO(g)��H2O(g)
�ף�? a mol?a mol?0 mol?0 mol
�ң�? 2 a mol? a mol?0 mol?0 mol
����? 0 mol?0 mol ?a mol?a mol
����? a mol?0 mol?a mol?a mol
���ݼ��˼����˼�룬������ȫ��ת��Ϊ��Ӧ����ּͱ��м�������ʵ���һ�����ҺͶ��м�������ʵ���һ������˼ͱ����ҺͶ����ڵ�Чƽ�⣬�ﵽƽ���CO�����ʵ������ף������ң������Һͼ���ȣ����൱���ڼĻ����϶����a mol CO2������Ӧ���Ũ�ȣ�ƽ�����ƣ���˴ﵽƽ���CO�����ʵ�����>�ף���n(CO)�Ĵ�С˳��Ϊ���ң���>�����ס�
�����Ѷȣ�һ��
4��ѡ���� ������ʵ��������������ԭ�����͵���
A�������Ȼ�����Һʱ����������ϡ����
B�������Ȼ�������Һʱ������������м
C���ں��з�̪�İ�ˮ�м�������NH4Cl,��Һ��ɫ���dz
D��������ͭ������Һ�м���һ�鵨�����������α����
�ο��𰸣�B
�������������ı�Ӱ��ƽ���1��������ƽ������ܹ��������ָı�ķ�����У����������������ԭ������ԭ�����������е�ƽ����ϵ��A���Ȼ�������ˮ��������ˮ�⣬���������Ȼ�����Һʱ����������ϡ�����Ŀ��������������ˮ�⣬A���������⣻B���������Ӽ��ױ��������������ӣ����������Ȼ�������Һʱ������������м��Ŀ���Ƿ�ֹ�������ӱ���������ƽ����ϵ��B�������⣻C����ˮ�д��ڵ���ƽ�⣬����ں��з�̪�İ�ˮ�м�������NH4Cl��Һ�����ư�ˮ�ĵ��룬��Һ�ļ��Խ�����ɫ���dz��C���������⣻D������ͭ����ˮ�����ܽ�ƽ�⣬���������ͭ������Һ�м���һ�鵨�����������α����D���������⣬��ѡB��
�����Ѷȣ�һ��
5��ѡ���� ��ͼ���¶Ⱥ�ѹǿ��X+Y 2Z��ӦӰ���ʾ��ͼ��ͼ���������ʾƽ����������Z���������������������ȷ����
2Z��ӦӰ���ʾ��ͼ��ͼ���������ʾƽ����������Z���������������������ȷ����
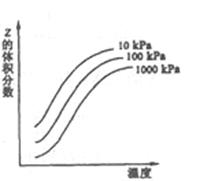
A��X��Y��Z��Ϊ��̬
B������ʱ�����������ܶȿ���Ϊ�˷�Ӧ�Ƿ�ﵽ��ѧƽ��[���ж�����
C�������¶�ʱ ����
����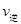 ��С��ƽ�������ƶ�
��С��ƽ�������ƶ�
D��ʹ�ô���Z�IJ�������
�ο��𰸣�B
�������������ͼ���֪�������¶ȵ����ߣ�������Z�ĺ��������ߣ����Է�Ӧ�����ȷ�Ӧ���������¶ȣ����淴Ӧ���ʾ������ӵģ�C����ȷ�����¶���ͬʱ��ѹǿԽ��������Z�ĺ���ԽС����˵������ѹǿ��ƽ�����淴Ӧ�����ƶ���˵������Ӧ���������ķ�Ӧ����X��Y��Z��Ϊ��̬����Ӧǰ�������������䣬A����ȷ������Zһ�������壬X��Y��ֻ����һ�������塣�ܶ��ǻ�����������������ݻ��ı�ֵ����Ӧ�����������DZ仯�ģ����Ե��ܶȲ��ٷ����仯ʱ������˵����Ӧ�ﵽƽ��״̬��C��ȷ���������ܸı�ƽ��״̬��D����ȷ������B��
�����Ѷȣ�һ��