1、选择题 在两份体积相同的氢氧化钠和稀硫酸溶液中分别加入过量铝粉,充分反应后,在相同状况下,若放出氢气的体积相同,则该氢氧化钠溶液与硫酸溶液的物质的量浓度之比为( )
A.3:1
B.1:3
C.2:3
D.3:2
参考答案:令生成的氢气的物质的量为3mol,则:
2Al+3H2SO4=2Al2(SO4)3+3H2↑
3mol 3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2mol 3mol
氢氧化钠和稀硫酸溶液的体积相等,所以所取氢氧化钠和稀硫酸溶液的浓度比等于溶质NaOH、H2SO4的物质的量的之比,即为2mol:3mol=2:3.
故选C.
本题解析:
本题难度:简单
2、选择题 相同物质的量的下列物质分别与等浓度的足量的NaOH溶液反应,消耗碱量最多的是
A.Al2O3
B.Al(OH)3
C.AlCl3
D.Fe(NO3)3
参考答案:C
本题解析:略
本题难度:简单
3、填空题 由铝和某些金属氧化物组成的混合物在化学上称为铝热剂,该混合物在高温条件下能发生置换反应。为确定某铝热剂样品(铝和氧化铁)的组成,分别进行下列实验:
(1)若取10.7 g该样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为a L。反应的化学方程式是?,样品中铝的质量分数是?(用含a的表达式表示)。
(2)若取同质量的样品,在高温下使其恰好反应,则a =?L;该反应的化学方程式是?。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为b L,该气体与(1)中所得气体的体积比a∶b =_______。
参考答案:⑴ 2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑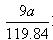 或0.075a
或0.075a
⑵ 3.36? 2 Al+ Fe2O3 2Fe + Al2O3
2Fe + Al2O3
⑶ 3∶2
本题解析:略
本题难度:简单
4、填空题 某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。

请回答下列问题。
(1)?图中涉及分离溶液与沉淀的方法是____________________________。
(2)? B、C、D、E四种物质的化学式为:
B__________、C__________、D__________、E__________。
(3) 写出下列反应的离子方程式:
沉淀F与NaOH溶液反应________________________________。
沉淀E与稀硫酸反应____________________________。
溶液G与过量稀氨水反应________________________________。
参考答案:(1) 过滤?(2) B:? Al2O3? C:? Fe2O3? D:? NaAlO2? E: Al(OH)3
(3) Al2O3+2OH-=AlO2-+H2O; Al(OH)3+3H+=Al3++3H2O;Al3++3NH3・H2O=3NH4++Al(OH)3↓
本题解析:Al2(SO4)3、Al2O3和Fe2O3中Al2(SO4)3溶于水,Al2O3溶于NaOH,可确定B:? Al2O3? C:? Fe2O3? D:? NaAlO2? E: Al(OH)3。
本题难度:一般
5、填空题 (10分)镁的化合物具有广泛用途,请回答有关镁的下列问题:
(1) 单质镁在空气中燃烧的主要产物是白色的_________,还生成少量的_____(填化学式);
(2) 物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸
镁),反应后容器内固体物质的质量不可能为:??
A.3.2g
B.4.0g
C.4.2g
D.4.6g