1、选择题 镁粉是制备焰火的原料,工业上通过冷却镁蒸气制得镁粉。下列气体中,可以用来冷却镁蒸气的是(? )
A.氩气
B.二氧化碳
C.氧气
D.空气
参考答案:A
本题解析:注意可用作镁蒸气的冷却剂不能和镁发生反应。镁和二氧化碳可发生反应生MgO和C,镁和氧气可反应生成MgO,成分有氮气,镁和空气的中氮气反应生成Mg3N2, 镁和惰性气体氩气不反应,故A项正确。
点评:熟悉金属镁的主要化学性质
本题难度:简单
2、选择题 将相同质量的Na、Mg、Al、Zn、Fe分别投入足量的稀盐酸中,置换出的H2按由多到少的顺序排列正确的是(? )
A.Zn>Fe>Na>Mg>Al
B.Al>Mg>Na>Fe>Zn
C.Na>Mg>Al>Fe>Zn
D.Fe>Zn>Mg>Al>Na
参考答案:B
本题解析:本题有以下3种解法。
方法一(设“一”法):设分别取Na、Mg、Al、Zn、Fe各1 g放入足量稀盐酸中。则:
(1)2Na+2H+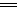 2Na++H2↑
2Na++H2↑
46 g?2 g
1 g?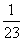 g
g
(2)Mg+2H+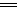 Mg2++H2↑
Mg2++H2↑
24 g? 2 g
1 g?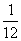 g
g
(3)2Al+6H+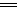 2Al3++3H2↑
2Al3++3H2↑
54 g? 6 g
1 g?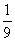 g
g
(4)Zn+2H+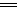 Zn2++H2↑
Zn2++H2↑
65 g?2 g
1 g?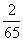 ?g
?g
(5)Fe+2H+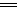 Fe2++H2↑
Fe2++H2↑
56 g? 2 g
1 g?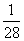 ?g
?g
比较数的大小顺序便可得到答案。
方法二(排除法):在方法一中只进行前三种计算,便知答案。
方法三(摩尔电子质量法):对方法一进行总结,可以发现以下规律:
等质量金属与足量酸反应,金属的相对原子质量与反应后金属化合价的比值(即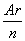 ,n为反应后金属的化合价)越小,生成H2越多;反应中,转移1 mol电子,需要金属的质量越小,等质量金属与酸反应生成H2越多。
,n为反应后金属的化合价)越小,生成H2越多;反应中,转移1 mol电子,需要金属的质量越小,等质量金属与酸反应生成H2越多。
本题难度:简单
3、选择题 以下有关正三价铝的叙述正确的是
[? ]
A.当向溶液中加入强酸溶液时,氢氧化铝主要发生酸式电离
B.当向溶液中加入强碱溶液时,氢氧化铝主要发生碱式电离
C.在强酸性环境中正三价的铝以Al3+形式存在于溶液中
D.在pH较大的溶液中正三价的铝以Al3+形式存在于溶液中
参考答案:C
本题解析:
本题难度:简单
4、填空题 (1)物质X是中学化学中的常见物质,X既能与稀硫酸反应,又能与烧碱溶液反应。
① 若X为氧化物,X的化学式是____________。
② 若X为单质,X用于焊接钢轨反应的化学方程式是_________________________。
③ 若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。X与稀硫酸反应的离子方程式是_________________________;X与足量稀氢氧化钠溶液反应的离子方程式是_________________________。
(2)科学家设计出新的航天飞船内的空气更新系统。其中一步是A和氢气在200℃~250℃时,镍催化剂作用下,生成甲烷和另一种物质。该反应的化学方程式是_________________________。
参考答案:(1)①Al2O3;②2Al+Fe2O3 2Fe+Al2O3;③HCO3-+H+==H2O+CO2↑;NH4++HCO3-+2OH-==
2Fe+Al2O3;③HCO3-+H+==H2O+CO2↑;NH4++HCO3-+2OH-==
NH3・H2O+CO32-+H2O
(2)CO2+4H2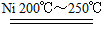 CH4+2H2O
CH4+2H2O
本题解析:
本题难度:一般
5、选择题 在①Al?②Al(OH)3?③H2SO4?④?NaHCO3?⑤Na2CO3中,与盐酸和氢氧化钠溶液均可反应的是?
[? ]
A.①②④?
B.①③⑤?
C.①②③④?
D.②④⑤
参考答案:A
本题解析:
本题难度:简单