1��ѡ���� ij�¶��£�������ͨ��NaOH��Һ�У���Ӧ�õ�NaCl��NaClO��NaClO3�Ļ����Һ����֪������NaOH��һ���¶����ܷ�����Ӧ��3Cl2+6NaOH=5NaCl+NaClO3+3H2O�������ⶨClO-��ClO3-�����ʵ���֮��Ϊ1��3�����������������Ʒ�Ӧʱ������ԭ����Ԫ�غͱ���������Ԫ�ص����ʵ���֮��Ϊ��������
A��21��5
B��11��3
C��3��1
D��4��1
�ο��𰸣�����ClO-��ClO3-��Ũ��֮��1��3����Cl��ClO-��ʧȥ1�����ӣ���Cl��ClO3-��ʧȥ5�����ӣ�һ��ʧȥ1+3��5=16�����ӣ���Cl��Cl-���õ�1�����ӣ���Ҫ16��ԭ�Ӳ��ܵõ�16�����ӣ����ԣ�����ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��=16����1+3��=4��1��
��ѡ��D��
���������
�����Ѷȣ�һ��
2�������� ij�о���ѧϰС�������һϵ�л�ѧʵ����ָ�����طֽ��ĺ���Ԫ�صĻ����ﶼ�ܺ�Ũ���ᷴӦ�Ƶ��������̻�����Ļ�ԭ���ﶼ��MnCl2���磺K2MnO4+8HCl= MnCl2+2Cl2��+2KCl+4H2O���������ֽ���������һЩ�йض�����ʵ�飬��Ҫ����ջ���㣨����������ۺϳɱ�״������
��1����ȡ��31.6gKMnO4��ĩ�������Թ��м��ȳ�ַ�Ӧ���ռ�������������?����ȡ31.6gKMnO4��ĩ���������ᷴӦ���ռ������������?��
��2����31.6gKMnO4��ĩ����һ��ʱ�䣬�ռ���1.12L�����ֹͣ���ȣ���ȴ�����������Ũ�����ټ��ȣ����ռ������������?��
��3����a molKMnO4��ĩ����һ��ʱ�䣬�ռ���V1L�����ֹͣ���ȣ���ȴ�����������Ũ�����ټ��ȷ�Ӧ��ֺ����ռ����������V2L����V2��?
����a��V1�����
�ο��𰸣���1��11.2L��2�֣���5.6L��2�֣���2��8.96L��2�֣���3��V2=56a ��2V1��2�֣�
���������
��1��?2KMnO4====K2MnO4+MnO2+O2�� 2KmnO4+16HCl=2KCl+2MnCl2+5Cl2��+8H2O
ֱ�Ӵ�����㼴�ã������ס�
��2��?��31.6gKMnO4��ĩ����һ��ʱ�䣬�ռ���1.12L����϶�����������ֹͣ���ȣ���ȴ�����������Ũ�����ټ��ȣ����ռ���������������������з���ʽ��������׳��������ǿ����õ�ʧ�����غ����㣺����1.12L����ʧ4��0.05mole,��������XmolCl2,��ʧȥ2��Xmole,��KMnO4��������Mn2+�õ�5 ��0.2=1mole,0.2+2X=1,X=0.4,��8.96L
��3��?�����õ�ʧ�����غ����㣺��a molKMnO4��ĩ����һ��ʱ�䣬�ռ���V1L����϶�����������ֹͣ���ȣ���ȴ�����������Ũ�����ټ��ȷ�Ӧ��ֺ����ռ����������V2L�϶�����������V1/22.4��4+ V2/22.4��2=5 a, V2=56a ��2V1
�����Ѷȣ�һ��
3��ʵ���� ��11�֣�Ϊ��̽��Cl2��SO2ͬʱͨ��H2O�����ķ�Ӧ��ijУ��ѧ��ȤС��ͬѧ���������ͼ��ʾ��ʵ��װ�á�
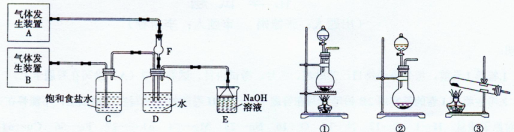
����գ�
��1���û�ѧ��ȤС���ͬѧΪ��ȡCl2��SO2���壬�ֲ���Na2SO3��70%��Ũ����Ϊԭ����ȡSO2������MnO2��Ũ���ᣨ12 mol��L-1��Ϊԭ����ȡCl2���ڴ�ʵ���У�F������������?�����巢��װ��BӦѡ��١��ڡ�������װ���е�?��ѡ����ţ���
��2��Dװ������Ҫ��Ӧ�����ӷ���ʽΪ��?��
��3��Ϊ��֤ͨ��Dװ����������Cl2��������SO2��������ȤС���ͬ!ѧ���������Լ����Ȼ�����Һ���Ȼ�������Һ�����軯����Һ��������Һ��Ʒ����Һ�����Ը��������Һ��
��Cl2����ȡ����D����Һ�μ���ʢ��?���Լ����ƣ���ͬ�����Թ��У��ټ��������������?��˵��Cl2������
��SO2������ȡ����D����Һ�μ���ʢ��?���Թ��ڣ�������������?��
�ο��𰸣�

���������
�ŷ�����?��Cl2ѡ ��?��Cl2��SO2��2H2O=4H����2Cl�D��SO42�D;��Cl2�ܽ�FeCl2������SO2���ܣ�����ѡ���Ȼ�������Һ��KSCN��C6H5OH����Һ����Һ�ʺ�ɫ����ɫ��������KMnO4��Һ����ɫ��ɫ��
�����Ѷȣ�һ��
4������� ��10�֣���ͼ��ʾ��ӦI����ӦII�ͷ�ӦIII���ǹ�ҵ�����г����ķ�Ӧ������A��BΪ�����C����������֮һ��D��K���������������H������ΪҺ̬�����J��һ�־���Ư�����õ��Σ���ӦIII��E��G��Ӧ��ԭ����ͬ��
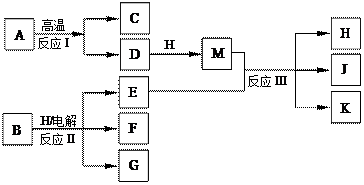
��1��C��J��ˮ��Һ��Ӧ�����ɵĺ�����ĵ���ʽ��?��
��2�� E��G��Ӧ�����ӷ���ʽ��?��
E��G��Ӧ�����ӷ���ʽ��?��
��3��J���ú��㲻�Ӵ�ˮ������������Ҳ�ֽ�����K�����ų����壬�÷�Ӧ�Ļ�ѧ����ʽ��?��
��4����ҵ�ϲⶨ��ӦIII��Ʒ����Ч�ɷ�J�ĺ������Ƚ�һ�����IJ�Ʒ����Һ���������KI��Һ��ϡ�����У�ʹ֮��Ӧ����I2��Ȼ����Na2S2O3����Һ�ζ�I2������������
����Na2S2O3����Һ�ζ�I2ʱѡ�õ�ָʾ����?��
������I2�ķ�Ӧ�����ӷ���ʽ��?��
�ο��𰸣���10�֣�ÿ��2�֣�
��1��
 ?
?
��2��Cl2 + 2OH�� ?Cl��+ ClO��+ H2O
?Cl��+ ClO��+ H2O
��3��Ca(ClO)2 ="=" CaCl2 +O2��
��4���ٵ�����Һ?�� ClO��+ 2I��+2H+��Cl��+ I2 + H2O
ClO��+ 2I��+2H+��Cl��+ I2 + H2O
�����������
�����Ѷȣ�һ��
5������� ����������š��ˮ��ͷ��ʱ�ྻ������ˮ������������ʱ��������������ˮ������������ͼ����ɽ������ˮ��˾������������ͼ��
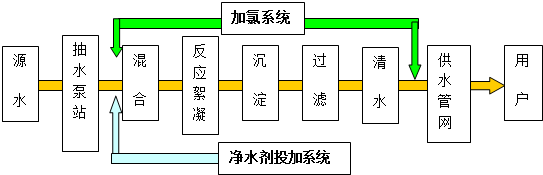
��ش��������⣺
��1����ˮ��վ��Դˮ���𣬼���ϵͳ���ȣ�Ŀ����______��
��2������______����ˮ����
��3����ͼΪ���˳أ���ʵ����Ҫ��ɹ��ˣ���Ҫ�IJ���������______��______��______��
�ο��𰸣���1���������̷���������ϵͳ���ȣ�Ŀ��������������ˮ��Ӧ��������ʹ����ᣬ���������ǿ������ɱ��������
�ʴ�Ϊ��ɱ��ˮ�еIJ�����
��2��������ˮ��Һ��ˮ�����ɵ��������������������������ˮ�е��������ã����Գ�ѡ����������ˮ����
�ʴ�Ϊ������[��KAl��SO4��2?12H2O]��
��3��������Ҫ�IJ�������Ϊ©�����ձ������������ʴ�Ϊ��©�����ձ�����������
���������
�����Ѷȣ�һ��