1、填空题 某元素的同位素MZX,已知M=30,且M-Z=16,则:
(1)X元素为_______。?
(2)X的气态氢化物电子式?。
(3)X单质与强碱溶液反应的化学方程式____?。
(4)X的氧化物与酸反应的化学方程式?。
参考答案:(1)Si?(2)略
(3)Si+2NaOH+H2O=Na2SiO3+2H2↑
(4)SiO2+4HF=SiF4+2H2O
本题解析:略
本题难度:简单
2、选择题 设X、Y、Z代表三种元素。已知:
(1) 和
和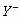 两种离子具有相同的电子层结构;
两种离子具有相同的电子层结构;
(2)Z元素原子核内质子数比Y元素原子核内质子数少9个;
(3)Y和Z两种元素可以形成4核42电子的 价阴离子。
价阴离子。
据此,请填空:
(1)Y元素是___________,Z元素是_____________。
(2)由X、Y、Z三种元素所形成的含68个电子的盐类化合物的化学式是______。
参考答案:(1)氯、氧(2)
本题解析:考查原子结构与元素推断,依题意,假设Y元素的原子序数为y,则Z元素的原子序数为 。若以
。若以 表示由这两种元素所形成的4核42电子的
表示由这两种元素所形成的4核42电子的 价阴离子,则下列关系式成立:
价阴离子,则下列关系式成立:
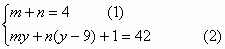
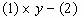 得
得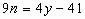
所以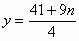
因为n为整数,将其可能的取值1、2和3分别代入上式,经检验确定: ,
,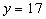 。所以,Y元素的原子序数为17,它是氯元素,而元素Z的原子序数
。所以,Y元素的原子序数为17,它是氯元素,而元素Z的原子序数 ,它是氧元素,进而可知X元素为钾元素,这三种元素所形成的含68个电子的盐类化合物的化学式为
,它是氧元素,进而可知X元素为钾元素,这三种元素所形成的含68个电子的盐类化合物的化学式为 (所含电子数为:
(所含电子数为: )
)
本题难度:简单
3、填空题 (本题共10分) A、B、C、D 四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。则元素:A为??B为?C为?,D的质子数和中子数相等,D 的原子符号为:?,它的最高价氧化物对应的水化物:?。
参考答案:C O N? S H2SO4
本题解析:B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,淡黄色固体化合物为Na2O2 ;B为O,C为Na ;原子序数是依次增大的,所以A为C,D的L层电子数等于K、M两个电子层上电子数之和,L层电子数为8,K层电子数等于为2,M层电子数等,6,D为S。
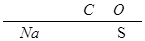
本题难度:一般
4、选择题 长式周期表共有18个纵行,从左到右排为1-18列,即碱金属为第一列,稀有气体元素为第18列。按这种规定,下列说法正确的是
A.第9列中元素中没有非金属元素
B.只有第二列的元素原子最外层电子排布为ns2
C.第四周期第9列元素是铁元素
D.第10、11列为ds区
参考答案:A
本题解析:第9列中元素是原来的第Ⅷ族元素,全部是金属,A正确;B不正确,例如He也满足;C不正确,第四周期第9列元素是钴元素;D不正确,应该是第11、12列为ds区,答案选A。
点评:该题是基础性试题的考查,试题存在考查知识对周期表结构的了解掌握情况,难度不大。该题的关键是熟练记住周期表的结构,有利于培养学生的灵活应变能力和知识的迁移能力。
本题难度:一般
5、填空题 (12分)A、B、C、D、E、F均为元素周期表前20号主族元素,其核电荷数依次增大。其中A、B同周期,B、D同主族且相邻,A、B、D三种元素的核电荷数之和为30。C、E同周期,可形成1:1型的离子化合物。F的最外层电子数大于1。请回答:
(1)A、B、C、D、E、F六种元素的元素符号分别为_______________________?__;
(2)用化学式表示A、D、E最高价氧化物的水化物酸性由强到弱的顺序:_______;
(3)用化学式表示D、E氢化物的还原性由强到弱的顺序:_______;
(4)请写出C、E最高价氧化物对应水化物之间反应的化学方程式:________________。
参考答案:(共12分)(1)C、O、Na、S、Cl、Ca (各1分)(2)HClO4>H2SO4>H2CO3 ?(2分)(3)H2S> HCl(2分)?(4)HClO4 + NaOH ==NaClO4 + H2O(2分)
本题解析:B、D同主族且相邻,则B是第二周期,D是第三周期。C、E同周期,可形成1:1型的离子化合物,则该化合物应该是氯化钠或硫化镁。如果是硫化镁,则BD的原子序数之和就≤22,则A的原子序数最小是8,这和A的原子序数小于B的矛盾,所以C是钠,E是氯,则A是碳,B是氧元素,D是硫元素,F是钙。
(1)分别是C、O、Na、S、Cl、Ca。
(2)非金属性越强,最高价氧化物的水化物的酸性越强,非金属性是Cl>S>C,则酸性强弱顺序是HClO4>H2SO4>H2CO3。
(3)非金属性越强,相应氢化物的还原性越弱,所以还原性强弱顺序是H2S> HCl。
(4)C、E最高价氧化物对应水化物分别是强酸和强碱,方程式为HClO4 + NaOH ==NaClO4 + H2O。
本题难度:简单