1、填空题 接触法制硫酸的核心反应是2SO2(g)+O2(g)?2SO3(g)△H<0.
(1)该反应的平衡常数K值的表达式:K=______;升高温度,K值将______(填“增大”、“减小”、“不变”)
(2)生产中用过量的空气能使SO2的转化率______(填“增大”、“减小”、“不变”),该反应为何在常压下进行______.
2、选择题 对于在一定条件下进行的可逆反应:2SO2+O2 2SO3,改变下列条件,可以提高反应物中活化分子百分数,但不改变SO2的转化率的是
2SO3,改变下列条件,可以提高反应物中活化分子百分数,但不改变SO2的转化率的是
[? ]
A.升高温度?
B.增大压强?
C.使用催化剂?
D.增大反应物浓度
3、填空题
寻找理想的新能源和更加有效的利用已有能源是现在能源问题研究的两个主要方向。
I.实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为_________(填序号)。
A.2H2(g)+O2(g)=2H2O(l) △H=-142.9kJ/mol
B.H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol
C.2H2+O2=2H2O(l) △H=-571.6kJ/mol
D.H2(g)+1/2O2(g)=H2O(g) △H=-142.9kJ/mol
Ⅱ.某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤:
①CaBr2+H2O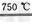 CaO+2HBr
CaO+2HBr
②2HBr+Hg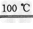 HgBr2+H2↑
HgBr2+H2↑
③HgBr2+___ ___+___
___+___
④2HgO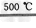 2Hg+O2↑
2Hg+O2↑
请你根据“原子经济”的思想完成上述步骤③的化学方程式:__________________;根据“绿色化学”的思想评估该方法制H2的主要缺点:________________
Ⅲ.氢气通常用生产水煤气的方法制得,其中CO(g)+ H2O(g) CO2(g)+H2(g) △H<0。在850℃时,K=1。
CO2(g)+H2(g) △H<0。在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K____(填“大于”“小于”或“等于”)1。
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO、3.0molH2O、1.0molCO和xmolH2,则:
①当x=5.0时,上述平衡向___(填“正反应” 或“逆反应”)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是____。
(3)在850℃时,若设x=5.0mol和x=6.0mol,其他物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a____(填“大于”“小于”或“等于”)b。
4、填空题 合成氨工业的核心反应是:N2(g)+3H2(g) 2NH3(g) △H=Q kJ/mol。反应过程中能量变化如图所示,回答下列问题:
2NH3(g) △H=Q kJ/mol。反应过程中能量变化如图所示,回答下列问题:
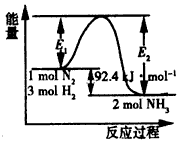
(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_______,E2______(填“增大”、“减小” 或“不变”)。
(2)在500℃、2×107Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5mol H2,充分反应后,放出的热量____(填“<”、“>”或“=”)46.2 kJ,理由是_____________________。
(3)关于该反应的下列说法中,正确的是_______。
A.△H>0,△S>0 B.△H>0,△S<0 C.△H<0,△S>0 D.△H<0,△S<0
(4)将一定量的H2(g)和N2(g)放入1L密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.10 mol,H2 为0.30 mol,NH3为0.10 mol。则该条件下达到平衡时H2转化为NH3的转化率为___________。该温度下的平衡常数K的值为__________。若升高温度,K值______(填 “增大”、“减小”或“不变”)。
(5)在上述(4)反应条件的密闭容器中,欲提高合成氨的转化率,下列措施可行的是______(填字母)。
A.向容器中按原比例再充入原料气 B.向容器中再充入惰性气体 C.改变反应的催化剂 D.分离出氨
5、选择题 在密闭容器中发生下列反应aA(g)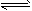 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
[? ]
A.A的转化率变大
B.平衡向正反应方向移动
C.D的体积分数变大
D.a <c+d