| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《化学实验》考点强化练习(2019年押题版)(二)
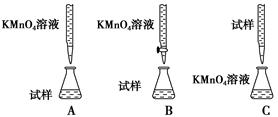 方案二 重量法 操作流程如下: 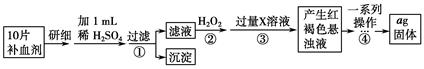 (4)步骤②中除用H2O2外还可以使用的物质是__________________________。 (5)步骤②是否可以省略________,理由是________________________________ _______________________________________。 (6)步骤④中一系列操作依次是:过滤、洗涤、________、冷却、称量。 (7)假设实验无损耗,则每片补血剂含铁元素的质量________g(用含a的代数式表示)。 参考答案:(1)250 mL容量瓶 (2)A (3)B (4)氯水(等其他合理的氧化剂) (5)不能 因为Fe2+与碱反应后在空气中加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量 (6)灼烧 (7)0.07a 本题解析:(1)据题意,配制一定物质的量浓度的KMnO4溶液250 mL,还需250 mL容量瓶(必须带上容量瓶的规格)。(2)由于高锰酸钾有强氧化性不能用盐酸酸化,也不用强氧化性酸(硝酸)酸化,通常用稀硫酸酸化。(3)由于高锰酸钾有强氧化性会腐蚀橡皮管,故只能用酸式滴定管(B装置)进行滴定实验。(4)除用H2O2外还可以使用氯水氧化Fe2+,不引入新的杂质离子。(5)因为Fe2+与碱反应后在空气中加热不能得到纯净的Fe2O3,无法准确计算Fe的含量,所以必须先用H2O2氧化Fe2+来实现。(6)步骤④依次将Fe(OH)3过滤、洗涤、灼烧(Fe(OH)3分解得Fe2O3、冷却、称量。(7)每片补血剂含铁元素的质量:a g÷160 g・mol-1×2×56 g・mol-1÷10片=0.07a g/片 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《氧化性和还.. | |