1、简答题 正确实验操作是实验成功关键请按要求完成下列各题
药品的取用
(1)药品取用“三”原则:
①“三不原则”:______.
②节约原则:______.
③处理剩余化学药品原则:______.
(2)药品取用方法(往试管里加固体药品或倾倒液体药品)
固体药品:①块状:用______夹取;操作要领是:“一平、二放、三慢竖”(将试管横放.用镊子将块状固体药品放入试管口,然后慢慢地将试管竖立起来,使块状固体缓缓滑至试管底部).
②粉末状:用______(或______)取用;操作要领是:“一斜、二送、三直立”(将试管倾斜,把盛有药品的药匙或纸槽送入试管底邵,然后使试管直立起来,让药品落入试管底部).
液体药品:操作要领是:“取下瓶塞______着放,标签______缓慢倒,用完盖紧原处放.”
(3)用量筒量取液体的方法:①读数时,应将量筒放______,并使视线与______处保持水平,②应根据量取液体体积的多少,选用大小适当的量筒.
(4)少量取液--滴管
给物质的加热.
(1)酒精灯的使用方法:①禁止向______的酒精灯里添加乙醇;②要用火柴点燃,禁止用______点燃另一只酒精灯;③用______加热;④熄灭时,用______灭,不能用嘴吹;⑤万一不慎碰倒酒精灯,应______.
玻璃仪器的洗涤
判别仪器干净方法:仪器上附着的水______.
参考答案:药品的取用
(1)①有些药品具有腐蚀性,有些药品有毒,所以“不能拿、不能闻、不能尝”.
故答案为:不能用手拿药品;不能把鼻孔凑近容器口去闻药品的气味;不得品尝任何药品的味道;
②严格按实验规定用量取用药品.如果没有说明用量,一般取最少量,液体lmL~2mL,固体只要盖满试管的底部.
故答案为:严格按实验规定用量取用药品.如果没有说明用量,一般取最少量,液体lmL~2mL,固体只要盖满试管的底部;
③取用的药品可能和某些物质反应而变质,有些有毒,所以实验时剩余的药品不能放回原瓶;不要随意丢弃;更不要拿出实验室.
故答案为:实验时剩余的药品不能放回原瓶;不要随意丢弃;更不要拿出实验室;
(2)药品取用方法
①块状固体为取用方便,在使用时一般用镊子夹取,故答案为:镊子;
②粉末状固体一般采用药匙或纸槽取用,瓶塞倒放是为了防止污染瓶塞,而污染药品;标签向着手心是防止瓶口残留的药品流下腐蚀标签.
故答案为:药匙,纸槽;倒;对着手心;
(3)因表面张力的存在,一般液体的液面是凹形的,量取液体在读数时视线要与凹液面最低处相平,否则会造成量取的液体体积偏大或偏小.
故答案为:平稳,液体的凹液面的最低处;
给物质加热.
(1)①如果向燃着的酒精灯内加酒精,酒精是易燃物,容易引起安全事故;
②用已燃的酒精灯点燃另一只酒精灯,容易倒出酒精而引起安全事故;
③酒精灯外焰温度最高,所以用外焰加热;
④灯帽盖灭使火焰与空气隔绝,使火焰缺少了燃烧需要的氧气;如果用嘴吹灭火将沿着灯芯进入酒精灯内引起火灾或爆炸.
⑤万一不慎碰倒酒精灯,应隔绝空气,所以应立刻用湿抹布扑盖.
故答案为:①燃着;②酒精灯;③外焰;④灯帽;⑤立刻用湿抹布扑盖;
玻璃仪器的洗涤
当洗过的玻璃仪器内的水既不聚成水滴,也不成股流下时,表示仪器已洗干净.
故答案为:既不聚成水滴,也不成股流下.
本题解析:
本题难度:一般
2、选择题 以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是 (? )
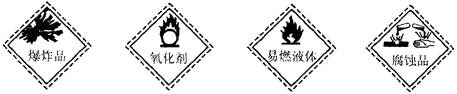
A 爆炸品?B 氧化剂?C 易燃液体? D 腐蚀品
参考答案:C
本题解析:乙醇属于可燃性液体,所以答案选C。
点评:该题是高考中的常见考点之一,属于常识性知识的考查,难度不大。该题的关键是掌握乙醇的性质,然后结合题干信息灵活判断即可,有利于培养学生的安全意识。
本题难度:简单
3、选择题 下列实验操作中,所使用的有关仪器要求干燥的是( )
A.配制一定物质的量浓度溶液时所用的容量瓶
B.氯化铵加热时所用的试管
C.做喷泉实验时用来收集氨气的烧瓶
D.用氯化钠跟浓硫酸反应制氯化氢时所用的反应容器烧瓶
参考答案:C
本题解析:窗体底端
窗体顶端
容量瓶中的少量水不影响溶液的浓度。氨水易挥发,因此制NH3时有少量水不影响NH3的生成。做喷泉实验时烧瓶未干燥(收集NH3时),挤入水后不易产生压强差。
本题难度:简单
4、选择题 下列实验操作与预期实验目的或所得实验结论一致的是
[? ]
?
实验操作
实验目的或结论
A.
某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体
?说明该钾盐是K2CO3
B.
向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤
?除去MgCl2溶液中少量FeCl3
C.
常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生
说明常温下Ksp( BaCO3)< Ksp( BaSO4)
D.
?C2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液
检验制得气体是否为乙烯
参考答案:B
本题解析:
本题难度:一般
5、实验题 以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
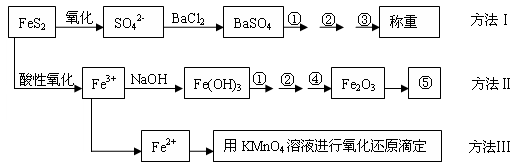
请回答下列问题:
(1)流程图中操作①、②、③分别指的是①_________、②__________、③________。
操作④、⑤用到的主要仪器是:④__________、⑤__________(每空填1-2个仪器)。
(2)判断溶液中SO42-离子已沉淀完全的方法是_________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,准确称取一定量的矿石试样,试样经溶解、预处理后,
A.用带有刻度的烧杯配制成100 mL试样溶液。
B.用量筒量取25.00 mL待测溶液,
C.并置于锥形瓶中。
D.用蒸馏水洗涤滴定管后装入KMnO4标准溶液,用该标准溶液滴定待测试样,(E)当溶液变成淡紫红色时,停止滴定,如30秒内不褪色,(F)读取并计算滴定管中消耗的KMnO4标准溶液体积,计算试样中的Fe元素含量。请指出该实验过程中错误操作步骤的编号________________________。
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是_____________________________________________。
(5)称取矿石试样1.60 g, 按方法Ⅰ分析,称得BaSO4的质量为4.66 g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是___________。
参考答案:
(1)过滤 (1分) 洗涤 (1分)?干燥 (1分) 坩埚、酒精灯 (1分)?天平 (1分)
(2)取上层清液滴加BaCl2溶液,若无白色沉淀生成,说明SO42-沉淀完全 (2分)
(3)A、B、D (3分)
(4)(2分)有三个可能的原因:(写出其中一种,即给2分)
① Fe(OH)3沉淀表面积大,易吸附杂质
②过滤洗涤时未充分将吸附的杂质洗去
③ Fe(OH)3灼烧不充分,未完全转化为Fe2O3
(5)75.0% (3分)
本题解析:(1)从溶液中得到纯净的固体需经过过滤、洗涤、干燥三步,第④步为灼烧使氢氧化铁分解为氧化铁,然后称量氧化铁的质量确定FeS2含量,所以使用的仪器分别为坩埚、酒精灯和天平;(2)取上层清液滴加BaCl2溶液,若无白色沉淀生成,说明SO42-沉淀完全;(3)A、配制溶液要用容量瓶,错误;B、量筒的读数只能精确到十分位,错误;D、滴定管要用待装液润洗,错误。(4)称量的固体质量高,导致结果偏高,故可能的原因有:① Fe(OH)3沉淀表面积大,易吸附杂质 ②过滤洗涤时未充分将吸附的杂质洗去 ③ Fe(OH)3灼烧不充分,未完全转化为Fe2O3;
(5)n(FeS2)=n(SO42-)/2=2n(BaSO4)/2=4.66÷233÷2=0.01mol
该矿石中FeS2的质量分数是0.01×120÷1.60=0.75
本题难度:一般