| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ�Ӱ�컯ѧ��Ӧ���ʵ����ء���Ƶ����Ԥ�⣨2019�����°棩(��)
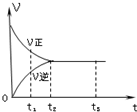 �ο��𰸣�A���ڿ��淴Ӧ�У����۸÷�Ӧ�Ƿ�ﵽƽ��״̬�����淴Ӧͬʱ���У���A���� ��������� �����Ѷȣ�һ�� 2��ʵ���� ��16�֣������£�ȡ��Ƭ������ȡ����κ������ͬ���澭��ɰֽ��ĥ����ȫ���������������Ƭ���ֱ���뵽ʢ�������ͬ��c(H+)��ͬ��ϡ�����ϡ������Һ����֧�Թܣ���ͬ���������ȡH2��ʵ���������±���
��2�������ϱ����ݣ���ó��Ľ����ǣ�?�� ��3������Ϊ������������Ŀ���ԭ���ǣ�д��һ�����ɣ��� __________________________________?___________________?_�� ��4�������ʵ�����ļ��������֤�� _______________________________________________?___________�� (5)����������趼������Ҫʹ����ϡ����������Ӧ�������������ʼӿ죬���Բ�ȡ�Ĵ�ʩ�У��о���������? �ο��𰸣�(1)2Al+6H+==2Al3++3H2����2�䣩 �����������1����������ϡ��������ᷴӦ�ų���������Ӧ�����ӷ���ʽ�� �����Ѷȣ�һ�� 3��ѡ���� ��ag ��״̼��Ƹ����������ᷴӦ����Ӧ����ʧ��������ʱ��ı仯������ͼ�е�ʵ����ʾ������ͬ�����£���b g ��a ��b ����ĩ״̼�����ͬŨ�ȵ����ᷴӦ������Ӧ��������ͼ�е�������ʾ��������ȷ���� A�p ? ? ? ? �ο��𰸣�C ��������� �����Ѷȣ�һ�� 4��ѡ���� ��ҵ��������ĵڶ�����Ӧ��2SO2(g)��O2(g) | |||||||||||||||||||
�ο��𰸣�B
������������ڸ÷�Ӧ�����������С�ҷ��ȵķ�Ӧ�����Ե��¶�����ʱ��ƽ�������ƶ���ƽ�ⳣ����С��ʹ�ô�����ƽ���ƶ�û��Ӱ�죬���Է�Ӧ��ת���ʲ��䣻ƽ�ⳣ��ֻ���¶ȵ�Ӱ�죬�����������������ʵ�����ƽ�ⳣ�����䣻ѹǿ����ƽ��������Ӧ�����ƶ�������������������ʵ���Ũ����������ͼ�Т٢ݢ�������������ȷ�ģ���ѡB��
���㣺��ѧƽ��ר��
�����Ѷȣ�һ��
5��ѡ���� ����CaCO3�����������ɶ�����̼�ķ�Ӧ������˵����ȷ����
[? ]
A. �÷�Ӧ�����ӷ���ʽΪCO32-+2H+=H2O+CO2��
B. �����Ũ�Ȳ�����������һ�������ɶ�����̼������һ������
C. ̼���������������ΪH+��CO32-��Ӧ���ƻ���CaCO3�ij����ܽ�ƽ��
D. CaCO3������������ǡ����ȫ��Ӧ���õ���Һ�д������й�ϵ��
2c(Ca2+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
�ο��𰸣�C
���������
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ���ܵ����.. | |
| �����Ŀ |