1、选择题 下列事实不能用勒夏特列原理解释的是
A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B.将FeCl3溶液加热蒸干最终得不到FeCl3固体
C.实验室用排饱和食盐水的方法收集氯气
D.经粉碎的黄铁矿在沸腾炉中燃烧得较快、较完全
参考答案:D
本题解析:
本题难度:简单
2、简答题 将1mol SO2和1mol O2通入体积不变的密闭容器,在一定温度和催化剂下达平衡,平衡时SO3为0.3mol,若此时再加1mol?SO2和1mol O2,则达新平衡时SO3的物质的量是( )
A.0.3mol
B.0.15mol
C.小于0.6mol
D.大于0.6mol
参考答案:再加1mol?SO2和1molO2,容器内压强增大,平衡向气体体积减小的方向移动,即向正反应方向移动;反应物转化率增大.
用极限法求出n(SO3)的范围,
假设反应物转化率与原平衡相同,此时n(SO3)=0.3mol×2=0.6mol,
假设2molSO2完全生成SO3,根据化学方程式2SO2+O2催化剂
本题解析:
本题难度:一般
3、简答题 向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:2X(g)?Y(g)+3Z(g)
(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为______mol/(L?min).
(2)若向达到(1)的平衡体系中充入氩气,则平衡向______(填“左“或“右“或“不移动“);
(3)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率与 (1)的平衡中的X的转化率相比较______.
A.无法确定B.一定大于 (1)
C.一定等于 (1)D.一定小于 (1)
(4)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为______.
参考答案:(1)容器内的压强与气体的物质的量成正比,容器内的压强为起始时的1.2倍,反应后的气体物质的量为:3mol×1.2mol=3.6mol,增加了0.6mol,
根据反应方程式,利用物质的量差计算:2X(g)?Y(g)+3Z(g) 物质的量变化△n
2 1 3 2
0.3mol 0.9mol 0.6mol
则用Y的物质的量浓度变化表示的速率为:0.3mol2L5min=0.03 mol/(L?min),
故答案为:0.03;
(2)体积为2L的固定密闭容器,由于充入氩气,容器内各组分的浓度没有发生变化,所以化学平衡不会移动,故答案为:不移动;
(3)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,反应体系内的压强增大,平衡向着逆向移动,X的转化率降低,
故选D;
(4)容器容积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,说明生成物Z浓度大于达到平衡时0.9mol;将3molX气体按照化学计量数全部转化为Z,c有最大值,最大值为4.5mol,所以c的范围为:.09<c≤4.5,
故答案为:0.9<c≤4.5.
本题解析:
本题难度:简单
4、选择题 对于反应2A(g)+xB(g)?4C(g)达到平衡时?C的浓度为1.2mol?L-1,当其它条件不变,把体积扩大1倍时,测得C的浓度为0.7mol?L-1,则x的值为( )
A.1
B.2
C.3
D.4
参考答案:A
本题解析:
本题难度:简单
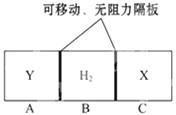
5、选择题 如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、C处分别充入等物质的量的X、Y两种气体.当隔板停止滑动时,下列说法正确的是( )
A.气体的体积:V(X)=V(Y)
B.物质的质量:m(X)<m(Y)
C.X的相对分子质量等于Y的相对分子质量
D.X的相对分子质量比Y的相对分子质量小