1、选择题 两种硫酸盐按一定比例混合后共熔,可制得化合物X且X溶于水能电离出K+、Cr3+、SO42-,若将2.83g?X中的Cr3+全部氧化为Cr2O72-后,溶液中的Cr2O72-可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O.若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀.由此可推断出X的化学式为( )
A.K2SO4?2Cr2(SO4)3
B.2K2SO4?Cr2(SO4)3
C.K2SO4?Cr2(SO4)3
D.K2SO4?
Cr2(SO4)3
参考答案:令2.83g?X中的Cr3+的物质的量为xmol,则:
? 2Cr3+~3I2
? 2mol?3×2×127g
? xmol? 3.81g
所以2mol:xmol=3×2×127g:3.81g,解得x=0.01,
4.66g硫酸钡的物质的量为4.66g233g/mol=0.02mol,
所以2.83gX的溶液中含有SO42-的物质的量为0.02mol,
根据电荷守恒可知2.83gX的溶液中含有K+的物质的量为0.02mol×2-0.01mol×31=0.01mol,
所以K2SO4为0.01mol×12=0.005mol,Cr2(SO4)3的物质的量为0.01mol×12=0.005mol,二者之比为1:1,
故X的化学式为K2SO4?Cr2(SO4)3,
故选C.
本题解析:
本题难度:简单
2、选择题 在相同条件下的三个反应:?2A-?+B2?==2B-?+A2;?2C-?+A2?==2A-?+C2;?2B-?+D2?==2D-?+B2,下列判断不正确的是
A.氧化性: B2> A2
B.还原性: C- > D-
C.2A- +D2 ==2D- + A2反应可以进行
D.2C- +B2 ==2B- + C2反应不能进行
参考答案:D
本题解析:在氧化还原反应中,氧化剂的氧化性强于氧化产物的,还原剂的还原性强于还原产物的,所以根据方程式可知,氧化性强弱顺序是D2、B2、A2、C2;还原性强弱顺序是C-、 A-、B-、D-,因此选项ABC都是正确的,D不正确,该反应是可以发生的,答案选D。
本题难度:困难
3、填空题 氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3-+4H++3e- = NO+2H2O
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:______________________________。
(2)反应中硝酸体现了_______性、_______性。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是_______mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:_____________________。
参考答案:(1)14HNO3+3Cu2O = 6Cu(NO3)2+2NO↑+7H2O
(2)酸;氧化
(3)0.6
(4)使用了较浓的硝酸,产物中有部分二氧化氮生成
本题解析:
本题难度:一般
4、选择题 下列物质的用途,利用了物质的氧化性的是
A.用漂白粉消毒游泳池中的水
B.用稀盐酸除去热水瓶胆壁上的水垢(主要成分是碳酸钙)
C.用食盐腌渍食物
D.用小苏打治疗胃酸过多
参考答案:A
本题解析:漂白粉消毒利用的是生成的HClO的强氧化性,盐酸除水垢利用的是盐酸的酸性,C项利用NaCl的防腐性,D项中利用小苏打的弱碱性.
本题难度:困难
5、填空题 近年来,江苏省酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下:
(?I?)将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液。
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。
(III)将盐酸加入NaHSO3溶液中得SO2气体回收,生成的NaCl循环利用。
①?写出步骤(I)反应的化学方程式:_________________?
②?写出步骤(III)反应的离子方程式:___________________
(2)还有学者提出利用?Fe?2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO42-而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成 SO42-的转化率。? ?
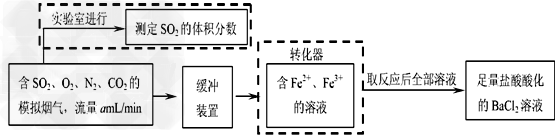
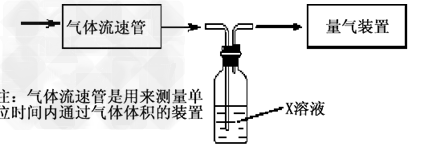
①?该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是(填序号)__________。(参考:还原性SO2?>?I-?>Br->Cl-)?
A.碘的淀粉溶液?B.酸性高锰酸钾溶液? ?C.氢氧化钠溶液?D.氯化钡溶液
②?若上述实验是在标准状况下进行的,X是已知体积和物质的量浓度的溶液,欲测定转化器中SO2氧化成SO42-的转化率,已知气体流速,还需测定的数据是_________________和加入盐酸酸化的氯化钡溶液后生成沉淀的质量。
(3)?为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及到的化学反应为:SO2+2CO=2CO2+?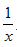 Sx 、 CO+?
Sx 、 CO+?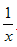 Sx=COS、2COS+SO2=2CO2+?
Sx=COS、2COS+SO2=2CO2+?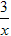 Sx 。其中COS中“C”化合价为____________。
Sx 。其中COS中“C”化合价为____________。
(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理:首先在消化细菌的作用下将NH4+氧化为NO3-:NH4++2O2=NO3-+2H++H2O,然后加入甲醇(CH3OH),NO3-和甲醇转化为两种无毒气体。请写出加入甲醇后反应的离子方程式________。
参考答案:(1)SO2+NaOH=NaHSO3?;?HSO3-+H+==SO2↑+H2O?
(2)AB?;?实验时间?
(3)+4?
(4)5CH3OH+6NO3-+6H+?==5CO2↑+3N2↑+13H2O
本题解析:
本题难度:一般