1������� ��15�֣�����������ʵ�����ɳ�����չ����Ҫ����ͼ���Ժ�H2S���ʵ���Ȼ��Ϊԭ����ȡ����������ͼ��

�ش��������⣺
��1����Ӧ�ڵĻ�ѧ����ʽΪ ��
��2����Ӧ�ܵ����ӷ���ʽΪ ��
��3�����������������ԭ�����£�
��CH4(g)��H2O(g) CO(g)��3H2(g) ��H����206.4 kJ��mol��1
CO(g)��3H2(g) ��H����206.4 kJ��mol��1
��CO(g)��H2O(g)  CO2(g)��H2(g) ��H����41.2 kJ��mol��1
CO2(g)��H2(g) ��H����41.2 kJ��mol��1
�ٶ��ڷ�Ӧ��һ���������ƽ����ϵ��H2�İٷֺ��������ܼӿ췴Ӧ���ʵĴ�ʩ�� ������ĸ���ţ���
a�������¶� b������ˮ����Ũ�� c��������� d������ѹǿ
�����÷�Ӧ��CO��һ��ת���������H2�IJ�������1.00 mol CO��H2�Ļ�����壨CO���������Ϊ20%����H2O��Ӧ���õ�1.18 mol CO��CO2��H2�Ļ�����壬��CO��ת����Ϊ ��
��������Ȼ����������������Ϊ5%���Ҽ�����ˮ������Ӧת���ɶ�����̼����������ת����Ϊ80%����ͨ����������1.00 m3��Ȼ�������Ͽ��Ƶ����� m3��ͬ��ͬѹ�����£���
��4��һ�������£���ͼ��ʾװ�ÿ�ʵ���л���ĵ绯ѧ���⣨���ɵ��л���Ϊ���壬���������л����
������Ŀ�����ĵ缫��ӦʽΪ ��
�ڸô���װ�õĵ���Ч��Ϊ�ǣ� �����ǣ�  ��100%������������С�����1λ��
��100%������������С�����1λ��

�ο��𰸣���1��2NH4HS��O2��2NH3��H2O��2S�� ��2�֣���2��SO2��I2��2H2O��4H+��SO42����2I�� ��2�֣�
��3���� a��2�֣� �� 90% ��2�֣� �� 3.09��2�֣�
��4���� C6H6��6H����6e����C6H12 ���л����д�ṹ��ʽ����2�֣� �� 51.7% ��3�֣�
�����������1���������������ԣ����������������ɵ���S�����������ͼ��֪��Ӧ�ڵĻ�ѧ����ʽΪ2NH4HS��O2��2NH3��H2O��2S����
��2����ˮ���������ԣ�������SO2�������ᣬ��Ӧ�ܵ����ӷ���ʽΪSO2��I2��2H2O��4H+��SO42����2I����
��3��������Ӧ�������������ȷ�Ӧ����a�������¶ȷ�Ӧ��������ƽ��������Ӧ������У�������������������ȷ��b������ˮ����Ũ�ȣ���Ӧ��������ƽ��������Ӧ�����ƶ���������������һ��������c����������ӿ췴Ӧ���ʵ�ƽ�ⲻ�ƶ��������������䣬����d������ѹǿ����Ӧ���ʽ��ͣ�����ѡa��
��1.00 mol CO��H2�Ļ�����壨CO���������Ϊ20%����CO�����������ʵ����ֱ���0.2mol��0.8mol������H2O��Ӧʱ����CO�����ʵ�����xmol������ݷ���ʽ��֪����CO2�����������ʵ����ֱ��Ƕ���xmol�����ں�õ�1.18 mol CO��CO2��H2�Ļ�����壬��0.2��x��x��0.8��x��1.18�����x��0.18������CO��ת����Ϊ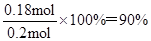 ��
��
��������Ȼ����������������Ϊ5%���Ҽ�����ˮ������Ӧת���ɶ�����̼����������ת����Ϊ80%����H2S�������0.05m3��������0.95m3��0.05m3H2S���տ��Եõ�����0.05m3�����ݷ�ӦI��֪���������������0.95m3��80%��3��2.28m3��CO�������0.95m3��80%��0.76m3����ͨ����Ӧ������������0.76m3������ͨ����������1.00 m3��Ȼ�������Ͽ��Ƶ�����0.05m3��2.28m3��0.76m3��3.09m3��
��4���ٸ��������֪��ʵ���Ŀ���ǵ绯ѧ���⣬���������Ϸ����ķ�ӦΪ����Ŀ�����������ϱ��õ��Ӻ����������ɻ����飬�缫��ӦʽΪC6H6��6H����6e����C6H12��
�ڵ��������������������ӷŵ���������������װ��ͼ��֪����������3.4mol����ת�Ƶ��ӵ����ʵ�����3.4mol��4��13.6mol������ˮ����ɿ�֪����1mol����ʱ����2mol������������3.4mol����ʱͬʱ����6.8mol��������μӷ�Ӧ�ı������ʵ�����xmol����μӷ�Ӧ�����������ʵ�����3xmol��ʣ�౽�����ʵ���Ϊ10mol��25%��xmol������Ӧ�ĺ�����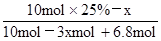 ��100%��10%�����x��
��100%��10%�����x�� �����Ա�ת��Ϊ������ת�Ƶ��ӵ����ʵ���Ϊ
�����Ա�ת��Ϊ������ת�Ƶ��ӵ����ʵ���Ϊ ��6����ô���װ�õĵ���Ч��Ϊ�ǣ�
��6����ô���װ�õĵ���Ч��Ϊ�ǣ� ��
��
���㣺���������Ʊ���������ͼ�ķ�����Ӧ��
�����Ѷȣ�����
2������� ��10�֣�һ����̼��һ����;�൱�㷺�Ļ�������ԭ�ϡ�
��1���������з�Ӧ���Խ�����ת��Ϊ���ȴ�99.9%�ĸߴ����� ����÷�Ӧ�ġ� H 0��ѡ�������������
����÷�Ӧ�ġ� H 0��ѡ�������������
��2���ڸ�����һ����̼�ɽ���������ԭΪ��������֪��
C(s)��O2(g)��CO2(g) �� H 1����393.5kJ��mol��1
CO2(g)��C(s) ��2CO(g) �� H 2����172.5kJ��mol��1
S(s)��O2(g) ��SO2(g) �� H 3����296.0kJ��mol��1
��д��CO��SO2���Ȼ�ѧ����ʽ ��
��3����ҵ����һ����̼��ȡ�����ķ�ӦΪ��CO(g)��H2O(g) CO2(g)��H2(g)����֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ9.0�������Ӧ��ʼʱ����2L���ܱ������г���CO ��H2O�����ʵ�������0.60mol��5minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ ��
CO2(g)��H2(g)����֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ9.0�������Ӧ��ʼʱ����2L���ܱ������г���CO ��H2O�����ʵ�������0.60mol��5minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ ��
��4����ͼ��һ������ȼ�ϵ��,����COΪȼ�ϣ�һ��������Li2CO3��Na2CO3���ڻ����Ϊ����ʣ�ͼ2�Ǵ�ͭ������װ��ͼ������ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�顣�ش��������⣺

��д��A�������ĵ缫��Ӧʽ ��
��Ҫ��ȼ�ϵ��Ϊ��Դ���д�ͭ�ľ���ʵ�飬��B��Ӧ���� �����C����D����������
�۵����ı�״����2.24LCOʱ��C�缫�������仯Ϊ ��
�ο��𰸣���1���� ��2��2CO(g)��SO2(g)��S(s)��2CO2(g) ��H����270kJ��mol��1 ��3��75%
(4)��CO��2e����CO32����2CO2 ��D ������6.4g
���������
�����������1����ӦNi��s��+4CO��g�� Ni��CO��4��g��Ϊ���Ϸ�Ӧ��������Ļ��Ϸ�ӦΪ���ȷ�Ӧ�����ȷ�Ӧ�ġ�H��0����2�����ݸ�˹���ɣ���Ӧ2CO+SO2=S+2CO2���ʱ�=��H1-��H2-��H3="-270" kJ?mol-1����3����5minĩ����COamol/L����CO(g)��H2O(g)
Ni��CO��4��g��Ϊ���Ϸ�Ӧ��������Ļ��Ϸ�ӦΪ���ȷ�Ӧ�����ȷ�Ӧ�ġ�H��0����2�����ݸ�˹���ɣ���Ӧ2CO+SO2=S+2CO2���ʱ�=��H1-��H2-��H3="-270" kJ?mol-1����3����5minĩ����COamol/L����CO(g)��H2O(g) CO2(g)��H2(g)��
CO2(g)��H2(g)��
��ʼ����mol/L���� 3 3 0 0
�仯����mol/L���� a a a a
5minĩ��mol/L���� 3-a 3-a a a
K=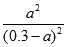 =9.0�����a=2.2.5mol/L����CO��ת����=
=9.0�����a=2.2.5mol/L����CO��ת����= ��100%=75%����4����CO���л�ԭ���ڸ����Ϸ���������Ӧ����CO2���缫��ӦʽΪ��CO-2e-+CO32-
��100%=75%����4����CO���л�ԭ���ڸ����Ϸ���������Ӧ����CO2���缫��ӦʽΪ��CO-2e-+CO32-
�����Ѷȣ�����
3��ѡ���� ���й��ڷ�Ӧ������˵����ȷ����
[? ]
A��Zn(s)+CuSO4(aq)==ZnSO4(aq)+Cu(s) ��H=216kJ/mol����E��Ӧ��>��E������
B��CaCO3(s)==CaO(s)+CO2(g) ��H=+178. 5kJ/mol����E��Ӧ��>��E������
C��HI(g) 1/2H2(g)+1/2I2(s) ��H=26.5kJ/mol���ɴ˿�֪1mol HI���ܱ������зֽ����Էų�26. 5kJ������
1/2H2(g)+1/2I2(s) ��H=26.5kJ/mol���ɴ˿�֪1mol HI���ܱ������зֽ����Էų�26. 5kJ������
D��H+(aq)+OH-(aq)==H2O(l) ��H= -57. 3kJ/mol����1mol NaOH��ˮ��Һ�뺬0.5mol H2SO4��Ũ�����Ϻ����57. 3kJ
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪����ʽ2H2(g)+O2(g)=2H2O(l) ��H1=-571��6KJ��mol-1������ڷ���ʽ 2H2O(l) =2H2(g)+O2(g)
��H2=����˵����ȷ����
[? ]
A������ʽ�л�ѧ��������ʾ������
B���÷�Ӧ��H2������
C���÷�Ӧ�ġ�H2=-571��6kJ��mol-1
D���÷�Ӧ�ɱ�ʾ36gˮ�ֽ�ʱ����ЧӦ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5��ѡ���� ���ж��Ȼ�ѧ����ʽ?H2��g��+I2��g���T2HI��g������H=+52kJ?mol-1�������У���ȷ���ǣ�������
A��1mol������1mol��������ȫ��Ӧ�ܷų�52kJ������
B��1������Ӻ�1���������ȫ��Ӧ��Ҫ����52kJ������
C��1molH2��g����1molI2��g����ȫ��Ӧ����2mol��HI����������52kJ������
D��
molH2��g����molI2��g����ȫ��Ӧ�ų�26kJ������
�ο��𰸣�C
���������
�����Ѷȣ�һ��