|
�߿���ѧ֪ʶ���������Ȼ�ѧ����ʽ������ǿ����ϰ��2019��Ѻ��棩(��)
2019-05-30 05:21:57
�� �� �� ��
|
1������� ��1����25���£���Ũ�Ⱦ�Ϊ0.1mol?L-1��MgCl2��CuCl2�����Һ����μ��백ˮ��������______�������ѧʽ�������ɸó��������ӷ���ʽΪ______������֪25��ʱKsp[Mg��OH��2]=1.8��10-11��KsP[Cu��OH��2]=2.2��10-20����
��2������ɴ�ʱ�£�N2H4����NO2��������Դ�����߷�Ӧ����������ˮ��������֪��
��N2��g��+2O2��g��=2NO2��g����H=+67.7kJ/mol
��N2H4��g��+O2��g��=N2��g��+2H2O��g����H=-534kJ/mol
���������������Ӧ���Ȼ�ѧ����ʽΪ��______
��3���ɴ�ʹ�õ�����ȼ�ϵ�ؾ��и��ܡ����Ͳ���Ⱦ�������ŵ㣮����ȼ�ϵ������ʽ�ͼ�ʽ���֣������ܷ�Ӧ��Ϊ��2H2+O2=2H2O����ʽ����ȼ�ϵ�صĵ������Һ��ǿ����Һ�������缫��Ӧʽ�ɱ�ʾΪ��2H2-4eһ=4H+������������ӦʽΪ______����ʽ����ȼ�ϵ���еĵ������Һ��ǿ����Һ���������缫��Ӧʽ�ɱ�ʾΪ��O2+2H2O+4e-=4OH-�����为����ӦʽΪ______��
�ο��𰸣���1��25��ʱ��Ksp[Mg��OH��2]=1.8��10-11��KsP[Cu��OH��2]=2.2��10-20��������ͭ���ܶȻ�����С��������þ���ܶȻ�������
������25���£���Ũ�Ⱦ�Ϊ0.1 mol?L-1��MgCl2��CuCl2�����Һ����μ��백ˮ��������������ͭ������
��Ӧ�Ļ�ѧ����ʽ�ǣ�CuCl2+2NH3?H2O=Cu��OH��2��+2NH4Cl��NH3?H2O��������ܲ�Cu��OH��2������ܲ�
�����ӷ���ʽΪ��Cu2++2NH3?H2O=Cu��OH��2��+2NH4+��
�ʴ�Ϊ��Cu��OH��2 �� Cu2++2NH3?H2O=Cu��OH��2��+2NH4+��
��2�����ݸ�˹���ɣ�����2���٣�+��2���ڣ���֪��
�������������Ӧ���Ȼ�ѧ����ʽΪ��2N2H4��g��+2NO2��g��=3N2��g��+4H2O��g����H=-1135.7kJ/mol
�ʴ�Ϊ��2N2H4��g��+2NO2��g��=3N2��g��+4H2O��g����H=-1135.7kJ/mol��
��3������ȼ�ϵ����������ʽ���Ǽ�ʽ�������ܷ�Ӧ��Ϊ��2H2+O2=2H2O ��
��ʽ����ȼ�ϵ�ظ����缫��ӦʽΪ��2H2-4e-=4H+��
�ã���-�ڣ�������ʽ����ȼ�ϵ�ص�������Ӧ��O2+4e-+4H+=2H2O��
��ʽ����ȼ�ϵ�ص������缫��ӦʽΪ��O2+2H2O+4e-=4OH-��
�ã���-�ۣ����ã�2H2-4e-+4OH-=4H2O���ʼ�ʽ����ȼ�ϵ�صĸ�����Ӧ��H2-2e-+2OH-=2H2O��
�ʴ�Ϊ��O2+4e-+4H+=2H2O��H2-2e-+2OH-=2H2O��
���������
�����Ѷȣ�һ��
2������� ��10�֣���ҵ���Ʊ�BaCl2�Ĺ�������ͼ��ͼ��

ij�о�С����ʵ�������ؾ�ʯ����Ҫ�ɷ�BaSO4���Թ�ҵ���̽���ģ��ʵ�顣����
�ϵã�
BaSO4(s) + 4C(s)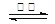 4CO(g) + BaS(s) ��H1 = +571��2 kJ��mol-1 �� 4CO(g) + BaS(s) ��H1 = +571��2 kJ��mol-1 ��
BaSO4(s) + 2C(s)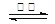 2CO2(g) + BaS(s) ��H2= +226��2 kJ��mol-1 �� 2CO2(g) + BaS(s) ��H2= +226��2 kJ��mol-1 ��
��1�����Ʊ�BaCl2�Ĺ�������ͼ������A�ù���NaOH��Һ���գ��õ����ơ�Na2Sˮ������ӷ���ʽΪ ��
�ڳ����£���ͬŨ�ȵ�Na2S��NaHS��Һ�У�����˵����ȷ���� ������ĸ����
A��Na2S��Һ��pH��NaHS��ҺpHС
B������Һ�к��е��������ͬ
C������Һ�е���ͬ���ͬŨ�ȵ����ᣬ���������������
D������Һ�м���NaOH���壬c(S2-)������
| E��NaHS��Һ�У�c(Na+) ��c(HS-) ��c(OH-) ��c (H+)
��2����BaCl2��Һ�м���AgNO3��KBr�������ֳ�������ʱ��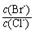 = �� ����֪��Ksp(AgBr)=5��4��10-13��Ksp(AgCl)=2��0��10-10�� = �� ����֪��Ksp(AgBr)=5��4��10-13��Ksp(AgCl)=2��0��10-10��
��3����ӦC(s) + CO2(g)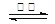 2CO(g)�Ħ�H = 2CO(g)�Ħ�H =
��4��ʵ�������б�����������̿��ͬʱ��Ҫͨ���������Ŀ���ǣ� ��ֻҪ���һ������
�ο��𰸣���1��S2����H2O HS����OH����D��E����2��2��7��10-3����3��+172��5KJ/mol����4��̿����ʹBaSO4��ֻ�ԭ HS����OH����D��E����2��2��7��10-3����3��+172��5KJ/mol����4��̿����ʹBaSO4��ֻ�ԭ
�����������1����BaSO4�뽹̿�ڸ����·�����Ӧ����BaS��BaS�����ᷢ����Ӧ��BaS+2HCl=BaCl2+H2S����H2S ���屻NaOH��Һ���յõ�Na2S��Na2S��ǿ�������Σ����������ˮ��ʹ��Һ�Լ��ԡ�ˮ������ӷ���ʽΪS2����H2O HS����OH������A��NaHS��H2S ��һ����������ģ�Na2S��H2S �Ķ�����������ģ����ڶ�Ԫ������˵��һ�����룾���������롣��Һ��������Ҫһ����������������ε�ˮ����ɣ�������ˮ�⣬˭��˭ˮ�⣬��Խ��Խˮ�⣬˭ǿ��˭�ԡ�������Һ�ļ���Na2S��NaHS����Na2S��Һ��pH��NaHS��ҺpH����B�����������ʵ���Һ�ж�����Na+��S2-��HS-��H2S��H+��OH-������������ͬ������C������Na2S��Һ�м�������ʱ�����ȷ���S2-+H+=HS-��û�����������Ȼ����HS-+H+=H2S�����ų����塣����NaHS��Һ�м�������ʱ��������HS-+H+=H2S�����ų����塣��������Һ�е���ͬ���ͬŨ�ȵ����ᣬ�����������ʲ���ȡ�����D������Na2S��NaHS����Һ�зֱ����NaOH��Һʱ����������OH-���ӵ�Ũ�ȣ�����ˮ��ƽ�⣺S2����H2O HS����OH������A��NaHS��H2S ��һ����������ģ�Na2S��H2S �Ķ�����������ģ����ڶ�Ԫ������˵��һ�����룾���������롣��Һ��������Ҫһ����������������ε�ˮ����ɣ�������ˮ�⣬˭��˭ˮ�⣬��Խ��Խˮ�⣬˭ǿ��˭�ԡ�������Һ�ļ���Na2S��NaHS����Na2S��Һ��pH��NaHS��ҺpH����B�����������ʵ���Һ�ж�����Na+��S2-��HS-��H2S��H+��OH-������������ͬ������C������Na2S��Һ�м�������ʱ�����ȷ���S2-+H+=HS-��û�����������Ȼ����HS-+H+=H2S�����ų����塣����NaHS��Һ�м�������ʱ��������HS-+H+=H2S�����ų����塣��������Һ�е���ͬ���ͬŨ�ȵ����ᣬ�����������ʲ���ȡ�����D������Na2S��NaHS����Һ�зֱ����NaOH��Һʱ����������OH-���ӵ�Ũ�ȣ�����ˮ��ƽ�⣺S2����H2O HS����OH����HS����H2O HS����OH����HS����H2O H2S��OH�������ƶ���ʹc(S2-)������������ȷ��E��NaHS=Na++ HS��; HS������ˮ�ⷴӦ HS����H2O H2S��OH�������ƶ���ʹc(S2-)������������ȷ��E��NaHS=Na++ HS��; HS������ˮ�ⷴӦ HS����H2O H2S��OH��Ҫ���ģ�����c(Na+) ��c(HS-)��HS��ˮ��������ˮ���������H+��ʹH+��Ũ�ȼ�С�����յ��ﵽˮ�ĵ���ƽ��ʱc(OH-) ��c (H+) ���εĵ���Զ�����������ˮ�ĵ��룬����c(HS-) ��c(OH-)�����E��NaHS��Һ�У�c(Na+) ��c(HS-) ��c(OH-) ��c (H+) ����ȷ����2����BaCl2��Һ�м���AgNO3��KBr��������Ӧ��Ag++Cl-="AgCl��;" Ag++Br-=AgBr����Ksp(AgBr)= C(Ag+)��C(Br-) =5��4��10-13; Ksp(AgCl)= C(Ag+)��C(Cl-)=2��0��10-10�����ֳ�������ʱ,C(Ag+)��ͬ�� H2S��OH��Ҫ���ģ�����c(Na+) ��c(HS-)��HS��ˮ��������ˮ���������H+��ʹH+��Ũ�ȼ�С�����յ��ﵽˮ�ĵ���ƽ��ʱc(OH-) ��c (H+) ���εĵ���Զ�����������ˮ�ĵ��룬����c(HS-) ��c(OH-)�����E��NaHS��Һ�У�c(Na+) ��c(HS-) ��c(OH-) ��c (H+) ����ȷ����2����BaCl2��Һ�м���AgNO3��KBr��������Ӧ��Ag++Cl-="AgCl��;" Ag++Br-=AgBr����Ksp(AgBr)= C(Ag+)��C(Br-) =5��4��10-13; Ksp(AgCl)= C(Ag+)��C(Cl-)=2��0��10-10�����ֳ�������ʱ,C(Ag+)��ͬ�� ��(3) ����-�ڣ���2�ɵã���ӦC(s) + CO2(g) ��(3) ����-�ڣ���2�ɵã���ӦC(s) + CO2(g) 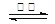 2CO(g)�Ħ�H =+172��5KJ/mol����4��ʵ�������б�����������̿��ͬʱ��Ҫͨ���������Ŀ����ʹBaSO4��ֻ�ԭ�õ�BaS�� 2CO(g)�Ħ�H =+172��5KJ/mol����4��ʵ�������б�����������̿��ͬʱ��Ҫͨ���������Ŀ����ʹBaSO4��ֻ�ԭ�õ�BaS��
���㣺����BaSO4����;��Na2S��NaHS��Һ�ıȽϡ��ܶȻ�������Ӧ�ü��Ȼ�ѧ����ʽ����д��֪ʶ��
�����Ѷȣ�һ��
3������� ��15�֣�X��Y��Z��W��ԭ���������������ǰ������Ԫ�أ�XԪ��ԭ�Ӻ����������ܼ������ܼ���������ȣ�Y�ĵ����ڿ�����ȼ������һ�ֵ���ɫ�Ĺ��壻ZԪ��ԭ�ӵ������������ȴθ����������2��W���ڲ�����ѳ����������ֻ��һ�����ӡ���ش�
��1��XԪ�������ڱ��е�λ���� ��W2�����ӵĺ�������Ų�ʽ
��2��Y���Ӻ�Z���ӱȽϣ��뾶�ϴ���� ��д���ӷ��ţ���ZԪ�غ���Ԫ�صļ���̬�⻯��е㲻ͬ��ԭ����
��3��ZԪ�صķǽ����Ա� ǿ������һ���ֽⷴӦ�Ʋ���ã��䷴Ӧ�Ļ�ѧ����ʽΪ
��4��X����������X��Z�γɵ���ԭ�ӻ������У��û���������е�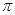 ���� ���� ���ĸ���֮���� ��YԪ������������Ӧˮ������С�մ�Ӧ�����ӷ���ʽΪ ���ĸ���֮���� ��YԪ������������Ӧˮ������С�մ�Ӧ�����ӷ���ʽΪ
��5����H2O2��ZԪ������������Ӧˮ����Ļ����Һ���ܽ�W���ʷ�ĩ����֪��
��W(s)+2H+(aq)=W2+(aq)+H2(g) ?H=-64.39KJ/mol
��2H2O2(l)=2H2O(l)+O2(g)?H=-196.46KJ/mol
��H2(g)+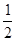 O2(g)= H2O(l) ?H=" -285.84" KJ/mol O2(g)= H2O(l) ?H=" -285.84" KJ/mol
����ZԪ������������Ӧˮ�������Һ�У�W��H2O2��Ӧ����W2����H2O���ȷ�Ӧ��ѧ����ʽΪ
�ο��𰸣���1���ڶ����ڵڢ�A�� [Ar]3d9
��2��S2�� HO���Ӽ����γ���������Ӽ��������ϴе�ϸ�
��3��ǿ H2SO4+Na2CO3=Na2SO4+CO2��+H2O
��4��1��1 HCO3��+OH��=CO32��+H2O
��5��Cu(s)+H2O2(l)+2H+(aq)=Cu2+ (aq)+2H2O(l) ��H=-319.68kJ/mol
���������XԪ��ԭ�Ӻ����������ܼ������ܼ���������ȣ���X ��CԪ�أ�Y�ĵ����ڿ�����ȼ������һ�ֵ���ɫ�Ĺ��壬��Y��NaԪ�أ�ZԪ��ԭ�ӵ������������ȴθ����������2����Z��SԪ�أ�W���ڲ�����ѳ����������ֻ��һ�����ӣ���Z��CuԪ�ء���1��XԪ�������ڱ��е�λ���ǵڶ����ڵڢ�A�壻29��Ԫ��Cu�����ӵĺ�������Ų�ʽ��[Ar]3d9����2��Y���Ӻ�Z���ӱȽϣ�ǰ����2��8�ĵ��Ӳ�ṹ��������2��8��8�ĵ��Ӳ�ṹ�����Ӻ�����Ӳ���Խ�࣬���Ӱ뾶Խ���������������а뾶�ϴ����S2-��H2O��H2S���Ƿ��Ӿ��壬���Ӽ�ͨ�����Ӽ���������ϣ���ˮ�ķ���֮����˷��Ӽ��������⣬����������������˷���֮���������������ˮ���۷е��H2S�ߡ���3��ZԪ�صķǽ����Ա�Xǿ������Ը���Ԫ�ص�����������Ӧ��ˮ���������ǿ���Ƚϣ��÷���ʽ��ʾ�ǣ�H2SO4+Na2CO3=Na2SO4+CO2��+H2O����4��X��Z�γɵ���ԭ�ӻ�����CS2�ǹ��ۻ�����ṹ����CO2���ṹʽ��S=C=S���û���������е�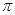 ���� ���� ���ĸ���֮����2:2=1:1��YԪ������������Ӧˮ������С�մ�Ӧ�����ӷ���ʽΪHCO3��+OH��=CO32��+H2O����5����+�ڡ�2+�ۣ������ɵã�Cu(s)+H2O2(l)+2H+(aq)=Cu2+ (aq)+2H2O(l) ��H=-319.68kJ/mol�� ���ĸ���֮����2:2=1:1��YԪ������������Ӧˮ������С�մ�Ӧ�����ӷ���ʽΪHCO3��+OH��=CO32��+H2O����5����+�ڡ�2+�ۣ������ɵã�Cu(s)+H2O2(l)+2H+(aq)=Cu2+ (aq)+2H2O(l) ��H=-319.68kJ/mol��
���㣺����Ԫ�ص��ƶϡ�Ԫ�������ڱ��е�λ�á���������Ų������Ӱ뾶�Ƚϡ������Ԫ�طǽ����ԵıȽϡ����ʷ����л�ѧ������Ӧ�����ӷ���ʽ���Ȼ�ѧ����ʽ��֪ʶ��
�����Ѷȣ�����
4������� ��1����25�桢101kPa�£�1gҺ̬�״�ȼ������CO2��Һ̬ˮʱ����22.7kJ����÷�Ӧ���Ȼ�ѧ����ʽӦΪ______��
��2����������������Ӧ����1molҺ̬ˮʱ����285.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ______����1gˮ����ת����Һ̬ˮ����2.444kJ����Ӧ2H2��g��+O2��g���T2H2O��g���ġ�H=______��
�ο��𰸣���1����1gCH3OHȼ�շ���22.7kJ����2molCH3OHȼ�շ���22.7��32��2=1452.8kJ�����ȼ�շ�Ӧ���Ȼ�ѧ����ʽΪ2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-1452.8kJ/mol��
�ʴ�Ϊ��2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l����H=-1452.8kJ/mol��
��2����������������Ӧ����1molҺ̬ˮʱ����285.8kJ�����H2��g��+12O2��g��=H2O��l����H=-285.8kJ/mol��
1gˮ����ת����Һ̬ˮ����2.444kJ�����H2O��g��=H2O��l����H=-43.992kJ/mol��
�ɸ�˹���ɿ�֪���١�2-�ڡ�2�õ���Ӧ2H2��g��+O2��g���T2H2O��g����
���H=��-285.8kJ/mol����2-��-43.992kJ/mol����2=-483.6kJ/mol��
�ʴ�Ϊ��H2��g��+12O2��g��=H2O��l����H=-285.8kJ/mol��-483.6kJ/mol��
���������
�����Ѷȣ�һ��
5������� CO�dz����Ļ�ѧ���ʣ��ڹ�ҵ��������;�ܹ㷺��
��1�� ��֪��ijЩ��Ӧ���Ȼ�ѧ����ʽ���£�
2H2��g��+SO2��g��=S��g��+2H2O��g�� ��H��+90.4kJ��mol��1
2CO��g��+O2��g��=2CO2��g�� ��H��-556.0kJ��mol��1
2H2��g��+O2��g��=2H2O��g�� ��H��-483.6kJ��mol��1
��д����CO��ȥ������SO2������S��g����CO2�Ȼ�ѧ����ʽ
��2�� ijȼ�ϵ����COΪȼ�ϣ��Կ���Ϊ��������������̬��K2CO3Ϊ����ʣ���д����ȼ�ϵ�������ĵ缫��Ӧʽ ��
��3����ij�¶��¡��ݻ���Ϊ2L�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��º��ݣ�ʹ֮������Ӧ��2H2��g����CO��g�� CH3OH��g������H����dJ��mol��1��d��0������ʼͶ����������ﵽƽ��ʱ���й��������£� CH3OH��g������H����dJ��mol��1��d��0������ʼͶ����������ﵽƽ��ʱ���й��������£�
ʵ��
| ��
| ��
| ��
| ��ʼͶ��
| 2 molH2��1 molCO
| 1 mol CH3OH
| 4 molH2��2 molCO
| ƽ��ʱn��CH3OH ��
| 0.5mol
| n2
| n3
| ��Ӧ�������仯
| �ų�Q1kJ
| ����Q2kJ
| �ų�Q3kJ
| ��ϵ��ѹǿ
| P1
| P2
| P3
| ��Ӧ���ת����
| ��1
| ��2
| ��3
|
�ٸ��¶��´˷�Ӧ��ƽ�ⳣ��KΪ ��
�����������еķ�Ӧ�ֱ��ƽ��ʱ�������ݹ�ϵ��ȷ���� ������ţ���
A����1����2��1 B��Q1��Q2��d
C����3����1 D��P3>2P1��2P2
E��n2��n3��1.0mol F��Q3��2Q1
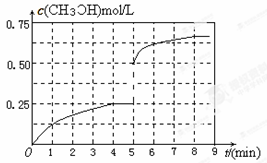
���������������������£�������������ϵ���ѹ����1L�����ڵ�8min�ﵽ�µ�ƽ�⣬�ӿ�ʼ����ƽ��ʱH2��ת����Ϊ65.5%��������ͼ�л�����5min ����ƽ��ʱCH3OH�����ʵ���Ũ�ȵı仯���ߡ�

��4��ʵ���ҳ��ü��ᣨһԪ�ᣩ���Ʊ�CO����֪25��ʱ��0.l mol/L����( HCOOH)��Һ��0.l mo1/L������Һ��pH�ֱ�Ϊ2.3��2.9��������ͬ���ʵ���Ũ�ȵ�����������Һ����HCOONa��Һ ��CH3COONa��Һ��Na2CO3��NaHCO3��Һ����pH�ɴ�С��˳���� ____����д��Һ��ţ�������0.l mo1/L HCOOH��Һ��0.l mo1/LHCOONa�������Ϻ����Һ������ȷ���� ____��
a��c(HCOO��)��c(HCOOH)��c��Na+����c��H+��
b��c(HCOO��)+c(HCOOH)=" 0.2" mo1/L
c��c(HCOO��)+2c(OH��)=c��HCOOH��+2c��H+��
d��c(HCOO��) ��c��Na+����c��H+����c(OH��)
�ο��𰸣���1��2CO(g)+SO2(g)=S(g)+2CO2(g) ��H=+18.0kJ/mol
��2��������O2+4e-+2CO2=2CO32-
��3����4����AB������ͼ��
��4���ۣ��ܣ��ڣ��٣�cd
�����������1�����ø�˹���ɣ���������ӦI+��ӦII-��ӦIII�ɵ�2CO(g)+SO2(g)=S(g)+2CO2(g) ��H=+18.0kJ/mol��
��2����COΪȼ�ϣ��Կ���Ϊ��������������̬��K2CO3Ϊ����ʣ���ȼ�ϵ�ص�������ӦΪO2+4e-+2CO2=2CO32-��
��3���ٸ��ݱ�������(����ʵ��)����������ʽ�ɵ�:
2H2��g����CO��g�� CH3OH��g�� CH3OH��g��
��ʼŨ�ȣ�mol/L����1 0.5 0
�仯Ũ�ȣ�mol/L����0.5 0.25 0.25
ƽ��Ũ�ȣ�mol/L����0.5 0.25 0.25
����ƽ�ⳣ��K=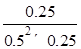 =4�� =4��
�ں��º��������£�ʵ���ʵ����Ϊ��Чƽ�⣬��Ϊ������Ӧ������У���Ϊ���淴Ӧ������У�����������·�Ӧ���ת���ʦ�1����2��1����Ӧ�ų������յ�������ֵ֮��Q1��Q2��d��ʵ�����Ӧ���Ǽ�2�����൱������ѹǿ����ƽ��������Ӧ�����ƶ���ʹ��Ӧ��ת��������3����1��ƽ��ʱn3��1.0mol��P3��2P1��Q3��2Q1����ѡAB��
���������������������£�������������ϵ���ѹ����1L��ѹ����˲�䣬�״���Ũ��Ϊԭ����2����Ȼ��ƽ��������Ӧ�����ƶ���ʹ�״�Ũ�Ƚ�һ������ֱ��ƽ�⣬�ݴ˿�����CH3OH�����ʵ���Ũ�ȵı仯����ͼ��
��4�����������Ϣ��֪��������Ա�����ǿ����HCOONa��Һ��CH3COONa��Һˮ��̶�С������������Һ��pH�ɴ�С��˳��Ϊ�ۣ��ܣ��ڣ��٣�����0.l mo1/L HCOOH��Һ��0.l mo1/LHCOONa�������Ϻ����Һ�����������غ�c(HCOO��)+c(HCOOH)=" 0.1" mo1/L������غ�Ϊc(HCOO��)+ c(OH��)=c��Na+��+c��H+��������Һ�����ԣ�����c��H+����c(OH��)����c(HCOO��) ��c��Na+����c��H+����c(OH��)���������غ�͵���غ��������ɵ�c(HCOO��)+2c(OH��)=c��HCOOH��+2c��H+�������ϣ�cd��ȷ��
���㣺�����˹���ɡ�ȼ�ϵ�ص缫��Ӧʽ��д����ѧƽ�⡢����ˮ������֪ʶ��
�����Ѷȣ�����
| 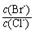 = �� ����֪��Ksp(AgBr)=5��4��10-13��Ksp(AgCl)=2��0��10-10��
= �� ����֪��Ksp(AgBr)=5��4��10-13��Ksp(AgCl)=2��0��10-10��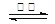 2CO(g)�Ħ�H =
2CO(g)�Ħ�H = 