1ЎўСЎФсМв ФЪЛбРФИЬТәЦРДЬҙуБҝ№ІҙжЈ¬ІўЗТИЬТәОӘОЮЙ«НёГчөДАлЧУЧйКЗ
AЈ®Na+ЎўK+ЎўSiO32ЈӯЎўSO42Јӯ
BЈ®NH4+ЎўNa+ЎўNO3ЈӯЎўClЈӯ
CЈ®K+ЎўCa2+ЎўHCO3ЈӯЎўClЈӯ
DЈ®Mg2+ЎўK+ЎўClЈӯЎўMnO4ЁD
ІОҝјҙр°ёЈәB
ұҫМвҪвОцЈәВФ
ұҫМвДС¶ИЈәТ»°г
2ЎўМоҝХМв ЈЁ10·ЦЈ©ЛжЧЕ№ӨТөөДСёЛЩ·ўХ№Ј¬ІъЙъөД·ПЛ®¶ФЛ®МеөДОЫИҫТІИХЗчСПЦШЎЈНЁ№эҝШЦЖИЬТәөДpH¶Ф№ӨТө·ПЛ®ЦРөДҪрКфАлЧУҪшРР·ЦАлКЗКөјК№ӨЧчЦРҫӯіЈК№УГөД·Ҫ·ЁЎЈПВұнКЗіЈОВПВҪрКфЗвСх»ҜОпөДKsp(іБөнИЬҪвЖҪәвіЈКэ)әНҪрКфАлЧУФЪДіЕЁ¶ИПВҝӘКјіБөнЛщРиөДpH(ұнЦРЕЁ¶ИОӘПаУҰpHКұИЬТәЦРУР№ШҪрКфАлЧУІъЙъіБөнөДЧоРЎЕЁ¶ИЈ»өұИЬТәЦРҪрКфАлЧУЕЁ¶ИРЎУЪ10-5 mol?L-1КұНЁіЈИПОӘёГАлЧУіБөнНкИ«)ЎЈ
ҪрКфАлЧУ
| Ksp
| pH(10-1 mol?L-1)?
| ?pH(10-5 mol?L-1)
|
?Fe3+
| ?4.0ЎБ10-38
| ?2.7
| ?3.7
|
Cr3+ ?
| 6.0ЎБ10-31
| 4.3
| 5.6
|
Cu2+
| 2.2ЎБ10-20
| ?4.7
| 6.7
|
Ca2+
| ?4.0ЎБ10-5
| ?12.3?
| ?14.3
|
(1)Діі§ЕЕіцөД·ПЛ®ЦРә¬УРCu2+әНFe3+Ј¬ІвөГЖдЕЁ¶ИҫщРЎУЪ0.1 mol?L-1ЎЈОӘіэИҘЖдЦРөДFe3+Ј¬»ШКХНӯЈ¬РиҝШЦЖөДpH·¶О§КЗ_______________________________ЎЈ
(2)ОӘБЛҙҰАнә¬УРCr2O72-ЛбРФИЬТәөД№ӨТө·ПЛ®Ј¬ІЙУГИзПВ·Ҫ·ЁЈәПт·ПЛ®ЦРјУИЛККБҝNaClЈ¬ТФFeОӘөзј«ҪшРРөзҪвЈ¬ҫӯ№эТ»¶ОКұјдЈ¬УРCr(OH)3әНFe(OH)3іБөнЙъіЙЕЕіцЈ¬ҙУ¶шК№·ПЛ®ЦРёхә¬БҝөНУЪЕЕ·ЕұкЧјЎЈ
ўЩCr2O72-ЧӘұдОӘCr3+өДАлЧУ·ҪіМКҪОӘ______________________ЎЈ
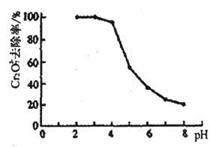
ўЪpH¶Ф·ПЛ®ЦРCr2O72-ИҘіэВКөДУ°ПмИзНјЎЈДгИПОӘөзҪв№эіМЦРИЬТәөДpHИЎЦөФЪ______·¶О§ДЪ¶ФҪөөН·ПЛ®ЦРөДёхә¬БҝЧоУРАыЈ¬ЗлЛөГчАнУЙЈә_________________________________ЎЈ
[ЧўЈәИҘіэВК(ЈҘ)=[(c0-c)ЈҜco]ЎБ100ЈҘЈ¬КҪЦРЈәcoЎӘҙҰАнЗ°·ПЛ®ЦРCr2O72-ЕЁ¶ИЈ¬cЎӘҙҰАнәу·ПЛ®ЦРCr2O72-өДЕЁ¶И]
(3)іБөнЧӘ»ҜФЪЙъІъЦРТІУРЦШТӘУҰУГЎЈАэИзЈ¬УГNa2CO3ИЬТәҝЙТФҪ«№шВҜЛ®№ёЦРөДCaSO4ЧӘ»ҜОӘҪПКиЛЙ¶шТЧЗеіэөДCaCO3Ј¬ёГіБөнЧӘ»ҜҙпөҪЖҪәвКұЈ¬ЖдЖҪәвіЈКэKЈҪ_________(РҙКэЦө)ЎЈ[ТСЦӘKsp (CaSO4)=9.1x10-6Ј¬Ksp (CaCO3)=2.8ЎБ10-9]
ІОҝјҙр°ёЈәЈЁ1Ј©3.7ЎЬpHЈј4.7ЈЁ2·ЦЈ©
ЈЁ2Ј©ўЩCr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2OЈЁ2·ЦЈ©
ўЪ4.3Ў«5.6ЈЁ»т5Ў«6Ј©ЈЁ2·ЦЈ©? pHФҪРЎЈ¬Cr2O72-өДИҘіэВКФҪҙуЈ¬ө«ДСРОіЙCr(OH)3іБөнҙУ·ПЛ®ЦР·ЦАлЈ»pHФҪҙуЈ¬Cr2O72-өДИҘіэВКФҪРЎЈЁ2·ЦЈ©
ЈЁ3Ј©3.25ЎБ103ЈЁ2·ЦЈ©
ұҫМвҪвОцЈәЈЁ1Ј©УЙЛщёшКэҫЭҝЙҝҙіцЈ¬Fe3+ФЪpH=3.7КұТСНкИ«іБөнЈ¬¶шCu2+ФЪpH=4.7КұІЕҝӘКјіБөнЈ¬ЛщТФОӘіэИҘЖдЦРөДFe3+Ј¬»ШКХНӯЈ¬РиҝШЦЖөДpH·¶О§КЗ3.7ЎЬpHЈј4.7
ЈЁ2Ј©ўЩ·ПЛ®ТФFeОӘөзј«ҪшРРөзҪвЈ¬МъЧчСфј«МъөзЧУЙъіЙFe2+ЈәFe ЎӘ2eЎӘ=Fe2+Ј¬Fe2+»№ФӯCr2O72-ЈәCr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O
ўЪЧЫәПҝјВЗЛщёшРЕПўЈ¬ЛдИ»pHФҪРЎЈ¬Cr2O72-өДИҘіэВКФҪҙуЈ¬ө«ДСРОіЙCr(OH)3іБөнҙУ·ПЛ®ЦР·ЦАлЈЁCr3+ФЪpH=4.3КұІЕҝӘКјіБөнЈ¬ФЪpH=5.6КұНкИ«іБөнЈ©Ј¬pHМ«ёЯЈ¬Cr2O72-өДИҘіэВКМ«РЎЈ¬ОЮКөјКТвТеЈ¬ЧЫәП·ЦОцҝЙЦӘpHИЎЦөФЪ4.3Ў«5.6ЈЁ»т5Ў«6Ј©·¶О§ДЪ¶ФҪөөН·ПЛ®ЦРөДёхә¬БҝЧоУРАы
ЈЁ3Ј©УЙЧӘ»Ҝ·ҪіМКҪөГЈәKЈҪKsp (CaSO4)=9.1x10-6 / Ksp (CaCO3)= 3.25ЎБ103
ұҫМвДС¶ИЈәТ»°г
3ЎўСЎФсМв ФЪПВБРёчИЬТәЦРЈ¬АлЧУТ»¶ЁДЬҙуБҝ№ІҙжөДКЗ?ЈЁ?Ј©?
AЈ®ЗҝјоРФИЬТәЦРЈә 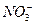 Ўў
Ўў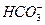 Ўў
Ўў Ўў
Ўў
BЈ®ә¬УР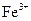 өДИЬТәЦРЈә
өДИЬТәЦРЈә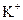 Ўў
Ўў ЎўH+ЎўAlO2-
ЎўH+ЎўAlO2-
CЈ®ДіОЮЙ«ИЬТәЦРЈә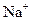 ЎўCu2+ЎўSO42-Ўў
ЎўCu2+ЎўSO42-Ўў
DЈ®КТОВПВЈ¬pH=1өДИЬТәЦРЈә Ўў
Ўў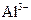 Ўў
Ўў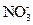 Ўў
Ўў
ІОҝјҙр°ёЈәD
ұҫМвҪвОцЈәВФ
ұҫМвДС¶ИЈәјтөҘ
4ЎўМоҝХМв ЈЁ10·ЦЈ©ДіҙэІвИЬТәЈЁСфАлЧУОӘNaЈ«Ј©ЦРҝЙДЬә¬УРSO42ЈӯЎўSO32ЈӯЎўNO3ЈӯЎўClЈӯЎўBrЈӯЎўCO32ЈӯЎўHCO3ЈӯЦРөДТ»ЦЦ»т¶аЦЦЈ¬ҪшРРИзНјЛщКҫөДКөСйЈ¬ГҝҙОКөСйЛщјУКФјБҫщ№эБҝЈ¬»ШҙрТФПВОКМвЈә
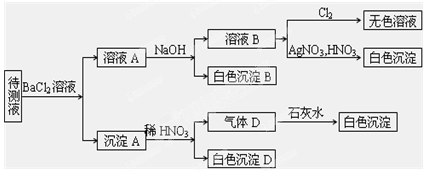
ЈЁ1Ј©ҙэІвТәЦРКЗ·сә¬УРSO42ЈӯЎўSO32ЈӯЈә_____________________ ЎЈ
ЈЁ2Ј©іБөнBөД»ҜС§КҪОӘ_________Ј»ЙъіЙіБөнBөДАлЧУ·ҪіМКҪОӘ
___________________ __ЎЈ
ЈЁ3Ј©ёщҫЭТФЙПКөСйЈ¬ҙэІвТәЦРҝП¶ЁГ»УРөДАлЧУКЗ___________________; ҝП¶ЁҙжФЪөДАлЧУ»№УР________________________ЎЈ
ІОҝјҙр°ёЈәўЕЦБЙЩә¬УРТ»ЦЦАлЧУ
ўЖBaCO3Ј¬2HCO3-+Ba2++2OH- = BaCO3Ўэ+2CO32-+2H2O
ўЗBrЈӯЎўS2ЈӯЈ»CO32-ЎўHCO3-
ұҫМвҪвОцЈәҙэІвТәәНВИ»Ҝұө·ҙУҰЙъіЙіБөнAЈ¬ЛөГчҙэІвТәЦРә¬УРSO42-ЎўSO32-ЎўCO32-ЦРөДТ»ЦЦЎўБҪЦЦ»тИэЦЦЈ¬ПтіБөнЦРјУПЎПхЛбәуЈ¬іБөнІҝ·ЦИЬҪвЙъіЙЖшМеЈ¬ЛөГчҙэІвТәЦРә¬УРCO32-Ј¬BaSO3ДЬұ»ПхЛбСх»ҜЙъіЙBaSO4Ј¬ЛщТФҙЛКөСйЦӨГчҙэІвТәЦРә¬УРSO42-ЎўSO32-ЦРөДТ»ЦЦ»тБҪЦЦЈ¬¶юСх»ҜМјәНЗвСх»ҜёЖ·ҙУҰЙъіЙBaCO3°ЧЙ«іБөнЈ»ИЬТәAЦРјУNaOHЙъіЙіБөнЈ¬NaOHәНHCO3-·ҙУҰЙъіЙCO32-Ј¬CO32-әНBa2+·ҙУҰЙъіЙBaCO3іБөнЈ¬ЛөГчҙэІвТәЦРә¬УРHCO3-Ј¬ИЬТәBЦРјУИлВИЖшөГОЮЙ«ИЬТәЛөГчГ»УРBrЈӯЎўS2ЈӯЈ»јУИлПхЛбәНПхЛбТшУРAgCl°ЧЙ«іБөнЈ¬ХвКЗУЙУЪЗ°ЖЪјУИлБЛВИ»ҜұөКЗЛщЦБЈ¬№КІ»ДЬИ·¶ЁКЗ·сУРCl-ЎЈ
ўЕНЁ№эТФЙП·ЦОцЦӘЈ¬ҙэІвТәЦРә¬УРSO42-ЎўSO32-ЦРөДТ»ЦЦ»тБҪЦЦЈ¬ТтОӘҙэІвТәјУИлBaCl2ИЬТәәНПЎHNO3ЙъіЙБЛBaSO4іБөнЈ¬BaSO4өДЙъіЙҝЙДЬАҙЧФSO42-»тSO32-ЦРөДТ»ЦЦ»тБҪЦЦЈ»
ўЖНЁ№эТФЙП·ЦОцЦӘЈ¬іБөнBКЗBaCO3Ј»ЙъіЙіБөнBөДАлЧУ·ҪіМКҪОӘ2HCO3-+Ba2++2OH- = BaCO3Ўэ+2CO32-+2H2OЈЁNaOH№эБҝЈ©Ј»
ўЗҙэІвТәЦРҝП¶ЁГ»УРөДАлЧУКЗBrЈӯЎўS2ЈӯЈ»ҝП¶ЁҙжФЪөДАлЧУ»№УРCO32-ЎўHCO3-ЎЈ
ҝјөгЈәҝјІйАлЧУ·ҙУҰЎЈ
ұҫМвДС¶ИЈәТ»°г
5ЎўСЎФсМв ДіИЬТәЦРҙжФЪҪП¶аөДOHЎӘЎўK+ЎўCO32ЎӘЈ¬ёГИЬТәЦР»№ҝЙДЬҙуБҝҙжФЪөДКЗ
AЈ®H+
BЈ®Ca2+
CЈ®NH4+
DЈ®SO42ЎӘ