1、填空题 (10分)如表所示为元素周期表的一部分,参照元素①~⑦在表中的位置,请回答下列问题:
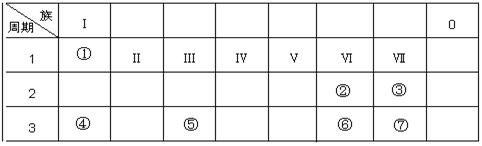
(1)③、④、⑦的原子半径由大到小的顺序为(用元素符号表示,下同) ;
(2)⑥和⑦的最高价含氧酸的酸性强弱为(用酸的化学式表示) ;
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 ;
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。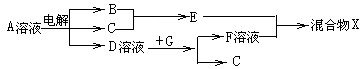
①写出D溶液与G反应的化学方程式: ;
②写出检验A溶液中溶质的阴离子的方法: ;
③常温下,若电解1L0.1mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为: ;
④若上图中各步反应均为恰好完全转化,则混合物X中含有的物质有: 。
参考答案:(1)(2分)Na>Cl>F (2)(2分)HClO4>H2SO4
(3)(2分)H2O2+2Fe2++2H+=2Fe3++2H2O (4)(4分,每小题1分)
① 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
② 取少量A溶液滴加几滴稀硝酸酸化的硝酸银溶液有白色沉淀生成
③ 0.01 mol. ④ NaCl、Al(OH)3和H2O(水不写不扣分)
本题解析:根据元素在周期表中的位置,可知①为H、②为O、③为F、④为Na、⑤为Al、⑥为S、⑦为Cl,则
(1)同周期自左而右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,故原子半径:Na>Cl>F,故答案为:Na>Cl>F;
(2)非金属性Cl>S,非金属性越强,最高价含氧酸的酸性越强,故酸性:HClO4>H2SO4,故答案为:HClO4>H2SO4;
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物为H2O2,在酸性溶液中能将Fe2+氧化Fe3+,同时生成水,反应离子方程式为:H2O2+2Fe2++2H+=2Fe3++2H2O,故答案为:H2O2+2Fe2++2H+=2Fe3++2H2O;
(4)由表中元素形成的物质,其中B、C、G是单质,B为黄绿色气体,则B为Cl2,D溶液显碱性,电解A溶液为电解氯化钠溶液生成氢气、氯气与氢氧化钠,故D为NaOH、C为H2,则E为HCl,G能与氢氧化钠溶液反应得到氢气与F,故G为Al,F为NaAlO2,则:
①D溶液与G反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
②检验NaCl溶液中溶质的阴离子的方法:取少量A溶液滴加几滴(稀硝酸酸化)硝酸银溶液有白色沉淀生成,故答案为:取少量A溶液滴加几滴(稀硝酸酸化)硝酸银溶液有白色沉淀生成;
③常温下,若电解1L 0.1mol/L的NaCl溶液,一段时间后测得溶液中的c(OH -)=10-2mol/L,则n(NaOH)=0.01mol/L×1L=0.01mol,由2NaCl+2H2O 2NaOH+H2↑+Cl2↑,可知成氯气为0.01mol×1/2=0.005mol,故转移电子物质的量=0.005mol×2=0.01mol,故答案为:0.01mol;
2NaOH+H2↑+Cl2↑,可知成氯气为0.01mol×1/2=0.005mol,故转移电子物质的量=0.005mol×2=0.01mol,故答案为:0.01mol;
④如图所示各步反应均为恰好完全转化,电解反应为2NaCl+2H2O 2NaOH+H2↑+Cl2↑,而2Al~2NaOH~2NaAlO2,得到偏铝酸钠与HCl物质的量之比为1:1,由H2O+HCl+NaAlO2
2NaOH+H2↑+Cl2↑,而2Al~2NaOH~2NaAlO2,得到偏铝酸钠与HCl物质的量之比为1:1,由H2O+HCl+NaAlO2
本题难度:困难
2、选择题 用惰性电极电解2L饱和氯化钠溶液,经过一段时间以后,电解液的pH上升至13
(Kw=10-14),则电解过程中两极上共产生的气体在标准状况下体积为
A.2.24L
B.4.48L
C.1.12L
D.11.2L
参考答案:B
本题解析:溶液中pH=13,说明溶液中OH-的浓度是0.1mol/L,所以氢氧化钠的物质的量是0.2mol。则根据2NaCl+2H2O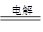 2NaOH+Cl2↑+H2↑可知,氢气和氯气的物质的量都是0.1mol,所以答案选B。
2NaOH+Cl2↑+H2↑可知,氢气和氯气的物质的量都是0.1mol,所以答案选B。
本题难度:一般
3、填空题 (14分)电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为?,在X极附近观察到的现象是:?;Y电极上的电极反应式是?。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是?,电极反应式是?,Y电极的材料是?,电极反应式是?。
参考答案:(1)2H++2e-=H2↑?有气泡,溶液变红;2Cl-―2e-=Cl2↑ (2)纯铜? Cu2++2e-=Cu?粗铜? Cu-2e-=Cu2+
本题解析:(1)X与电源的负极相连,作阴极,溶液中的氢离子放电,反应式2H++2e-=H2↑。由于氢离子放电,破坏了阴极周围水的电离平衡,导致溶液中OH-的浓度大于氢离子的,所以溶液显碱性。Y和电源的正极相连,作阳极,溶液中的氯离子放电,反应式为2Cl-―2e-=Cl2↑。
(2)粗铜精炼时,粗铜和电源的正极相连,作阳极。纯铜和电源的负极相连,作阴极。
本题难度:一般
4、选择题 用惰性电极电解Fe2(SO4)3和CuSO4的混合溶液,下列说法正确的是
[? ]
A.阴极反应式为:Cu2++2e-==Cu,当有Cu2+存在时,Fe3+不放电
B.阴极上首先析出铁,然后析出铜
C.阴极先是Fe3+放电,后Cu2+放电
D.阴极上不可能析出铜
参考答案:C
本题解析:
本题难度:一般
5、填空题 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病,KI、KIO3曾先后用于加碘盐中。
(1)工业上可以通过铁屑法生产KI,其工艺流程如下:
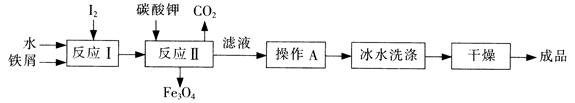
①反应I生成铁与碘的化合物,若该化合物中铁元素与碘元素的质量比为21:127,则加入足量碳酸钾时,反应Ⅱ的化学方程式为 。
②操作A包括 ;用冰水洗涤的目的是 。
(2)KIO3可以通过H2O2氧化I2先制得HIO3,然后再用KOH中和的方法进行生产。
①烹饪时,含KIO3的食盐常在出锅前加入,其原因是 。
②若制得1284 kg KIO3固体,理论上至少需消耗质量分数为30%的双氧水 kg。
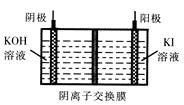
③KIO3还可通过下图所示原理进行制备。电解时总反应的离子方程式为 。若忽略溶液体积的变化,则电解结束后阴极区的pH与电解前相比 (选填“增大”、“减小”或“不变”)。
参考答案:(1)① Fe3I8 + 4K2CO3 = Fe3O4 + 8KI + 4CO2↑ (2分)
②加热浓缩、冷却结晶、过滤 (2分)
洗涤除去表面可溶性杂质,同时减少KI的溶解损失 (2分)
(2)①在较高温度下KIO3易分解(2分) ②1700 (2分)
③I一+ 3H2O通电IO3- + 3H2↑ (2分) 不变(2分)
本题解析:(1)①反应I生成铁与碘的化合物,铁元素与碘元素的质量比为21:127,即物质的量比是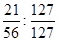 =3:8,故反应方程式是Fe3I8 + 4K2CO3 = Fe3O4 + 8KI + 4CO2↑。
=3:8,故反应方程式是Fe3I8 + 4K2CO3 = Fe3O4 + 8KI + 4CO2↑。
②用冰水洗涤的目的是洗涤除去表面可溶性杂质,同时减少KI的溶解损失;
(2)①烹饪时,含KIO3的食盐常在出锅前加入,其原因是在较高温度下KIO3易分解;
②因为H2O2氧化I2先制得HIO3:5H2O2+I2==2HIO3+4H2O,即5H2O2~2IO3-,1284 kg KIO3固体为6k mol,故m(H2O2)= 5/2×6kmol×34g・mol-1/30%=1700kg。
③虽然阴极区有大量氢氧根离子生成,但阳极区反应消耗氢氧根离子,氢氧根离子通过阴离子交换膜到阳极区反应,总反应中没有酸或碱生成以及消耗。故而阴极区反应前后pH没有变化。当然,如果题目没有“忽略溶液体积变化“的说明,情况就不同了,随着电解的进行,总反应耗水,阴极区pH会增大。
考点:官能团为酯键的芳香化合物的性质。
本题难度:一般