1������� ��һ����1����ͼΪ���������IJ��ֽṹ���е��������Ŵ�
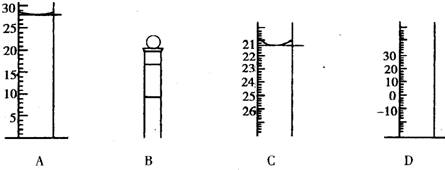
Aͼ��Һ����ʾ��Һ�����Ϊ______mL�����������������е�ij�ֲ���һҺ��������ƽ��ʱ����ΪN?mL������ʱ����ΪM?mL����M��N������ʹ�õ�������______������ĸ��ţ���
��2�����ξ��ᴿ��õ�NaCl��Һ���پ��������ᾧ����ɵþ��Σ�
������������ʹ�õ��Ĵ�������������Ϊ______��
�ڸ�ͬѧ�����þ��������Һ��������һʵ�飮ʵ������Ҫ��80mL?l?mol/L��NaCl��Һ�����ƹ�������������ƽ��ȡ�ľ�������Ϊ______g�����ڶ��ݵIJ��������Ĺ�������Ϊ______��
����������δ����ǩ���Լ�ƿ�зֱ�װ������ϡ��Һ��FeSO4����H2SO4����BaCl2����H2O2����Al��NO3��3����NaOH��
��1��ijͬѧ�벻�������Լ�����ͨ�����Թ�ȡ����������Һ�����������ʵ������Լ�ƿ������ȷ�ı�ǩ�����ܳɹ���______?����ܡ����ܡ�����
��2��ʵ���з��֣���һ���ڻ��ʱ�������Լ��μӵ�˳��ͬ���������Բ�ͬ����������______����һ���ڻ��ʱ�������Լ��μӺ��ʱ�䲻ͬ���������Բ�ͬ����������______�������漰������ԭ��Ӧ�Ļ�ѧ����ʽΪ______��
��3�������ͬѧ����FeSO4������������Fe2+��ԭ�Ե�ʵ�飬ÿ�μ������������Ѽ�������ʵ���Һ�����ϣ���д������������Ӧ�����ӷ���ʽ______��______��
��4��ʵ����ʵ�������Ƶ�FeSO4��Һ���ɳ��ڱ��棬���ڱ���ʱ����FeSO4��Һ����ʱ��������������______�����ţ���ֹˮ�⣬�����ټ���______�����������ƣ�Ч������ã�
�ο��𰸣���һ����1����Ͳ����ʱҪ����Һ�����͵㣬�Ҿ�ȷ��Ϊ0.1�������Ϊ28.0 mL�����Ӷ���������Ͳ�ȴ��µ�����ֵ�����������˵��������ֵ��ʵ��ֵƫС�����˴�ƫ���ˣ��ʿ̶�Ϊ���µ�����С����ѡC���ʴ�Ϊ��28.0��C��
��2��������ʳ����Һ�е�ˮ��Ҫ��������������Ϊ���ʣ��ʴ�Ϊ��������
������80mL?l?mol/L��NaCl��ҺҪ����100 mL������ʳ��0.1mol������Ϊ5.85 g����ƽ�ľ�ȷ��Ϊ0.1g���ʳ���5.9 g����Ҫ100?mL����ƿ������Һ��
�ʴ�Ϊ��5.9��100?mL����ƿ��?
������ ?FeSO4H2SO4BaCl2H2O2Al��NO3��3NaOHFeSO4��ɫ����dz��ɫ��ƺ�ɫ��ɫ����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫH2SO4����ɫ��������BaCl2��ɫ������ɫ����H2O2dz��ɫ��Һ��ɻƺ�ɫ����Al��NO3��3�μ���������ʱ���������ְ�ɫ��������֮�������г���NaOH��ɫ����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ�μ���������ʱ���������ְ�ɫ��������֮�������г�����1�����ȿ���ͨ����ɫ����ȷ������dz��ɫ��Ϊ����������
�����������μ�������Һ�����ְ�ɫ������Ϊ�Ȼ��������ְ�ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ�����������ƣ�dz��ɫ��ɺ��ɫ��Һ����˫��ˮ��
���Ȼ����μ���������Һ�����ְ�ɫ���������?���������Ƶμ�������Һ�����ְ�ɫ��������ɫ�������ܽ��Ϊ���������ʿ������֣��ʴ�Ϊ���ܣ�?
��2�����������Ƶμӵ��������У����ְ�ɫ��������ɫ�������ܽ⣬���������μӵ����������г��ְ�ɫ�������̻���ʧ�õ�������Һ���������Լ��μӵ�˳��ͬ���������Բ�ͬ�������Ǣݺ͢ޣ�
�������������������ƣ���Ӧ������ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ���������Լ��μӺ��ʱ�䲻ͬ���������Բ�ͬ������Ϊ�ٺ͢ޣ�������ԭ��Ӧ�Ļ�ѧ����ʽΪ�����������������ķ�Ӧ������������4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
�ʴ�Ϊ���ݺ͢ޣ��ٺ͢ޣ�4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
��3��Fe2+��ԭ�Լ���������������Ϊ�����ӵĹ��̣�����Ϊ����������˫��ˮ�ķ�ӦҺ����Ϊ������ķ�Ӧ�����ӷ���ʽ���£�3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
2Fe2++2H++H2O2�T2Fe3++2H2O���ʴ�Ϊ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��2Fe2++2H++H2O2�T2Fe3++2H2O��
��4��������������ʱ�������ܽ⣬���Է�ֹ����������ˮ���������������Һ���ױ������������ӣ��������������������ӷ�Ӧ�����������ӣ�
�ʴ�Ϊ���ڣ���ö������
���������
�����Ѷȣ�һ��
2��ѡ���� ���������У������ڼ��ȵ���
[? ]
A����Ͳ
B������ƿ
C����ͷ�ι�
D���Թ�
�ο��𰸣�D
���������
�����Ѷȣ���
3������� ָ��ʹ�������������Ѿ�ϴ�Ӹɾ�������Ʒʱ�ĵ�һ��������
��1��������ƽ______��
��2����Һ©��______��
��3����ɫʯ����ֽ���鰱��______��
�ο��𰸣���1��ʹ��������ƽ�ĵ�һ���ǵ�ƽ������ƽ�����������ȷ��
�ʴ�Ϊ����ƽ��
��2��ʹ�÷�Һ©��ʱ���������Ƿ�©ˮ�����Ե�һ������Ϊ��©��
�ʴ�Ϊ����©��
��3���������ܹ���������������ӣ��ú�ɫʯ����ֽ���鰱��ʱ�������Ƚ���ֽʪ��
�ʴ�Ϊ����ʪ��
���������
�����Ѷȣ�һ��
4��ѡ���� ������������©������������������ƽ���ܷ�Һ©������������ƿ������Ͳ����ȼ�ճף����������ʷ�����ǣ�������
A���٢ڢݢ�
B���ڢۢݢ�
C���٢ڢܢ�
D���ۢܢޢ�
�ο��𰸣���©�������ڹ��ˣ������������ڷ��벻���ܵĹ����Һ�壬�ʢ���ȷ��
�������������������Һ���������ᴿ��һ�ֲ����������ڷ������ܵĹ����Һ�壬�ʢ���ȷ��
����ƽ����������ҩƷ���������������������ʷ��룬�ʢ۴���
�ܷ�Һ©���Ƿ��뻥�����ܵ��ܶȲ�ͬ��Һ����������ʢ���ȷ��
��������ƿ����������ʵ�飬������һ�ַ������ʵķ����������ڷ������ܵ�����Һ�壬�ʢ���ȷ��
����Ͳ��������ȡҺ����������������������ʷ��룬�ʢ���
��ȼ�ճ���������ȼ��ʵ���õ����������������ʷ��룬�ʢߴ���
��ѡC��
���������
�����Ѷȣ���
5��ѡ���� ��������ƽ������������ʱ��������Ʒ��������������ϵ�λ�õߵ���ƽ��ʱ�����ϵ���������Ϊ10g������Ϊ0.5g������Ʒ������Ϊ��������
A��10.5g
B��10.0g
C��11g
D��9.5g
�ο��𰸣�D
���������
�����Ѷȣ���