1、选择题 某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s)△H>0。下列叙述正确的是
Z(g)+W(s)△H>0。下列叙述正确的是
[? ]
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.平衡后加入X,上述反应的△H增大
2、选择题 在固定容积的密闭容器中,可逆反应2X(?)+Y(g)?Z(s)已达到平衡,此时升高温度则气体混合物的密度增大.下列叙述正确的是( )
A.正反应为放热反应,X可能是气态、液态或固态
B.正反应为放热反应,X一定为气态
C.若X为非气态,则正反应为吸热反应
D.若加入少量的Z,该平衡向左移动
3、选择题 常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:(N2O4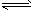 2NO2 △H >0)(a)将两容器置于沸水中加热(b)在活塞上都加2kg的砝码在以上两情况下,甲和乙容器的体积大小的比较,正确的是
2NO2 △H >0)(a)将两容器置于沸水中加热(b)在活塞上都加2kg的砝码在以上两情况下,甲和乙容器的体积大小的比较,正确的是
[? ]
A.(a)甲>乙(b)甲>乙
B.(a)甲>乙(b)甲=乙
C.(a)甲<乙(b)甲>乙
D.(a)甲>乙(b)甲<乙
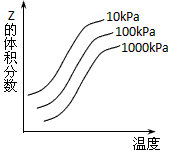
4、选择题 下图是温度和压强对X+Y 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中
Z的体积分数。下列叙述正确的是
[? ]
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中只有一种为气态,Z为气态
D.上述反应的逆反应的△H>0
5、填空题 某反应的平衡常数表达式为 ,恒容时,温度升高.H2浓度减小。分析下列问题:
,恒容时,温度升高.H2浓度减小。分析下列问题:
(1)该反应的化学方程式为:____________。
(2)温度升高,该反应的K值______________(填“增大”“减小”或“不变”),化学平衡移动后达到新的平衡,CO2和CO体积比_______________(填“增大”“减小”或“不变”)。
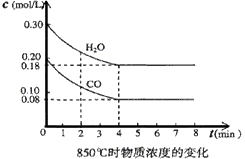
(3)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生反应,CO和H2O浓度变化如下图,则 0-4min的平均反应速率v(CO)=______ mol/(L・min),850℃的化学平衡常数的值K= __________。
(4)850℃时,在相同容器中发生反应CO2+ H2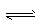 CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、 二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时 v(正) ______v(逆)(“大于”“ 小于”“等于”)。
CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、 二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时 v(正) ______v(逆)(“大于”“ 小于”“等于”)。