1���ƶ��� ��7�֣�ij���廯����A������ͼ��ʾ����ϵ�б仯����֪E��Һ�м��백ˮ������İ�ɫ�����ܿ��Ϊ����ɫ������Ϊ���ɫ��
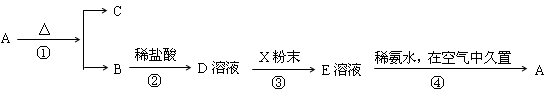
��1����д���������ʵĻ�ѧʽ��A?��C?��
��2���ڢ٢ڢܸۢ�����Ӧ������������ԭ��Ӧ����?(�����)��
��3����ֱ�д����Ӧ�ڵĻ�ѧ����ʽ�ͷ�Ӧ�۵����ӷ���ʽ����?����?��
�ο��𰸣���1��A��Fe(OH)3? C��H2O
��2���ۢ�
��3��Fe2O3 +6HCl===2FeCl3+3H2O? 2Fe3++Fe===3Fe2+
����������ɡ�E��Һ�м��백ˮ������İ�ɫ�����ܿ��Ϊ����ɫ������Ϊ���ɫ����A������֪AΪ��������������֪BΪ��������CΪˮ��DΪ�Ȼ�����EΪ�Ȼ���������
��1��A��Fe(OH)3? C��H2O
��2����2Fe(OH)3 ?Fe2O3 +3H2O�����ϼ۵ı仯�����ڷ�������ԭ��Ӧ��
?Fe2O3 +3H2O�����ϼ۵ı仯�����ڷ�������ԭ��Ӧ��
��Fe2O3 +6HCl=2FeCl3 +3H2O�����ϼ۵ı仯�����ڷ�������ԭ��Ӧ��
��2FeCl3 +Fe=3FeCl2��Fe�Ļ��ϼ۷����ı䣬����������ԭ��Ӧ��
��4Fe(OH)2 +O2 +2H2O=4Fe(OH)3��Fe�Ļ��ϼ۷����ı䣬����������ԭ��Ӧ��
�ʴ��Ǣۢ�
��3�����ݣ�2���Ĵ𰸿�֪��Fe2O3 +6HCl===2FeCl3+3H2O? 2Fe3++Fe===3Fe2+
��������Ϥ���ʵ�����������Ϊ�ƶ����ͻ�ƿڡ������Ŀ����Ϣ��һȷ����
�����Ѷȣ�һ��
2������� Ŀǰ������ʹ����㷺�Ľ���֮һ����֪�ڸ����£�Fe��ˮ�����ɷ�����Ӧ��?
Ӧ������װ�ã���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ����¡�Fe��ˮ�����ķ�Ӧʵ�顱��
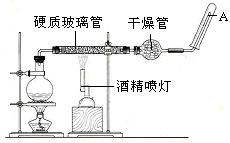
��ش����е����⡣
�������ڱ��е�λ����_______
��д���÷�Ӧ�Ļ�ѧ����ʽ��?��
��3���������������������ﷴӦԭ�������Ӹֹ죬�÷�Ӧ�Ļ�ѧ����ʽΪ?
��4���������Ͳ���ɵĺϽ�a mol������Pt�����ʵ�������Ϊx���гɷ�ĩ״��ȫ��Ͷ�뺬bmol HNO3��ϡ��Һ�У�ʹ���ַ�Ӧ����HNO3�Ļ�ԭ����ֻ��NO���Իش��������⣺
����HNO3���������ӣ���Һ�еĽ������ӺͲ�������ijɷ�����������������������ӷ�����д�±��հף�
?
| ��
| ��
| ��
| ��
|
��Һ�еĽ�������
| ?
| Fe2+
| ?
| ?
|
��������ɷ�
| Fe��Pt
| ?
| Pt
| Pt
|
?
�ڵ�x="0.5" ������Һ��Fe3+��Fe2+�����ʵ�����ȣ��ڱ�״���¹�����112mLNO��
��a =?��b =?��
�ο��𰸣���1���������ڣ��ڢ� ��? (1��)
��2��3Fe+4H2O(g) Fe3O4+4H2?(2��)
Fe3O4+4H2?(2��)
��3��2Al+Fe2O 3 Al2O3 + 2Fe? (2��)? (�𰸺���������)
Al2O3 + 2Fe? (2��)? (�𰸺���������)
��4����(2��)
?
��
��
��
��
��Һ�еĽ�������
Fe2+
Fe2+
Fe2+ Fe3+
Fe3+
��������ɷ�
Fe��Pt
Pt
Pt
Pt
��a =0.012��b = 0.02? (2��)
�����������1��Fe��Ԫ�����ڱ���λ�ڵ������ڣ��ڢ� �塣
��2��Fe��H2O��g����Ӧ����Fe3O4��H2����ѧ����ʽΪ��3Fe+4H2O(g)  Fe3O4+4H2
Fe3O4+4H2
��3���������������ﷴӦԭ�������Ӹֹ죬��ѧ����ʽΪ��2Al+Fe2O 3 Al2O3 + 2Fe?
Al2O3 + 2Fe?
��4������Ϊ��Feʣ�࣬������Һ����Fe2+������HNO3�����࣬Feȫ����Ӧ������ֻ��Pt��������HNO3������Fe2+������ΪFe3+����Һ����Fe2+��Fe3+��HNO3�ﵽ������ȫ��ת��ΪFe3+��
����Һ��Fe3+��Fe2+�����ʵ�����ȣ���Fe2+�����ʵ���Ϊnmol����Fe3+ҲΪnmol������������ԭ��Ӧ�����غ��֪��2n+3n=0.112L��22.4L/mol��3����n=0.003mol��Fe2+��Fe3+��Ϊ0.003mol��Pt�����ʵ�������Ϊx=0.5����Pt�����ʵ���Ϊ0.006mol������a=0.003mol+0.003mol+0.006mol=0.012mol��HNO3��Ӧ��ת��ΪFe(NO3)2��Fe(NO3)3��NO������HNO3�����ʵ���b=0.003mol��2+0.003mol��3+0.112L��22.4L/mol=0.02mol��
�����Ѷȣ�һ��
3������� ����ͼ��ʾ��װ���У���NaOH��Һ����м��ϡH2SO4�Ʊ�Fe��OH��2��ɫ������
�����Թܢ��������Լ���______��
�����Թܢ��������Լ���______��
��Ϊ���Ƶ�Fe��OH��2��ɫ��������ȷ�IJ���˳����______����������ţ�
A����ֹˮ��?B�������Թܢ���ڴ��ų���H2�Ĵ���
C���н�ֹˮ��?D�����Թܢ�͢��м����Լ�����������
��д���˹������漰���Ļ�ѧ����ʽ______��
�ο��𰸣����������ᷴӦ�����������ر�ֹˮ�У���ʹװ�æ���ѹǿ���ʹ���е�ҩƷ������У�����е�ҩƷ��Ӧ�õ��������������������Թ�I������Լ�ϡH2SO4����м���������������Һ���ʴ�Ϊ��ϡH2SO4����м��
���Թ�I������Լ�ϡH2SO4����м���������������Һ�����ܲ���������������ʹװ�æ���ѹǿ���ʹ���е�ҩƷ��������������У�����е�ҩƷ�������Ʒ�Ӧ�õ��������������ʴ�Ϊ��NaOH��Һ��
�۴����漰������������飬����Ҫ���װ�õ������ԣ���������װ���м����Լ����������ӣ���ֹˮ�У�����������������װ�â�Ҫ����װ�â��п����Ƿ��ž���Ҫ��װ�âܿڼ�������Ĵ��ȣ������崿�����ر�ֹˮ�У�������ѹ����ʹ���е�ҩƷ������У�����е�ҩƷ��Ӧ�õ��������������ʴ�Ϊ��DABC��
�������������ᷴӦ�������������������ܻ���û��Ӧ�������������������������Ӧ�������������������������ƣ��������������ᷴӦ���������ƺ�ˮ��������������������Ӧ��������������ˮ���ʴ�Ϊ��FeSO4+2NaOH�TFe��OH��2��+Na2SO4����д����H2SO4+2NaOH�TNa2SO4+2H2O����H2SO4+Fe��OH��2�TFeSO4+2H2O����
���������
�����Ѷȣ�һ��
4��ʵ���� ��16�֣�ͭ��Ũ���ᷴӦ��ʵ��װ����ͼ��ʾ��
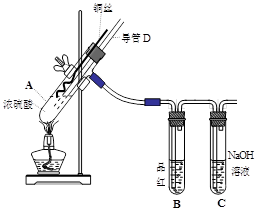
��1�� װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ��?����Ӧ�������Թ�B�е�������?���Թ�C��������?��
��2�� ����D���¶�(���߶�)Ӧλ��?��Һ���ϡ�Һ���£�������D�������У���ʵ��������ų�װ���е�SO2����?��
ʵ���з����Թ��ڳ��˲�����ɫ�����⣬��ͭ˿���滹�к�ɫ��������ɣ����п��ܺ���CuO��Cu2O��CuS��Cu2S��Ϊ̽���ijɷ֣����������µ�ʵ�顣
�������Ͽ�֪��Cu2O + 2HCl =CuCl2+ Cu + H2O�� 2Cu2O + O2���� 4CuO��2CuS+3O2����2CuO+2SO2��Cu2S+2O2����2CuO+SO2��CuS�� Cu2S��ϡHCl����Ӧ��
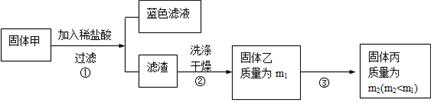 ��3�� �������ڿ���������ʱ��ʹ�õ�ʵ���������˲����������żܡ��ƾ����⣬�������У�?��
��3�� �������ڿ���������ʱ��ʹ�õ�ʵ���������˲����������żܡ��ƾ����⣬�������У�?��
��4�� ���չ����У���������Ӧ�⣬�����ܷ�����Ӧ�ķ���ʽΪ?��
��5�����ۣ�������CuO�����϶����е�������?��
�ο��𰸣�33.��16�֣���1��Cu +2H2SO4(Ũ) ��CuSO4+SO2��+2H2O (2��)��Ʒ����Һ��ɫ��2�֣������ն����SO2����ֹ��Ⱦ������2�֣�
��2��Һ���£������� (4��)
��3�������ǡ�����������ǯ����2�֣�����ǯ��д���۷֣�
��4��2Cu+O2��2CuO (2��)
��5��CuS��2�֣�
��������� ��1�� ��ʵ���о�����ͭ��Ũ����ķ�Ӧ�������Aװ���з����ķ�Ӧ����ʽΪCu +2H2SO4(Ũ) ��CuSO4+SO2��+2H2O����Ӧ����SO2���ɣ����B�е�Ʒ����Һ��Ư����ɫ��C�Թ������չ���SO2��Ŀ�ģ���ֹSO2��Ⱦ������
��2�� ����Aװ�����Ʊ�SO2�ķ���װ�ã����Ե���D���¶˱��������Һ�У����ܷ�ֹ������SO2����ӵ���D���ݳ�����������D����������ʵ������������ų�Aװ�õ�SO2��ͬʱ�ܹ�ƽ��A��B����ѹ����ֹB��Һ�嵹��������������ǰ�D�¶˴���Һ������
��3�� ���յ�ʵ���þ߱���ʹ�����µ�������������������ʹ�õĻ��������ǡ�����ǯ�ȡ�
��4���������е��жϣ��ù��������CuO��Cu2O��CuS��Cu2S�������ϡ�����ܽ⣬������֪�ķ�Ӧ����Ӧ�õ��Ĺ����ҿ�����Cu��CuS��Cu2S���Թ����ҽ������գ���˳�����֪�ļ������շ�Ӧ�⣬�����ܷ����ķ�ӦΪ����ͭ������2Cu+O2��2CuO��
��5�� ���ݣ�4���ķ��������÷�Ӧ�ķ���ʽ�Ը��ֳɷ����ս�������ƶϷ�������Cu���գ���������CuOʹ�������أ���CuS���գ����ղ���CuOʹ������С����Cu2S���գ���������CuO���������䡣���Ҫ��������������ǰ��������С��������б��뻹������ʹ����ǰ��������С��CuS��
�����Ѷȣ�һ��
5������� ij����֣���Ҫ�ɷ�ΪFe����Ʒ�к�������ͭ����ȣ������ɷֺ��ԣ���Ϊ�˲ⶨ�úϽ������ĺ���������������¹������̣�
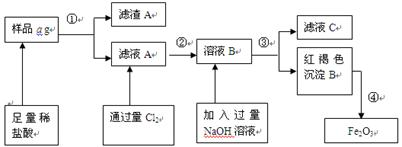
(1)ȡ��Ʒa g����ȡʱʹ�õ���Ҫ��������Ϊ_____?_______��
(2)��ҺA��������Ҫ����_______??��__? __ _��д��ѧʽ����
�����ٵ�����?����ʹ�õIJ���������______________________________��
(3)д������ҺB���ɺ��ɫ����B�����ӷ���ʽ________________________________��
(4) ������Fe2O3�������������Ϊb g���������Ʒ����Ԫ�ص������ٷ����ı���ʽΪ���ú�a��b��ʽ�ӱ�ʾ��_____________��
(5)�����֤��ҺA�к�Fe2+��������Fe3+______________________?_____________��
�ο��𰸣�(1)������ƽ
(2) FeCl2��AlCl3���� ���� ��?©�����ձ��������� ������д���÷֣�©дһ����1�֣�
(3) Fe3+ + 3OH - ="=" Fe(OH)3��
(4) (7b/10a)��100%? {��(70b/a)%}
(5)ȡ������ҺA���Թ��У��μ���KSCN��Һ����Һ����ɫ��(2��)
�ټ���ˮ����ͨ����������Һ��ΪѪ��ɫ����1�֣�?������������Ҳ���ԣ�
�����������
�����Ѷȣ�һ��