1、选择题 下列事实不能用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.H2、I2、HI混合气体加压后颜色变深
C.红棕色的NO2加压后颜色先变深再变浅
D.工业上生产硫酸的过程中使用过量的空气,以提高二氧化硫的利用率
参考答案:B
本题解析:如果改变影响平衡的1个条件,平衡就向能够减弱这种改变的方向进行,中这就是勒夏特列原理,该原理适用于所有的平衡体系。A、开启啤酒瓶后,越强减小,气体的溶解度减小,因此瓶中马上泛起大量泡沫,可以用勒夏特列原理解释,A不符合题意;B、反应H2+I2 2HI是体积不变的可逆反应,因此H2、I2、HI混合气体加压后平衡不移动,但单质碘的浓度增大,因此颜色变深,不能用勒夏特列原理解释,B正确;C、NO2存在平衡关系2NO2
2HI是体积不变的可逆反应,因此H2、I2、HI混合气体加压后平衡不移动,但单质碘的浓度增大,因此颜色变深,不能用勒夏特列原理解释,B正确;C、NO2存在平衡关系2NO2 N2O4,因此红棕色的NO2加压后平衡向正反应方向移动,所以颜色先变深再变浅,可以用勒夏特列原理解释,C不符合题意;D、SO2与氧气反应的方程式为2SO2+O2
N2O4,因此红棕色的NO2加压后平衡向正反应方向移动,所以颜色先变深再变浅,可以用勒夏特列原理解释,C不符合题意;D、SO2与氧气反应的方程式为2SO2+O2 2SO3,增大氧气的浓度平衡向正反应方向移动,因此SO2的浓度增大,D不符合题意,答案选B。
2SO3,增大氧气的浓度平衡向正反应方向移动,因此SO2的浓度增大,D不符合题意,答案选B。
本题难度:简单
2、填空题 (16分)现有反应:mA(g)+nB(g)?pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为?热反应,且m+n?p(填“>”、“=”“<”)。
(2)减压时,A的质量分数?(填“增大”“减小”或“不变”)。
(3)若加入B(体积不变 ),则A的转化率?(填“增大”“减小”或“不变”)。
),则A的转化率?(填“增大”“减小”或“不变”)。
(4)若升高温度,则平衡时B、C的浓度之比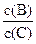 将?(填“增大”“减小”或“不变”)。
将?(填“增大”“减小”或“不变”)。
(5)若加入催化剂,平衡时气体混合物的总物质的量?(填“增大”“减小”或“不变”)。
(6)若B是有色物质,A、 C均无色,则加入C(体积不变)时混合物颜色?(填“变深”、“变浅”或“不变”);而维持容器内压强不变,充入氖气时,混合物颜色?(填“变深”、“变浅”或“不变”)。
参考答案:(16分)
(1)放热?,>?(2)增大?(3)增大
(4)减小?(5)不变?( 6)变深,变浅
6)变深,变浅
本题解析:略
本题难度:一般
3、选择题 对于3W(g) + 2X(g) = 4Y(g) + 3Z(g) ,下列反应速率关系正确的是
[? ]
A.υ(W) =3υ(Z)
B.2υ(X) =3υ(Z)
C.2υ(X) =υ(Y)
D.3υ(W) =2υ(X)
参考答案:C
本题解析:
本题难度:简单
4、选择题 在恒温恒容的密闭容器中进行的气体反应:H2(g)+Br2(g) 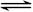 ?2HBr(g),能说明反应已达平衡状态的是 ( ? )
?2HBr(g),能说明反应已达平衡状态的是 ( ? )
A.容器内混合气体颜色不随时间改变而改变
B.H2、Br2的反应速率相等
C.容器内的压强不随时间改变而改变
D.混合气体的密度不随时间改变而改变
参考答案:A
本题解析:
正确答案:A
A.正确,容器体积不变,容器内混合气体颜色不随时间改变而改变,说明Br2浓度不变;? B.不正确,H2、Br2的方程式前计量数相同,H2、Br2的反应速率比是1:1
C.不正确,本反应是气体体积不变的反应,容器内的压强不随时间改变而改变? D.不正确,本反应全是气体,气体的总质量不随反应进行而改变,混合气体的密度不随时间改变而改变。
本题难度:一般
5、计算题 (8分)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应: N2(g)+3H2(g) 2NH3(g)(注:要求每步均要写出计算过程)
2NH3(g)(注:要求每步均要写出计算过程)
(1)若反应进行到某时刻t时,nt(N2)="6.5" mol,nt(NH3)="3" mol,计算a的值。
(2)反应达平衡时,混合气体的体积为358.4 L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(3)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)等于多少?
参考答案:(8分)
(1)解法一:由反应的化学方程式得知,反应掉的N2和生成NH3的物质的量之比为1∶2,设反应掉N2的物质的量为x mol。则x∶6=1∶2?解之x=3 ?a=6.5+1.5=8。
解法二:? N2?+3H2 2NH3
2NH3
开始时:a? b? 0
转化? 1.5? 4.5? 3
t时:?6.5 ? 3
在t时生成3 mol NH3,消耗了1.5 mol N2,所以a=6.5+1.5=8(3分)
(2)n (NH3)=(358.4L/22.4L/mol)×25%="16" mol×25%="4" mol(3分)
(3) 3∶3∶2(3分)
本题解析:略
本题难度:一般