1、选择题 醋酸是一种常见的弱酸,为了证明醋酸是弱电解质,某同学开展了题为“醋酸是弱电解质的实验探究”的探究活动。该同学设计了如下方案,其中错误的是 ( )
A.先配制一定量的0.10 mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质
B.先配制一定量0.01 mol/L和0.10 mol/L的CH3COOH,分别用pH计测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质
C.取等体积、等pH的CH3COOH溶液和盐酸分别与足量锌反应,若测得反应过程中醋酸产生H2较慢且最终产生H2较多,则醋酸为弱酸
D.配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质
参考答案:C
本题解析:
答案:C
C.不正确,取等体积、等pH的CH3COOH溶液和盐酸分别与足量锌反应,因醋酸难电离,醋酸浓度较大,若测得反应过程中产生H2较快且最终产生H2较多,则醋酸为弱酸
本题难度:简单
2、选择题 已知存25°时几种物质的0. 1mol.L-1溶液的电离度如下表:

将足量锌粉分别放入等体积且氢离子浓度相等的下列溶液中:
①H2SO4溶液;②HCl溶液;③CH3COOH溶液;④NaHSO4溶液。
放出氢气的量的关系正确的是(假设浓度对电离度的影响忽略不计)
[? ]
A.①=②=④>③
B.②>④>①>③
C.③>①>④>②
D.③>④>①>②
参考答案:D
本题解析:
本题难度:一般
3、选择题
A.Fe3+、NO 、Cl-、Na+
、Cl-、Na+
B.Ca2+、HCO 、Cl-、K+
、Cl-、K+
C.NH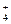 、Fe2+、SO
、Fe2+、SO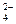 、NO
、NO
D.Cl-、SO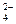 、K+、Na+
、K+、Na+
参考答案:BC
本题解析:c水(H+)=1.0×10-13 mol・L-1,则该溶液可能是强碱性溶液,也可能是强酸性溶液,总之,水的电离被抑制。因而“一定不可能大量存在”是指酸性和碱性条件下都不能大量存在。
本题难度:一般
4、选择题 可以判定某酸(HA)是强电解质的事实是( )
A.该酸加热至沸腾不分解
B.0.01 mol・L-1该酸的pH=2
C.该酸可以溶解Cu(OH) 2
D.该酸与CaCO3反应放出CO2
参考答案:B
本题解析:强电解质完全电离,不存在电离平衡,B中氢离子浓度和该一元酸的浓度相等,说明完全电离,不存在电离平衡,所以选项B正确;A是酸的稳定性,C和D都是表现酸性,但并能确定是否是强电解质,答案选B。
点评:弱电解质的证明,是基于与强电解质对比进行的。弱电解质与强电解质最大的区别就是弱电解质存在电离平衡,而强电解质不存在电离平衡。因此只要证明有电离平衡存在,就证明了弱电解质。
本题难度:简单
5、填空题 现有25℃时,0.1 mol/L的氨水。请回答下列问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中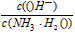 ____(填“增大”“减小”或“不变”)。
____(填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式__________________;所得溶液的pH_______7(填“<”“>”或“=”), 用离子方程式表示其原因__________________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol/L,则c(SO42-)=_____________。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比1:1,则所得溶液中各离子物质的量浓度由大到小的顺序是______________。
参考答案:(1)减小
(2)NH3・H2O+H+=NH4++H2O;<;NH4++H2O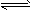 NH3・H2O+H+
NH3・H2O+H+
(3)a/2mol/L
(4)c(NH4+)>c(SO42-)>c(H+)>c(OH-)
本题解析:
本题难度:一般