1������� д����SiO2Ϊԭ���Ʊ�H2SiO3�Ļ�ѧ����ʽ___________________________��
�ο��𰸣���ì�ܣ�ԭ����ϡ�
�����������������CO2��SiO2��Na2SiO3��H2CO3��H2SiO3�Ȼ���������ʣ�����ͬѧ�ǵ������������Լ�˼ά�������Ժ�����ԡ���Ӧ��������Һ�н��еķ�Ӧ����Ӧ֮�����ܹ�����������������H2CO3��H2SiO3����Ӧ���ϡ�ǿ�������ᡱ�ĸ��ֽⷴӦԭ��������Ӧ�����ڸ�������״̬�µķ�Ӧ������CO2�ɴ����������ݳ���ʹ�÷�Ӧ���Է�������������H2CO3��H2SiO3�ء�
����������������ˮ��Һ�н��еĸ��ֽⷴӦ�����ǹ��������֮��ķ�Ӧ����ˮ�����������dz����µķ�Ӧ�����Ǹ��������µķ�Ӧ��������Ӧ��������ͬ��ʵ����û�пɱ��ԣ���Ϊ���ǵķ�Ӧԭ������Ӧ�����뱾�ʾ���ͬ��
�����Ѷȣ���
2������� ��14�֣�һ�������£�����A��Eת����ϵ��ͼ������AΪ���ʣ�������EΪ��ɫҺ�塣
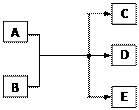
��1����A��C��D������Ԫ�أ�CΪ�ȼҵ��ԭ�ϣ�
D��Һ����Ư���ԣ���A��B��Ӧ�Ļ�ѧ����ʽ��?��D��Һ��ʹKI������Һ����ɫ����D��KI����Һ�з�Ӧ�����ӷ���ʽ��?������B��Һ��NH4HCO3��Һ���ȣ���������G�����ӷ���ʽ��?��G������������������?��
��2����AΪ��ɫ������BΪij���Ũ��Һ��D���γ��������ɫ���塣A��B��Ӧ�Ļ�ѧ��?��a molA��������B��ַ�Ӧ��������Dͨ��NaOH��Һ�У�ǡ����ȫ��Ӧ��������NaOH�����ʵ����ķ�Χ��?��
��3��������1������2���е�D����ʹƷ����Һ��ɫ��������ɫ�����Һ��̽��ʹƷ����Һ��ɫ�����ʵ�ʵ�鷽����?��
�ο��𰸣���14�֣�ÿ��2�֣���1�� Cl2+2NaOH=NaCl+NaClO+H2O��2I��+ClO��+H2O=I2+Cl��+2OH������
NH4����HCO3����2OH�� = ��CO32����NH3����2 H2O����������?��
��2��Cu+2H2SO4��Ũ����14�֣�ÿ��2�֣���1�� Cl2+2NaOH=NaCl+NaClO+H2O��2I��+ClO��+H2O=I2+Cl��+2OH������
NH4����HCO3����2OH�� = ��CO32����NH3����2 H2O����������?��
��2��Cu+2H2SO4��Ũ��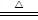 CuSO4+SO2��+2H2O��a mol��n(NaOH)��2a mol��
CuSO4+SO2��+2H2O��a mol��n(NaOH)��2a mol��
��3��ȡ������ɫ�����Һ���ȣ�����Һ�ָ���ɫ������SO2ʹƷ����ɫ������Һ����죬����NaClOʹƷ����ɫ�������𰸾��÷֣��� CuSO4+SO2��+2H2O��a mol��n(NaOH)��2a mol��
��3��ȡ������ɫ�����Һ���ȣ�����Һ�ָ���ɫ������SO2ʹƷ����ɫ������Һ����죬����NaClOʹƷ����ɫ�������𰸾��÷֣���
�����������
�����Ѷȣ�һ��
3������� ���г�����������A��B��C�ͳ�������ס��ҡ���������D��E��F��G��H������֮���ܷ������·�Ӧ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������
 ?
?
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ�� A?����?
��2��д����Ӧ�ڵĻ�ѧ����ʽ?
��3��д�����з�Ӧ���ӷ���ʽ��
��Ӧ��?
��Ӧ��?
��Ӧ��?
�ο��𰸣���1��Na? HCl
��2��H2+Cl2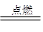 2HCl
2HCl
��3����Ӧ�ۣ�2Al��2H2O��2OH����2AlO2����3H2��
��Ӧ�ݣ�2Fe2��+ Cl2=?2Fe3�� ��2Cl��?��Ӧ�ޣ�Fe3��+ 3OH��=?Fe(OH)3��
�����������������A����ɫ��ӦΪ��ɫ��ӦΪNa����ˮ��Ӧ���ɵ������ΪH2��DΪNaOH������ɫ������ΪCl2�����ΪHCl��EΪ���ᣬ����NaOH��Ӧ����������BΪAl�����ɫ����HΪFe��OH��3����CΪFe��FΪFeCl2?��GΪFeCl3����1�������Ϸ�����֪AΪNa����ΪHCl�ʴ�Ϊ��Na��HCl��2����Ӧ��ΪH2+Cl2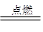 2HCl��3����Ӧ�۵Ļ�ѧ����ʽΪ��2Al+2NaOH +2H2O==2NaAlO2 + 3H2�������ӷ���ʽΪ��2Al+2H2O+2OH��==2AlO2��+3H2������Ӧ��ΪFeCl2��Cl2�ķ�Ӧ������ʽΪ2FeCl2+Cl2�T2FeCl3�����ӷ���ʽΪ��2Fe2++Cl2="2" Fe3++2Cl-?��Ӧ����ΪFeCl3��NaOH�ķ�Ӧ������ʽΪFeCl3+3NaOH�TFe��OH��3��+3NaCl�����ӷ���ʽΪ��Fe3+ +3OH-�TFe��OH��3����
2HCl��3����Ӧ�۵Ļ�ѧ����ʽΪ��2Al+2NaOH +2H2O==2NaAlO2 + 3H2�������ӷ���ʽΪ��2Al+2H2O+2OH��==2AlO2��+3H2������Ӧ��ΪFeCl2��Cl2�ķ�Ӧ������ʽΪ2FeCl2+Cl2�T2FeCl3�����ӷ���ʽΪ��2Fe2++Cl2="2" Fe3++2Cl-?��Ӧ����ΪFeCl3��NaOH�ķ�Ӧ������ʽΪFeCl3+3NaOH�TFe��OH��3��+3NaCl�����ӷ���ʽΪ��Fe3+ +3OH-�TFe��OH��3����
�����Ѷȣ�һ��
4������� ��Ԫ�����ڱ�������Ԫ���У�A��B��C��M�ǵ��ʡ�M��һ���ճ����ý������й�ת����ͼ��
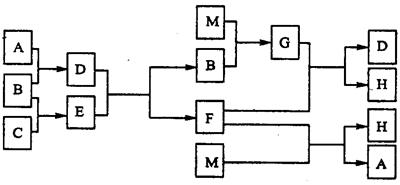
��ش�
��1��Ԫ��M��Ԫ�����ڱ���λ�ã�?���ڣ�?���塣
��2����д��B��C�ڼ��������·�Ӧ�Ļ�ѧ����ʽ��?
�� C��D��Ӧ�Ļ�ѧ����ʽΪ��?
��д��M��F��ˮ��Һ��Ӧ�����ӷ���ʽ��?
��3����1mol E��1mol̼�����ƻ�Ϸ����ܱ������м��ȣ�������300�澭��ַ�Ӧ���ų����塣
���
�������ڲ����Ĺ����������Ƽ������ʵ���?��
���������з����Ļ�ѧ��Ӧ�Ļ�ѧ����ʽ��?��
�ο��𰸣���15�֣�
��1��������A����1�֣�
��2��2Na+O2?Na2O2��2�֣�? 2Na+2H2O=2NaOH+H2����2�֣�
��3��2Al+2OH��+2H2O?2AlO2��+3H?2����2�֣�
��4��̼���ƣ�1�֣���1mol��1�֣����������ƣ�1�֣� 1mol��1�֣�
2NaHCO3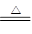 Na2CO3+H2O��+CO2��? 2Na2O2+2CO2
Na2CO3+H2O��+CO2��? 2Na2O2+2CO2?2Na?2CO3+O2
2Na2O2+2H2O===4NaOH+O2��ÿ��1�֣�
���������һ��Ҫע�Ȿ�����漰��Ԫ�ؾ�Ϊ������Ԫ�أ�M��һ���ճ����ý�������֪MΪ�������͵���B�ɷ�Ӧ������B�Ļ����P���ʣ��ɲ²�BΪ������������֪D��E�ֱ�����A��C��������Ӧ�õ�����Ϊ�������ҿɷ�Ӧ�������������Ʋ��D��EӦ����Na2O2��CO2��Na2O2��H2O������D��E�IJ���F��������Ӧ��֪D��EӦ����Na2O2��H2O��Ӧ������F��NaOH����F��NaOH����M��������Ӧ������A��H����֪AΪ������
����Ϊֹ����֪A��B��C�ֱ�Ϊ�������������Ƶ��ʡ�
��3����1mol Na2O2��1mol̼�����ƻ�Ϸ����ܱ������м��ȣ��������з�Ӧ��
2NaHCO3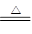 Na2CO3+H2O��+CO2��
Na2CO3+H2O��+CO2��
2Na2O2+2CO2?2Na?2CO3+O2
2Na2O2+2H2O===4NaOH+O2��ÿ��1�֣�
NaHCO3�ֽ��������������ǡ����Na2O2��Ӧ������Ӧ�IJ��
�����Ѷȣ�һ��
5������� A��B��C��X��Ϊ�����Ĵ��������֮��������ת����ϵ������Ʒ����ȥ����
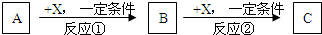
�Իش�
��1����X��ǿ�����Ե��ʣ���A��������______��
a��S?b��N2?c��Na?d��Mg?e��Al
��2����X�ǽ������ʣ���C��ˮ��Һ�е���AgNO3��Һ������������ϡHNO3�İ�ɫ��������B�Ļ�ѧʽΪ______��C��Һ������ʱӦ��������X�������ǣ��ñ�Ҫ�����ֺ����ӷ���ʽ��ʾ��______�������C��Һ�н���Ԫ�ؼ�̬�IJ���������______��
��3����A��B��CΪ��ij����Ԫ�ص��������XΪǿ����ʣ�A��Һ��C��Һ��Ӧ����B����B�Ļ�ѧʽΪ______��X�Ļ�ѧʽ����Ϊ��д����ͬ�����ʣ�______��______����Ӧ�ٵ����ӷ���ʽΪ______��
�ο��𰸣���1����X��ǿ�����Ե��ʣ���ת����ϵAX
���������
�����Ѷȣ�һ��