1��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ����
A����������ͨ����������������Һ�У�H2S��2OH��=S2����2H2O
B����������ϡ���ᷴӦ��Fe��2H+=Fe2++H2��
C���Ȼ�����Һ��Ũ��ˮ��Ӧ��Fe3+��3OH��=Fe(OH)3��
D��Al2O3�������Al2O3��6H+ =2Al3����3H2O
�ο��𰸣�AD
���������
��ȷ�𰸣�A D
B������ȷ����������ϡ���ᷴӦ��Fe��4H+��NO3�D=Fe3����NO����2H2O
C������ȷ���Ȼ�����Һ��Ũ��ˮ��Ӧ��Fe3+��3NH3��H2O=Fe(OH)3����3NH4��
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ�У��������ӷ���ʽH����OH����H2O��ʾ����
A��NH4Cl+NaOH NaCl��NH3��+H2O
NaCl��NH3��+H2O
B��NaOH+HNO3��NaNO3+H2O
C��M g(OH)2+2HCl��MgCl2+2H2O
D��NaOH +NaHCO2��NaHCO3+H2O
�ο��𰸣�B
����������������ӷ���ʽH����OH����H2O��֪���÷�Ӧ����ǿ���ǿ�Ӧ�������ɵ����ǿ����Եģ�����ѡ��B��ȷ������ѡ��Ǵ���ģ���ѡB��
�������������ӷ���ʽ�������Ա�ʾ����ķ�Ӧ�������Ա�ʾijһ�෴Ӧ�����Կ��ܻ��ж����ѧ����ʽ��Ӧͬһ�����ӷ���ʽ������ھ����ж�ʱ��Ҫע�⡣
�����Ѷȣ�һ��
3��ѡ���� ������CO2ͨ��NaOH��Ba(OH)2�Ļ��ϡ��Һ�У����ɳ��������ʵ�����n����ͨ��CO 2�����V���Ĺ�ϵ��ͼ��ͼ��AB�α�ʾ���Ⱥ����ӷ���ʽ�ǣ�?��
2�����V���Ĺ�ϵ��ͼ��ͼ��AB�α�ʾ���Ⱥ����ӷ���ʽ�ǣ�?��
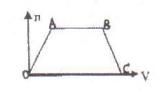
��CO2+OH-=HCO3-
��CO2+2OH-=CO32-+H2O
��CO32-+Ba2+=BaCO3��
��BaCO3+CO2+H2O=Ba2++2HCO3-
��CO32-+CO2+H2O=2HCO3-
A���ڢ�
B���ݢ�
C���ܢ�
D���ܢ�
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��д��ȷ����
[? ]
A��̼�������Һ�м�������ʵ���������������Һ��Ca2++2HCO3-+2OH-=CaCO3��+2H2O+CO32-
B����NaAlO2��Һ�м���������Һ�����ԣ�A1O2-+4H+=Al3++2H2O
C����̼�������Һ�м��������NaOH��Һ��HCO3-+OH-=CO32-+H2O
D��Cl2��H2O��Ӧ��Cl2+H2O=2H++Cl-+C1O-
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5��ѡ���� �����������Һ����μ���Ba(OH)2��Һ�����ܷ����ķ�Ӧ�����ӷ���ʽ��
A��NH4+ + SO42��+ Ba2+ +OH�� BaSO4��+ NH3��H2O
BaSO4��+ NH3��H2O
B��2Al3+ + 3SO42��+3Ba2+ +6OH�� 3BaSO4��+ 2Al(OH)3��
3BaSO4��+ 2Al(OH)3��
C��Al3+ + 2SO42��+ 2Ba2+ + 4OH�� 2BaSO4��+ AlO2��+ 2H2O
2BaSO4��+ AlO2��+ 2H2O
D��NH4++Al3+ +2SO42��+2Ba2+ +4OH�� 2BaSO4��+ Al(OH)3��+ NH3��H2O
2BaSO4��+ Al(OH)3��+ NH3��H2O
�ο��𰸣�BD
��������������[NH4Al��SO4��2?12H2O]��һ�ָ��Σ�������Һ����μ���Ba��OH��2��Һ����������������ӣ�ͬʱ���������ӳ��������ӣ������������������࣬���������ȫ��������ͬʱ�����ӳ�����ȫ�����������������Ӻ�笠����ӽ������һˮ�ϰ����������������ܽ��ڰ�ˮ�У��������������������������������ܽ⣬�������ӷ�Ӧ˳����д���ӷ���ʽ�жϣ�A����Ӧ�������������������ᱵ����������������������A����B��NH4Al��SO4��2��Ba��OH��2����2��3��Ϸ�Ӧ�������ᱵ����������������������ʱ��������ӹ�������Ӧ�����ӷ���ʽΪ2Al3+ + 3SO42��+3Ba2+ +6OH�� 3BaSO4��+ 2Al(OH)3����B��ȷ��C��NH4Al��SO4��2��Ba��OH��2����1��2ǡ�÷�Ӧ�������ᱵ��������������������һˮ�ϰ�������������������0.5mol����������������ȫ�ܽ⣬��Ӧ�����ӷ���ʽΪ��NH4++Al3++2SO42-+2Ba2++5OH-��2BaSO4��+NH3?H2O+AlO2-+2H2O��C����ȷ��D��NH4Al��SO4��2��Ba��OH��2����1��2ǡ�÷�Ӧ�������ᱵ��������������������һˮ�ϰ�����Ӧ�����ӷ���ʽΪNH4++Al3+ +2SO42��+2Ba2+ +4OH��
3BaSO4��+ 2Al(OH)3����B��ȷ��C��NH4Al��SO4��2��Ba��OH��2����1��2ǡ�÷�Ӧ�������ᱵ��������������������һˮ�ϰ�������������������0.5mol����������������ȫ�ܽ⣬��Ӧ�����ӷ���ʽΪ��NH4++Al3++2SO42-+2Ba2++5OH-��2BaSO4��+NH3?H2O+AlO2-+2H2O��C����ȷ��D��NH4Al��SO4��2��Ba��OH��2����1��2ǡ�÷�Ӧ�������ᱵ��������������������һˮ�ϰ�����Ӧ�����ӷ���ʽΪNH4++Al3+ +2SO42��+2Ba2+ +4OH�� 2BaSO4��+ Al(OH)3��+ NH3��H2O����D��ȷ����ѡBD��
2BaSO4��+ Al(OH)3��+ NH3��H2O����D��ȷ����ѡBD��
�����Ѷȣ���