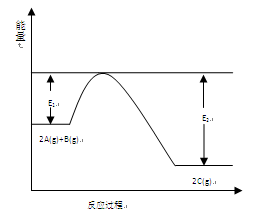
1、填空题 (9分)一定条件下,在一容积可变的密闭容器中,反应: 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
时间(min)
| 0
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
|
n(A)
| 2.00
| 1.90
| 1.82
| 1.76
| 1.64
| 1.54
| 1.50
| 1.50
| 1.50
|
n(B)
| 1.00
| 0.95
| 0.91
| 0.88
| 0.82
| 0.77
| 0.75
| 0.75
| 0.75
|
n(C)
| 0
| 0.10
| 0.18
| 0.24
| 0.36
| 0.46
| 0.50
| 0.50
| 0.50
|
回答下列问题:
(1)反应 的正反应△H?(填“大于”或“小于”)0。
的正反应△H?(填“大于”或“小于”)0。
(2)该反应平衡时,下列说法不正确的是?
(A)气体的密度不再改变?(B)A的物质的量浓度不变
(C)放出或吸收的热量不再变化?(D)v正(A)=v逆(A)=0
(3)toC时,在一容积为2L的恒容密闭容器内加入0.4molA和0.6molB,在一定条件下发生反应,反应中C的物质的量浓度变化情况如下图:
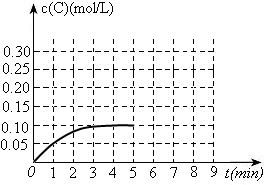
①该温度下,反应: 的平衡常数K=?。
的平衡常数K=?。
②反应进行到1分钟时B物质的量为?。
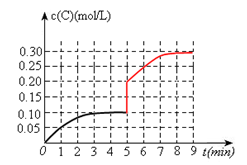
③在第5min时,将容器的体积缩小一半后,若在第8min达到新的平衡时A的总转化率为75%,请在上图中画出第5min到新平衡时C的物质的量浓度的变化曲线。
参考答案:(共9分)
(1)<?(2)D (3)①? 4?②0.55mol?③画图
本题解析:(1)产物总能量小于反应物总能量,故正反应是放热反应,△H<0
(2)化学平衡是一动态平衡,v正(A)=v逆(A)≠0
(3)①由图可知,平衡时c(C)=0.1mol/L,由方程式可求出c(A)、c(B)分别为0.1mol/L、0.25mol/L,进而可求出K=4
②由图可知,反应进行到1分钟时c(C)=0.05mol/L,即0.1mol,可求出B消耗了0.05mol;还剩余0.55mol
③在第5min时,将容器的体积缩小一半,c(C)瞬间增大一倍,即0.2mol/L;在第8min达到新的平衡时A的总转化率为75%,则可求出生成C为0.3mol,c(C)=0.3mol/L。
本题难度:一般
2、选择题 一定条件下,在反应2SO2 (g) +O2(g)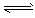 2SO3(g)平衡体系中: n (SO2) =2.0 mol/L , n(O2) = 0.8 mol/L, n (SO3)=2.4 mol/L ,则 SO2 的起始浓度的范围为
2SO3(g)平衡体系中: n (SO2) =2.0 mol/L , n(O2) = 0.8 mol/L, n (SO3)=2.4 mol/L ,则 SO2 的起始浓度的范围为
[? ]
A . 0.4~2.0 mol/L
B . 0.4~4.4 mol/L
C . 0~4 mol/L
D . 无法确定
参考答案:B
本题解析:
本题难度:一般
3、选择题 在高温、高压和催化剂条件下的密闭容器中,进行反应:N2(g)+3H2(g) 2NH3(g),下列有关说法不正确的是(?)
2NH3(g),下列有关说法不正确的是(?)
A.达到平衡时,正反应速率等于逆反应速率
B.增大氢气的浓度可增大反应速率
C.在上述条件下,氢气能全部转化为氨气
D.达到平衡时,体系中各物质的浓度不再改变
参考答案:C
本题解析:因为是可逆反应,氢气不能全部转化为氨气,达到平衡时,体系中各物质的浓度不再改变。
本题难度:一般
4、选择题 一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是(? )
 ?
?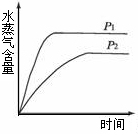
温度(T)的影响 ?压强(p)的影响
A.CO2(g)+2NH3(g) 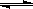 CO(NH2)2(s) + H2O(g);△H<0
CO(NH2)2(s) + H2O(g);△H<0
B.CO2(g)+ H2(g) 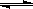 CO(g) + H2O(g);△H>0
CO(g) + H2O(g);△H>0
C.CH3CH2OH(g) 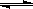 CH2=CH2(g) + H2O(g);△H>0
CH2=CH2(g) + H2O(g);△H>0
D.2C6H5CH2CH3(g) + O2(g )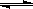 2C6H5CH=CH2(g) + 2 H2O(g);△H<0
2C6H5CH=CH2(g) + 2 H2O(g);△H<0
参考答案:A
本题解析:根据图像可知,T2大于T1,P1大于P2。温度高水蒸气的含量降低,说明升高温度平衡向逆反应方向移动,即正反应是放热反应;压强增大,水蒸气的增大,说明增大压强,平衡向正反应方向移动,即正反应是体积减小的,所以答案选A。
本题难度:一般
5、填空题 (14分)中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子
| K+
| Na+
| NH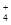
| SO
| NO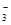
| Cl-
|
浓度/mol?L-1
| 4×10-6
| 6×10-6
| 2×10-5
| 4×10-5
| 3×10-5
| 2×10-5
|
根据表中数据计算PM2.5待测试样的pH = ? 。
(2) NOx是汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
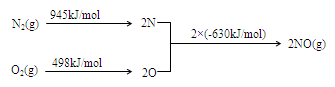
① N2(g)+O2(g) 2NO(g)△H=?。
2NO(g)△H=?。
②当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式?。
③ 汽车汽油不完全燃烧时还产生CO,有人设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g),已知该反应的△H>0,该设想能否实现??。
(3)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
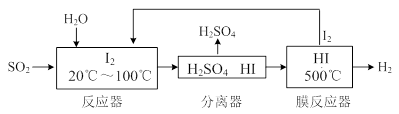
① 用离子方程式表示反应器中发生的反应 ? 。
② 用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是?。
③ 用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量、长寿命的镍氢电池。电池充放电时的总反应为:Ni(OH)2+M  ?NiO(OH)+MH,电池放电时,负极电极反应式为 ? ; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸。
?NiO(OH)+MH,电池放电时,负极电极反应式为 ? ; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸。
参考答案:⑴ 4?⑵① +183kJ/mol;② 2NO+2CO催化剂 2CO2+N2;③ 不能
⑶① SO2+I2+2H2O=SO +2I-+4H+?
+2I-+4H+?
②HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行?
③MH+OH--e-=H2O+M
本题解析:(1)题目所示的微粒中阳离子所带的正电荷数是:4×10-6×1+6×10-6×1+2×10-5×1=3×10-5mol/L,阴离子所带的负电荷总数是:2×4×10-5+1×3×10-5+1×2×10-5=13×10-5 mol/L>3×10-5mol/L,根据溶液呈电中性原理,溶液中还应该含有大量的H+。所以溶液显酸性。c(H+)=13×10-5 mol/L-3×10-5mol/L=1×10-4 mol/L,所以pH="4." (2)①反应热就是断裂化学键吸收的热量与形成化学键释放的热量的差值。因此 N2(g)+O2(g 2NO(g)△H=+945KJ/mol+498KJ/mol-2×630KJ/mol=+183KJ/mol。②NO被CO还原的化学方程式为2NO+2CO催化剂 2CO2+N2;③由于该反应是体系混乱程度减小的吸热反应,体系的自由能大于0,所以设想是不能实现的。① 根据图示可知:用离子方程式表示反应器中发生的反应是:SO2+I2+2H2O=SO
2NO(g)△H=+945KJ/mol+498KJ/mol-2×630KJ/mol=+183KJ/mol。②NO被CO还原的化学方程式为2NO+2CO催化剂 2CO2+N2;③由于该反应是体系混乱程度减小的吸热反应,体系的自由能大于0,所以设想是不能实现的。① 根据图示可知:用离子方程式表示反应器中发生的反应是:SO2+I2+2H2O=SO +2I-+4H+。②2HI(g)
+2I-+4H+。②2HI(g) H2(g)+I2(g). HI分解反应是可能反应。在反应中使用膜反应器分离出H2,减小生成物的浓度,平衡正向移动,有利于反应正向进行。③根据总反应方程式可知:在电池放电时,负极电极反应式为MH+OH--e-=H2O+M。2.5的溶液的酸碱性、热化学方程式与化学键的关系、浓度对平衡移动的影响、离子方程式的书写、镍氢电池的电极反应式的书写的知识。
H2(g)+I2(g). HI分解反应是可能反应。在反应中使用膜反应器分离出H2,减小生成物的浓度,平衡正向移动,有利于反应正向进行。③根据总反应方程式可知:在电池放电时,负极电极反应式为MH+OH--e-=H2O+M。2.5的溶液的酸碱性、热化学方程式与化学键的关系、浓度对平衡移动的影响、离子方程式的书写、镍氢电池的电极反应式的书写的知识。
本题难度:一般