|
高考化学知识点归纳《反应速率与平衡的有关计算》高频考点强化练习(2019年最新版)(六)
2019-06-25 20:49:40
【 大 中 小】
|
1、选择题 在100mL某混合溶液中,c(HNO3)=0.4mol/L,c(H2SO4)=0.1mol/L,向其中加入?1.92g铜粉,微热,充分反应后溶液中c(Cu2+)为
A.0.15mol/L
B.0.3mol/L
C.0.225mol/L
D.无法计算
参考答案:C
本题解析:分析:铜与硝酸反应,与硫酸不反应,硫酸存在的情况下,溶液中发生离子反应3Cu+8H++2NO3-=3Cu2++2NO+3H2O,结合铜、硝酸根、氢离子的物质的量根据离子方程式进行过量计算,再根据不足的物质计算铜离子的物质的量,结合c=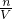 计算铜离子浓度. 计算铜离子浓度.
解答:溶液中的氢离子既包括硝酸电离的又包括硫酸电离的.所以n(H+)=0.4mol/L×0.1L+0.1mol/L×0.1L×2=0.06mol,
n(NO3-)n=0.4mol/L×0.1L=0.04mol.1.92g铜的物质的量为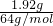 =0.03mol; =0.03mol;
硝酸和铜反应的离子方程式如下:3Cu+8H++2NO3-=3Cu2++2NO+3H2O?
?3Cu~~~~~8H+~~~~2NO3-~~~~3Cu2+.
?3? ?8?2? 3?
0.03mol?0.08mol?0.02mol?
所以氢离子的物质的量不足,根据氢离子的物质的量计算,由离子方程式可知0.06mol氢离子反应,消耗铜的物质的量为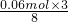 =0.0225mol;所以生成的铜离子的物质的量为0.0225mol. =0.0225mol;所以生成的铜离子的物质的量为0.0225mol.
所以溶液中c(Cu2+)=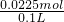 =0.225mol/L. =0.225mol/L.
故选:C.
点评:本题考查混合物的计算,题目难度中等,根据离子方程式判断离子过量是解答本题关键.
本题难度:简单
2、填空题 (12分)在2 L密闭容器中加入1 mol N2和3 mol H2,发生反应:N2+3H2 2NH3 2NH3
(1)该反应是否属于氮的固定??(填“是”或“否”)
(2)充分反应后,?(填“能”或“不能”)得到2 mol NH3?为什么??
(3)下列能判断反应达到平衡状态的是?
A.N2、H2、NH3的浓度不再发生变化
B.N2、H2、NH3的分子数相等
C.单位时间内生成a mol N2,同时生成3a mol H2
D.容器中的压强不再发生变化
| (4)若经5s后,剩下的N2为0. 5 mol,则用H2浓度变化来表示的反应速率是多少?
5s末NH3浓度是多少?
参考答案:(1)是;?(2)不能;因为该反应是可逆反应,反应物不能完全转化为生成物
(3)AD?(4)0. 15 mol・L-1・s-1;0. 5 mol・L-1
本题解析:(1)游离态的氮直接转化为化合态的氮的过程是氮氮固定,所以该反应属于氮的固定。
(2)由于这是1个可逆反应,所以1 mol N2和3 mol H2发生反应,不可能生成2mol氨气。
(3)在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。所以A正确。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此B不正确。选项C中反应速率的方向是相同的,所以不能说明。由于反应前后体积是变化的,所以压强也是变化的。因此当压强不再发生变化时,可以说明反应达到了平衡状态。
(4)? N2+3H2 2NH3 2NH3
起始量(mol)? 1? 3? 0
转化量(mol)? 0.5? 1.5? 1.0
平衡量(mol0?0.5? 1.5? 1.0
所以用H2浓度变化来表示的反应速率是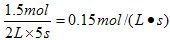
此时氨气的浓度是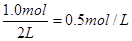
本题难度:一般
3、计算题 (6分)如下图所示,关闭活塞K,向A中充入1molX和1molY,向B中充入2molX和2molY,起始时VA=VB=aL。在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:
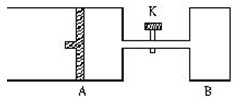
X+Y 2Z+2W+Q;ΔH<0(X、Y、Z、W均为气体),达到平衡时,VA=1.2aL。试回答: 2Z+2W+Q;ΔH<0(X、Y、Z、W均为气体),达到平衡时,VA=1.2aL。试回答:
(1)A中X的转化率αA=________。
(2)A、B中X转化率的关系:αA________αB(填“>”、“=”或“<”)。
(3)打开活塞K,一段时间后又达到平衡时,A的体积为________L(连通管中气体体积不计)。
参考答案:(1)20%? (2)>? (3)2.6a
本题解析:考查可逆反应的有关计算,一般采用三段式。
(1)? X? +? Y 2Z+2W 2Z+2W
起始量(mol)? 1? 1? 0? 0
转化量(mol)? x? x? 2x? 2x
平衡量(mol)? 1-x? 1-x? 2x? 2x
达到平衡时,VA=1.2aL
所以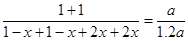
解得x=0.2mol
所以A中X的转化率αA=0.2÷1×100%=20%
(2)根据反应的方程式可知,正反应是体积增大的,因此压强也是增大的。A保持温度和压强,B保持温度和体积不变。因此在反应过程中B中的压强大于A中的压强,由于压强越大,越步利于平衡向正反应方向进行,因此A中的转化率高于B中的转化率。
(3)在温度和压强不变的情况下,打开活塞K,由于X和Y的起始物质的量之比是相等的,因此平衡是等效的,所以最终平衡时容器的体积应该是1.2aL×3=3.6aL,所以A中的体积是3.6aL-aL=2.6aL。
本题难度:一般
4、简答题 某温度下,可逆反应2NO2?
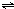
?N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
(1)此混合气体中NO2与N2O4的物质的量之比.
(2)若反应温度与容器容积不变,开始输进的是N2O4气,从逆向反应达平衡时,求N2O4的转化率.
参考答案:(1)混合气体的密度是相同条件下氢气的36倍,所以混合气体的平均相对分子质量为36×2=72,
利用十字交叉法计算NO2与N2O4的物质的量之比:
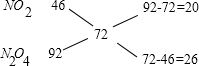
所以n(NO2):n(N2O4)=20:26=10:13,
答:混合气体中NO2与N2O4的物质的量之比为10:13;
(2)与原平衡完全等效,平衡时各组分的物质的量与原平衡相同.
平衡时混合气体中NO2与N2O4的物质的量之比为10:13,令NO2与N2O4的物质的量分别为10mol、13mol.
? ?N2O4
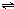
?2NO2?
开始(mol):13+5=18? 0
变化(mol):5? 10-0=10
平衡(mol):13? 10
所以N2O4的转化率为5mol18mol×100%=27.8%,
答:N2O4的转化率为27.8%.
本题解析:
本题难度:一般
5、选择题 一定温度下在一定体积的密闭容器中,下列叙述不能作为可逆反应A(g)+3B(g)  2C(g)达到平衡状态标志的是( )。 2C(g)达到平衡状态标志的是( )。
①C的生成速率与C的消耗速率相等 ②单位时间内生成a mol A,同时生成3a mol B ③A、B、C的浓度不再变化 ④C的物质的量不再变化 ⑤混合气体的总压强不再变化 ⑥混合气体的总物质的量不再变化 ⑦单位时间消耗a mol A,同时生成3a mol B ⑧A、B、C的分子数之比为1∶3∶2
A.②⑧? B.④⑦? C.①③? D.⑤⑥
参考答案:A
本题解析:关于平衡状态的判断,一定要根据实际反应分析选项,判断是否达到平衡状态,只有在平衡状态下具备的性质才能作为“标志”。本题中的反应是一个反应前后气体物质的量不等的可逆反应。②在反应过程中的任意时刻都符合。⑧可能是平衡状态,也可能不是平衡状态。
本题难度:一般
|