1、选择题 下列微粒中一定能促进水电离的是
A.所有离子中,半经(径)最小的离子
B.含1个原子核18电子的阴离子
C.含1个原子核10电子的阳离子
D.含有的电子数与质子数均与Na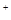 相同,共含有5个原子核的微粒
相同,共含有5个原子核的微粒
参考答案:D
本题解析:促进水电离的措施:(1)升高温度;(2)加入活泼的金属;(3)加入能发生水解的盐;(4)电解某些盐溶液;
A错,所有离子中,半经(径)最小的离子为氢离子,相当于加酸,抑制水的电离;
B错,含1个原子核18电子的阴离子可以是:(1)若氯离子,不影响水电离;(2)若硫离子,则促进水的电离;
C错,含1个原子核10电子的阳离子可以是:(1)钠离子,不影响水电离;(2)铝离子,则促进水的电离;
D正确,Na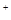 具有11个质子,10个电子;共含有5个原子核的微粒要求具有11个质子,120个电子的为铵根离子,属于弱碱阳离子,能促进水的电离;
具有11个质子,10个电子;共含有5个原子核的微粒要求具有11个质子,120个电子的为铵根离子,属于弱碱阳离子,能促进水的电离;
本题难度:一般
2、选择题 短周期元素X、Y、Z在元素周期表中的位置如下图所示,下列说法正确的是(?)
A.X、Y、Z三种元素中,X的非金属性最强
B.原子半径的大小顺序:Z>Y
C.Y的最高正化合价为+7
D.Y的氢化物的稳定性比Z的弱
参考答案:B
本题解析:根据元素在周期表中的相对位置可知,X是He,Y是F,Z是S。F的非金属性最强,A不正确,B正确;F没有正价,C不正确;氟的非金属性强于S的,则HF的稳定性强于H2S的,D不正确,所以答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般
3、选择题 A元素原子L电子层比B元素原子的L电子层多3个电子,B元素原子核外电子总数比A 元素原子电子总数少5个,则A、B可形成
A.AB? B.A2B? C.B3A2? D.A3B2
参考答案:D
本题解析:略
本题难度:简单
4、填空题 (7分)用“>”、“<”回答下列问题:
①酸性:H3PO4?H2SiO3 ?。H2CO3?H2SiO3
②碱性:Mg(OH)2?Ca(OH)2?Mg(OH)2?Al(OH)3
③气态氢化物稳定性;H2S??H2O? H2O??HCl
④还原性:? H2O ??HCl
??HCl
参考答案:(1)>、>(2)<、>(3)<、>(4)>
本题解析:略
本题难度:一般
5、选择题 砷为第4周期第ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是(?)
A.砷在通常情况下是固体
B.可以存在-3、+3、+5等多种化合价
C.砷的还原性比磷弱
D.As2O5对应水化物的酸性比H3PO4弱
参考答案:C
本题解析:同主族自上而下非金属性逐渐减弱,最高价氧化物的水化物的酸性逐渐减弱,D正确。同主族元素性质和结构是相似的,所以AB都是正确的。非金属性越强,相应阴离子的还原性越弱,所以选项C是错误的。答案选C。
本题难度:简单