1、选择题 在密闭容器中有H2、O2、Cl2的混合气体。电火花点燃,容器中的三种气体恰好完全反应,冷却到室温后得到液体产物的溶质质量分数是33.6%,则容器中原H2、O2、Cl2的体积比是()
A.2∶1∶1
B.9∶4∶1
C.4∶2∶2
D.9∶4∶3
参考答案:B
本题解析:本题主要考查Cl2和非金属的反应及溶质的质量分数的计算方法。
解法一:常规方法。
设原混合气体中分别含O2体积是x,Cl2体积是y。据题意,当产物中HCl气体溶于生成的水中得到盐酸。由阿伏加德罗定律,V1∶V2=n1∶n2。
2H2+O2 2H2O
2H2O
(2x)?x? (2x)
H2+Cl2 2HCl
2HCl
(y)?y? (2y)
33.6%=2y× ×100%,
×100%,
解得x∶y=4∶1由于V(H2)=2x+y,
则V(H2)∶V(O2)∶V(Cl2)=9∶4∶1。
选B。
解法二:挖潜法。
通过反应方程式2H2+O2 2H2O和H2+Cl2
2H2O和H2+Cl2 2HCl,仔细观察题中所溶物质的体积,挖掘出潜在关系:H2的总物质的量等于O2的物质的量的两倍加上Cl2的物质的量。故
2HCl,仔细观察题中所溶物质的体积,挖掘出潜在关系:H2的总物质的量等于O2的物质的量的两倍加上Cl2的物质的量。故
V(H2)=2V(O2)+V(Cl2),分析选项,只有B才能恰好完全反应:9=2×4+1。
本题难度:简单
2、选择题 与标准状况下V L CO2所含氧原子数目相同的水的质量是?
A.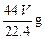
B.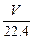 g?
g?
C. g
g
D.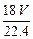 g?
g?
参考答案:C?
本题解析:标准状况下的V L CO2所含氧原子的物质的量为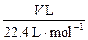 ×2=
×2=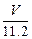 ?mol,含相同氧原子数的H2O的物质的量为
?mol,含相同氧原子数的H2O的物质的量为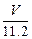 ?mol,其质量为
?mol,其质量为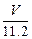 ?mol×18 g・mol-1。
?mol×18 g・mol-1。
本题难度:简单
3、简答题 实验室要配制100mL?0.2mol?L-1?Na2CO3溶液.请回答下列问题.
(1)用托盘天平称取无水碳酸钠固体的质量为______?g.
(2)需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和______.
(3)下列操作中,可能造成所配制溶液的浓度偏低的是______(填序号).
①碳酸钠固体未充分干燥?②称量时左盘放砝码?③转移溶液时有少量滴洒.
参考答案:(1)实验室配制1mol/L的Na2CO3溶液100mL需要Na2CO3的质量为:0.1L×0.2mol/L×106g/mol=2.1g.
故答案为:2.1g.
(2)配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.
所以需要的仪器有托盘天平、药匙、烧杯、玻璃棒、100mL容量瓶、胶头滴管.
所以还需要用的仪器为:托盘天平、药匙、100mL容量瓶.
故答案为:托盘天平、药匙、100mL容量瓶.
(3)①碳酸钠固体未充分干燥,实际称取的碳酸钠的质量偏小,所配溶液的浓度偏低;
②称量时左盘放砝码,由于使用游码,实际称量的碳酸钠的质量为1.9g,称取的碳酸钠的质量偏小,所配溶液的浓度偏低;
③转移溶液时有少量滴洒,移入容量瓶内碳酸钠的物质的量减少,所配溶液的浓度偏低.
故选:①②③.
本题解析:
本题难度:一般
4、填空题 (10分)
(1)标准状况下, CO2 的密度为?(保留两位小数)。?
的密度为?(保留两位小数)。?
(2)标准状况 下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为?。
下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为?。
(3)12.4gNa2X中含Na+ 0.4 mol,则X的相对原子质量为 ?。
(4)在标准状况下,一个装满氯气的容器 的质量为74.6克,若装满氮气则重66克,那么此容器的容积为?。
的质量为74.6克,若装满氮气则重66克,那么此容器的容积为?。
(5)在一定温度和压强下,7g氯气的体积为7.5L,在同样条件下,15L某未知气体的质量8.4 g,该未知气体的相对分子质量为?。
参考答案:(1)1.96g・L-1? 2)44g・mol-1?(3)16(4)4.48L?(5)42.6
本题解析:略
本题难度:一般
5、选择题 下列说法不正确的是
A.磷酸的摩尔质量与6.02×1023个磷酸分子的质量在数值上相等
B.6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14 : 1
C.32g氧气所含的氧原子数目为2×6.02×1023
D.0.5×6.02×1023个一氧化碳分子所占体积是11.2L
参考答案:D
本题解析:A 正确,磷酸的摩尔质量在数值上是1mol磷酸的质量,6.02×1023个磷酸分子的质量也是1mol磷酸的质量,所以,在数值上相等
B 正确,6.02×1023个氮分子和6.02×1023个氢分子的质量比就是1mol氮气和1mol氢气的质量比,等于14 : 1
C 正确,32g氧气为1mol,所含的氧原子数目为2×6.02×1023
D 错误,没有说明标准状况。
本题难度:一般