|
|
|
高考化学试题《原电池原理》试题特训(2019年最新版)(七)
2019-06-25 21:02:45
【 大 中 小】
|
1、选择题 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如下图装置①。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列有关叙述不正确的是
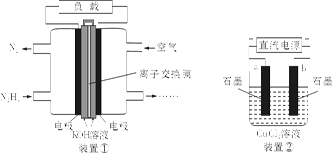
A.该燃料电池负极发生的电极反应为:N2H4+4OH-?4e-==N2↑+4H2O
B.用该燃料电池作为装置②的直流电源,产生7.1g Cl2至少需加入0.5 mol N2H4
C.该燃料电池中,电子从左侧电极经外电路流向右侧电极,溶液OH-迁移到左侧
D.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
|
2、填空题 (1)事实证明,原电池中发生的反应通常是放热反应。利用下列化学反应可以设计成原电池的是 。?
A.C(s)+H2O(g) CO(g)+H2(g) ΔH>0 CO(g)+H2(g) ΔH>0
B.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l) ΔH<0 NaCl(aq)+H2O(l) ΔH<0
C.2H2(g) +O2(g) 2H2O(l) ΔH<0 2H2O(l) ΔH<0
D.CaCO3(s)+2HCl(aq) CaCl2(aq)+H2O(l)+CO2(g) ΔH<0 CaCl2(aq)+H2O(l)+CO2(g) ΔH<0
E.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH<0 CO2(g)+2H2O(l) ΔH<0
(2)有A、B、C、D四种金属,将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等物质的量浓度的盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化,如果把铜浸入C的盐溶液里,有金属C析出。据此判断A、B、C、D的活动性由强到弱的顺序是 。?
3、选择题 下列关于原电池的叙述中,错误的是
A.用导线连接的两种不同金属同时插入液体中,就能形成原电池
B.原电池是将化学能转化为电能的装置
C.在原电池中,电子流出的一极是负极,发生氧化反应
D.在原电池中,电子流入的一极是正极,发生还原反应
4、选择题 如图装置所示,铜片上发生的反应为
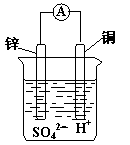
A.Zn2++ 2e一 =Zn
B.2H++2e一= H2 ↑
C.Zn一2e一=Zn2+
D.Cu2++2e一= Cu
5、选择题 X、Y、Z、W四块金属分别用导线两两相连浸入稀硫酸中组成原电池。X、Y相连时,X为负极;Z、W相连时,电流方向是W→Z;X、Z相连时,Z极上产生大量气泡,W、Y相连时,W极发生氧化反应。据此判断四种金属的活动顺序是( )
A.X>Z>W>Y
B.Z>X>Y>W
C.X>Y>Z>W
D.Y>W>Z>X
|