1、选择题 化学反应可视为旧键断裂和新键生成的过程。键能是形成(拆开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供以下键能(kJ・ mol-1): P-P:198,? P-O:360,O-O:498,则化学反应P4(白磷)+3O2=P4O6的反应热△H为 (?)

A.-1638 kJ・mol-1
B.+1638 kJ・mol-1
C.-126 kJ・mol-1
D.+126kJ・mol-1
参考答案:A
本题解析:各化学键键能为P-P?198kJ?mol-1、P-O?360kJ?mol-1、O-O?498?kJ?mol-1,根据反应热△H=反应物总键能-生成物总键能,所以反应P4(白磷)+3O2=P4O6的反应热
△H=6×198kJ?mol-1+3×498kJ?mol-1-12×360kJ?mol-1=-1638kJ?mol-1,所以本题的答案选择A。
点评:本题考查了化学反应中能量的变化,该考点是高考考查的重点和热点,本题要掌握的是反应热△H=反应物总键能-生成物总键能,本题难度不大。
本题难度:一般
2、选择题 在相同条件下,下列物质分别与H2反应,当消耗等物质的量H2时放出热量最多的是
[? ]
A.Cl2
B.Br2
C.I2
D.S
参考答案:A
本题解析:
本题难度:简单
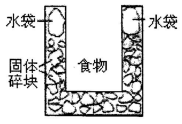
3、选择题 右图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。制造此加热杯可选用的固体碎块是
A.硝酸铵
B.生石灰
C.氯化镁
D.石灰石
参考答案:B
本题解析:水与固体碎块混和,杯内食物温度逐渐上升,这说明和水的混合过程是放热的。则选项B正确,A中是吸热的,C中热量不明显,D中不溶于水,答案选B。
点评:该题是基础性试题的考查,试题贴近生活实际,有利于调到学生的学习兴趣和学习积极性。该题基础性强,旨在考查学生灵活运用基础知识解决实际问题的能力,难度不大,记住常见的热量变化即可。
本题难度:一般
4、选择题 下列说法正确的是( ▲ )
A.任何化学反应都伴随着能量的变化
B.1 mol H2SO4和 1 mol Ba(OH)2完全反应所放出的热量称为中和热
C.在101kPa 时,1 mol 碳燃烧放出的热量就是碳的燃烧热
D.在化学反应中需要加热的反应就是吸热反应
参考答案:A
本题解析:略
本题难度:一般
5、选择题 1mol碳完全燃烧后可放出393.5KJ的热量,下列热化学方程式正确的是:?
A.C(s)+O2(g)=CO2(g);△H =" +393.5" kJ?mol-1
B.C(s)+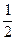 O2(g)=CO(g);△H = -393.5 kJ?mol-1
O2(g)=CO(g);△H = -393.5 kJ?mol-1
C.C+O2=CO2;△H = -393.5 kJ?mol-1
D.C(s)+O2(g)=CO2(g);△H = -393.5 kJ?mol-1
参考答案:D
本题解析:略
本题难度:简单