1、填空题 下表是元素周期表前四周期的一部分,X、Y、Z、R、Q、W、J是7种元素的代号。回答下列问题时,涉及元素书写的请用相应的元素符号。
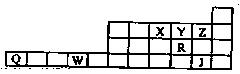
(1)J基态原子的核外电子排布式为?。基态Q2+中未成对电子数为?;R和Y的简单离子与Na+三种离子的半径大小顺序为?。
(2)X、Y、Z三种元素电负性由大到小的排序是?;X与Y的第一电离能:X?Y(填“<”“>”或“=”),其理由是?。
(3)检验某溶液中是否含有Q3+的方法是?。
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为?
?。
(5)化学家直到1971年利用XeZ2(Xe为氙)和含JY―3的溶液反应才制得JY-4。反应中除生成JY-4外,还得到了Xe和一种弱酸。写出该离子反应方程式并标出电子转移方向和数目:?。
2、选择题 如图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B原子的质量数,B原子的原子核内质子数等于中子数。下列叙述正确的是
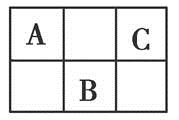
A.最高价氧化物对应水化物的酸性:C>B
B.C单质是氧化性最强的非金属单质
C.A的氢化物中一定只含有极性键
D.B在第三周期ⅦA族
3、选择题 锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性。下列关于锂的判断可能正确的是( )
A.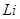 能在空气中燃烧
能在空气中燃烧
B.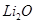 熔点较低
熔点较低
C.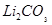 能溶于水
能溶于水
D. 受热易分解
受热易分解
4、选择题 下列物质是化合物的是
A.氯化钠溶液
B.氧气
C.干冰
D.黑火药
5、选择题 关于卤素(F、Cl、Br、I)的化学性质的叙述,错误的是
A.随原子序数逐渐增大,单质跟水的反应能力逐渐减弱
B.随原子序数逐渐增大,单质的氧化性逐渐减弱
C.将氯水加到KI-淀粉溶液中,溶液变蓝
D.随原子序数逐渐增大,氢化物的稳定性逐渐增强