1、选择题 某元素原子的第二层电子数是第一层与第三层电子数之和,该元素属于
A.金属元素
B.非金属元素
C.稀有气体元素
D.不能确定
参考答案:B
本题解析:由原子核外电子排布规律可知第二层电子数为8,第一层为2,可求出第三层电子为6个,核外电子数为16,在原子中核外电子数等于质子数,所以原子的质子数为16,质子数决定元素种类,故该元素为硫元素,为非金属元素.
故选B
考点:原子的定义与构成;元素的简单分类.
点评:本题难度一般,主要考查原子核外电子排布规律及元素种类的判断.考查学生灵活运用所学化学知识分析和解决实际问题的能力.
本题难度:一般
2、选择题 Na2O2、HCl和Al2O3在水中反应,若最后所得溶液中只含AlO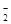 、Na+、Cl-,则Na2O2、HCl和Al2O3的物质的量之可能为(?)
、Na+、Cl-,则Na2O2、HCl和Al2O3的物质的量之可能为(?)
A.4∶6∶1
B.8∶6∶1
C.3∶3∶1
D.4∶6∶3
参考答案:A
本题解析:设Na2O2、HCl和Al2O3的物质的量分别是a、b、c。则有关的反应方程式是2Na2O2+2H2O=4NaOH+O2↑、NaOH+HCl=NaCl+H2O、2NaOH+Al2O3=2NaAlO2+H2O。由于最后所得溶液中只含AlO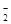 、Na+、Cl-,所以2a=b+2c。根据选项中的数据可知,A是正确的,其余都是不可能的,答案选A。
、Na+、Cl-,所以2a=b+2c。根据选项中的数据可知,A是正确的,其余都是不可能的,答案选A。
点评:该题的关键是根据反应的方程式,得出三种物质的物质的量之间的某种关系,然后借助于数学上的排除法,进行筛选即可。
本题难度:一般
3、选择题 下列反应既属于氧化还原反应,又是吸热反应的是
A.铝片与盐酸反应
B.Ba(OH)2・8H2O与NH4Cl反应
C.灼热的炭与CO2的反应
D.NaOH溶液与CH3COOH溶液反应
参考答案:C
本题解析:考查常见的放热反应和吸热反应。一般金属和水或酸反应,酸碱中和反应,一切燃烧,大多数化合反应和置换反应,缓慢氧化反应 如生锈等是放热反应。大多数分解反应,铵盐和碱反应,碳、氢气或CO作还原剂的反应等是吸热反应。据此可知选项C正确,答案选C。
本题难度:困难
4、实验题 (6分)某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等离子,进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀产生;(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成;(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;(4)另取少量步骤(3)中的滤液,加入NaOH溶液至溶液显碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有?离子,一定不含有 ?离子,还有一种离子不能确定是否存在,要检验这种离子的实验方法是(只填写实验名称和观察到的现象)
?
参考答案:(1)Ag+、 Ba2+、 NH4+?(2)Fe3+
(3)焰色反应?透过蓝色钴玻璃火焰呈紫色
本题解析:氯离子和银离子反应生成白色沉淀,所以根据实验(1)现象判断一定有Ag+;
钡离子和硫酸根离子反应生成白色沉淀,根据实验(2)现象判断一定有Ba2+;
Fe3+与KSCN反应使溶液呈血红色,根据实验(3)现象判断一定没有Fe3+;
铵根离子和碱在加热条件下能反应生成刺激性气味的氨气,根据实验(4)现象判断一定有NH4+
钾离子检验用焰色反应 , 透过蓝色钴玻璃火焰呈紫色。
点评:本题考查常见阳离子的检验,阳离子的检验方法有:常规检验法、焰色反应、特殊检验法;离子检验时,要注意排除其它离子的干扰。
本题难度:一般
5、选择题 向10mL?0.1mol/L的硫酸铜溶液中加入10mL?0.15mol/L的氢氧化钠溶液时,产生一种蓝色沉淀,经测定溶液中的铜离子已几乎被沉淀完全。该沉淀的主要成分是
A.Cu(OH)2
B.3Cu(OH)2・CuSO4
C.Cu2(OH)3
D.Cu2(OH)2SO4
参考答案:B
本题解析:反应生成Cu(OH)20.75mol,剩余CuSo40.25mol,二者物质的量之比为3:1,铜离子全部沉淀,因此选B。如果只认为沉淀只是Cu(OH)2,则剩余的CuSO4中的铜离子就没有沉淀,与题设条件矛盾。
本题难度:一般