1、计算题 1996年诺贝尔化学奖授予对发现C60有重大贡献的三位科学家。C60分子是形如球状的多面体,如右图,该结构的建立基于以下考虑:C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;C60分子只含有五边形和六边形;碳与碳之间既有单键又有双键,每个碳原子仍然满足四个价键饱和;多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2。
请完成下列问题:
(1)一个C60分子中有多少个五边形和多少个六边形?
(2)一个C60分子中有多少个C=C?
(3)已知C70分子的结构模型也遵循C60的那些规律,请确定C70分子结构中上述几项参数。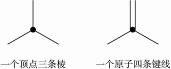
参考答案:(1)一个C60分子中有12个五边形和20个六边形。
(2)一个C60分子中有30个C=C。
(3)C70分子结构中的五边形和六边形的个数分别为12、25,C―C单键数和C=C双键数分别为70、35。
本题解析:(1)设C60分子中含有 个五边形和
个五边形和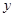 个六边形。?
个六边形。?
先求欧拉定理中棱边数:每个顶点伸出三条棱,而每条棱又总是由两个顶点共有,所以,每个顶点单独伸出的棱有3×1/2=1.5条,60个顶点共伸出的棱为60×1.5=90条。至此,依据欧拉定理可写出: ①
①
为了求出 和
和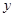 ,还要建立一个方程式。因为五边形和六边形构成多面体时是共用棱边和顶点的,所以,还可以根据棱边数守恒和顶点数守恒写出两个方程式。
,还要建立一个方程式。因为五边形和六边形构成多面体时是共用棱边和顶点的,所以,还可以根据棱边数守恒和顶点数守恒写出两个方程式。
棱边数守恒:每条棱是由两个多面体共用的,所以,一个五边形单独占有的棱边数为5/2=2.5条,一个六边形单独占有的棱边数为6/2=3条,所以,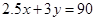 ②
②
至此联立①②可以解得: =12,
=12,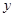 =20。
=20。
(2)首先要明确一个概念:在图中顶点间形成的棱都以单线标出,但有的是表示单键,有的是表示双键。从空间结构来说,每个碳原子连接三条棱,而从化学价键来说,每个碳原子连接四条键线。(一个双键也只是一个键,可以说有两条键线但不能说是两个键)。设一个C60分子中含的C―C单键数和C=C双键数分别为 ,则根据棱边守恒有:
,则根据棱边守恒有: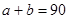 ④
④
再利用键线守恒列一个方程式。每个原子连接四条键线而每条键线被两个原子所共有,所以,每个原子单独占有的键线数为4/2=2,所以,60个碳原子共有键线120条: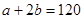 ⑤
⑤
联立④⑤解得: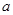 =60,
=60,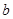 ?=30。即C60中含的双键数为30。
?=30。即C60中含的双键数为30。
(3)设C70分子结构中的五边形和六边形的个数分别为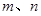 ,设C―C单键数和C=C双键数分别为
,设C―C单键数和C=C双键数分别为 ,则一个C70分子中的棱边总数为70×1.5=105;依据欧拉定理有:
,则一个C70分子中的棱边总数为70×1.5=105;依据欧拉定理有: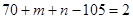 ⑥;依据顶点数守恒有:
⑥;依据顶点数守恒有: ⑦;联立⑥⑦得:
⑦;联立⑥⑦得: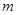 =12,
=12, =25。?
=25。?
根据棱边守恒又写出: =105 ⑧;根据键线守恒有:
=105 ⑧;根据键线守恒有: =70×2=140 ⑨;联立⑧⑨得:
=70×2=140 ⑨;联立⑧⑨得: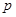 =70,
=70,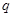 =35。即C70中含的双键数为35。
=35。即C70中含的双键数为35。
本题难度:简单
2、填空题 如图所示的结构为高温超导领域里的一种化合物―钙钛矿晶体结构,该结构是其晶体中具有代表性的最小重复单位。
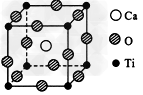
?(1)在该物质的晶体结构中,每个钛离子周围与它 ?最接近且距离相等的钛离子、钙离子各有_____个、?______个。 ?
(2)该晶体结构中,氧、钛、钙的原子个数比是____,该物质的化学式可表示为____。
(3)若钙、钛、氧三元素的相对原子质量分别为a、b、c,晶体结构图中正方体边长(钛原子之间的距离)为d?nm(1?nm=?10-9?m),则该晶体的密度为________g/cm3。
参考答案:(1)6;8?
(2)3:1:1;CaTiO3
(3)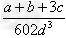
本题解析:
本题难度:一般
3、选择题 下列各组物质中,按熔点由低到高排列正确的是(?)
A.O2、I2、Hg
B.CO2、KCl、SiO2
C.HF、HCl、HI
D.SiO2、NaCl、SO2
参考答案:B
本题解析:A、Hg常温下为液态,所以三者的熔点由低到高排列O2、Hg、I2,错误;B、CO2属于分子晶体,熔点最低,KCl属于离子晶体,熔点低于原子晶体,SiO2属于原子晶体,熔点最高,正确;C、HF分子间存在氢键,熔点最高,错误;D、SiO2属于原子晶体,熔点最高,错误,答案选B。
本题难度:一般
4、选择题 臭氧分子的结构如图,呈V型,三个原子以一个O原子为中心,与另外两个O原子分别构成共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键:三个O原子均等地享用这4个电子。则下列微粒中与O3的结构最相似的是
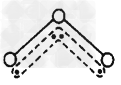
[? ]
A.SO2?
B.C3H6?
C.CO2?
D.CNO-
参考答案:A
本题解析:
本题难度:简单
5、简答题 A、B、C、D、E五种元素中,A原子第三能层轨道上成对电子数等于未成对电子数,B原子核外电子分处3个不同能级,且每个能级上排布的电子数相同,C的价电子排布式为nsnnpn+2,D的核电荷数是A与C的核电荷数之和,E在元素周期表的各元素中电负性最大.请回答下列问题:
(1)A的最高价氧化物的化学式为______,中心原子的VSEPR构型为______.
(2)AC2与BC2分子的立体结构分别是______和______,相同条件下两者在水中的溶解度较大的是______(写分子式),理由是______.
(3)D的元素符号是______,它的价电子排布式为______,在形成化合物时它的最高化合价为______.
(4)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键______.
参考答案:A原子第三能层轨道上成对电子数等于未成对电子数,价电子排布应为3s23p4,应为S元素,B原子核外电子分处3个不同能级,且每个能级上排布的电子数相同,应为1s22s22p2,应为C元素,C的价电子排布式为nsnnpn+2,n应为2,则C应为O元素,D的核电荷数是A与C的核电荷数之和,则原子序数为24,应为Cr元素,E在元素周期表的各元素中电负性最大,应为F元素,
(1)A为S,最高价氧化物为SO3,形成3个δ键,且没有孤电子对,为平面三角形分子,故答案为:SO3;平面三角形;
(2)AC2与BC2分别为SO2和CO2,SO2中形成2个δ键,且有1个孤电子对,为V形,CO2中形成2个δ键,且没有孤电子对,为直线形分子,SO2为极性分子,易溶于水,
故答案为:V形;直线形;SO2;SO2与水都为为极性分子,根据相似相溶的性质可知易溶于水;
(3)D为Cr,它的价电子排布式为3d54s1,价层电子为6,则最高化合价为+6价,故答案为:Cr,3d54s1;+6;
(4)E为F元素,电负性较大,对一个的氢化物含有氢键,水溶液中含有F-H…F、F-H…O、O-H…F、O-H…O等氢键,故答案为:F-H…F、F-H…O、O-H…F、O-H…O.
本题解析:
本题难度:一般