1、填空题 (12分)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示)
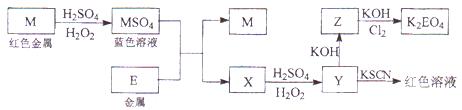
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:?。
(2)某同学取X的溶液,酸化后通入氧气再加入KI、淀粉溶液,变为蓝色,写出与上述变化过程相关的离子方程式:?、?。
(3)写出Cl2将Z氧化为K2EO4的化学方程式:?。
参考答案:

本题解析:略
本题难度:一般
2、填空题 (8分)在加热条件下发生某一化学反应,现对反应体系内的X、Y、Z、Q四种物质是行测定,测得如下数据:
物质
| X
| Y
| Z
| Q
|
反应前质量/g
| 40.0
| 4.6
| 37.8
| 0.0
|
反应后质量/g
| 43.6
| 待测数据
| 12.6
| 3.2
|
请回答下列问题:
(1)上表中“等测数据”的数值是?,此密闭容器中化学反应类型属于?反应(填基本反应类型)。
(2)若X是水,Y是氮的氧化物,且反应式的计量系数比n(X):n(Y):n(Z):n(Q)=2:4:4:1,写出化学反应的方程式:?。
(3)反应结束后,若将反应体系内的Y物质取出,要标准状况下测得其体积小于11.2L,其原因是?。
参考答案:(1)23(2分)分解(2分)
(2)4HNO3===4NO2↑+O2↑+2H2O(2分)
(3)因为2NO2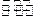 N2O2,存在平衡,有部分NO2转化为N2O4,使NO2体积变小。(2分)
N2O2,存在平衡,有部分NO2转化为N2O4,使NO2体积变小。(2分)
本题解析:略
本题难度:简单
3、推断题 图中的物质均是中学化学中常见的物质,甲、乙 均是离子化合物,且阴、阳离子个数比均为1:1。甲是发酵粉的主要成分,乙是一种常用的化肥。B、D在常温常压下是气体。请回答下列问题
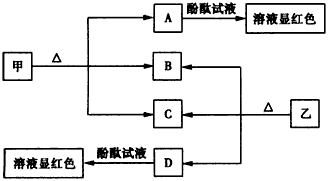
(1)甲的俗名是________。
(2)向A、D物质的水溶液中分别滴入酚酞试液后,溶液均显红色,说明溶液均显________(填“酸”或 “碱”)性,其原理是否相同?____(填“相同” 或“不相同”),请用必要的文字加以解释并写出离 子方程式:_____________________
(3)向饱和氯化钠溶液中通入气体D至饱和后,再通入足量的气体B可制得物质甲,写出该反应的化学方 程式:________________。
参考答案:(1)小苏打
(2)碱;不相同;碳酸钠水解显碱性:CO32-+H2O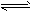 HCO3-+OH-;氨气溶于水生成的NH3・H2O电离显碱性:NH3・H2O
HCO3-+OH-;氨气溶于水生成的NH3・H2O电离显碱性:NH3・H2O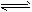 NH4++OH-,所以加入酚酞试液后溶液均显红色
NH4++OH-,所以加入酚酞试液后溶液均显红色
(3)NaCl+CO2+H2O+NH3=NaHCO3↓+NH4Cl
本题解析:
本题难度:一般
4、填空题 现有X、Y、Z、W四种元素,其原子序数依次递增.已知有如下情况:
①X、Y、Z的单质在常温下均为气体.
②X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色.
③XZ极易溶于水,在水溶液中电离出X+和Z-.XZ的水溶液可使石蕊试液变红.
④两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体.
⑤Z的单质溶于X2Y中,所得溶液具有漂白作用.
⑥由Y、Z、W三种元素组成的化合物M受热催化分解,可制得元素Y的单质.
请完成下列问题:
(1)化合物M的化学式为______,1mol M中含有的电子的物质的量为______mol.
(2)用化学方程式表示Z单质的实验室检验方法______.
(3)写出Z的单质溶于X2Y中反应的化学方程式:______,若该反应中有2mol电子发生转移,则参加反应的Z单质在标况下的体积为______L.
参考答案:现有X、Y、Z、W四种元素,其原子序数依次递增,
由①X、Y、Z的单质在常温下均为气体、②X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色、③XZ极易溶于水,在水溶液中电离出X+和Z-.XZ的水溶液可使石蕊试液变红可知,X为H,Z为Cl,
由④两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体,则Y为O,
⑤Z的单质溶于X2Y中,所得溶液具有漂白作用,反应生成HClO具有漂白性,
⑥由Y、Z、W三种元素组成的化合物M受热催化分解,可制得元素Y的单质,则W为K,M为KClO3,
(1)M为KClO3,1molM含电子为1mol×(19+17+8×3)=60mol,故答案为:KClO3;60;?
(2)利用湿润的淀粉KI试纸检验氯气,则Z单质的实验室检验方法为Cl2+2KI=2KCl+I2,故答案为:Cl2+2KI=2KCl+I2;
(3)Z的单质溶于X2Y中反应的化学方程式为Cl2+H2O=HClO+HCl,有2mol电子发生转移,则参加反应的Z单质在标况下的体积为2mol×22.4L/mol=44.8L,
故答案为:Cl2+H2O=HClO+HCl;44.8.
本题解析:
本题难度:一般
5、填空题 (12分)下图是一些常见单质、化合物之间的转化关系图。有些反应中的部分物质及反应条件被略去。A和B组成元素相同,在常温下都是无色液体。D和E的组成元素相同,且E为红棕色的气体。I和K的组成元素相同,I在常温下是无色有毒气体,
J是红棕色固体,G是目前用量最多、用途最广的金属单质。
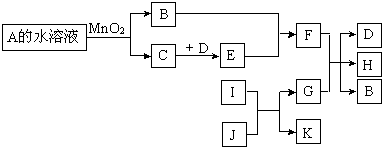
(1)A的化学式是?。
(2)K的电子式是??。
(3)请写出E和B反应的化学方程式?。
(4)请写出G和足量的F稀溶液反应的离子方程式?。
(5)常温下G?(填“能”或“不能”)溶解于浓的F溶液中,原因是?。
参考答案:(1)H2O2?(2)略?(3)3NO2+H2O=2HNO3+NO
(4)Fe+4H++NO3-=Fe3++NO↑+2H2O(5)不能?钝化
本题解析:依题意可知A为H2O2、B为H2O、C为O2、D为NO、E为NO2、F为HNO3、G为Fe、H为Fe(NO3)2或者Fe(NO3)3、I为CO、J为Fe2O3、K为CO2
常温铝铁在浓硝酸和浓硫酸中钝化。
本题难度:一般