1��ѡ���� Ư���ڿ����з�����ʧЧ����Ҫԭ����
A��Ca(ClO)2���ȶ����ֽ�
B��Ca(ClO)2������ˮ�ֶ�����
C��Ca(ClO)2�������е�ˮ��CO2��Ӧ
D��Ca(ClO)2�������е�O2��Ӧ
�ο��𰸣�C
������������������������̼�ᣬ��Ca(ClO)2�������е�ˮ��CO2��Ӧ�����ɴ������̼��ƣ����������ֽ�Ӷ�ʧЧ���ʴ�ΪC��
�����Ѷȣ�һ��
2��ѡ���� ȡ��ˮ�ķ����Թ��У����Ϊ���ֱ�������͡�CCl4���ƾ���NaCl��Һ�����ã�������ȷ����
A��������Һ�ֲ㣬�²���Ϻ�ɫ
B��������Һ�ֲ㣬�²���Ϻ�ɫ
C��������Һ�ֲ㣬�²���ػ�ɫ
D��������Һ���ֲ㣬��Һ���ػ�ɫ��ɻ���ɫ
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
3��ѡ���� ���й����ȵ�˵����ȷ���ǣ� ?��
A��Cl2���к�ǿ�������ԣ��ڻ�ѧ��Ӧ��ֻ����������
B��35 17Cl��37 17ClΪ��ͬ�ĺ��أ��в�ͬ�Ļ�ѧ����
C����ҵ�ϣ����õ�ⱥ��ʳ��ˮ���Cl2
D��1.12LCl2����1.7NA�����ӣ�NA��ʾ����٤��������
�ο��𰸣�C
���������������ClΪ0�ۣ������м�ۣ��������������л�ԭ�ԣ�A����35 17Cl��37 17Cl��������ͬ����������ͬ���Dz�ͬ�ĺ��أ����ǵ�������ͬ����ѧ������ͬ��B����ҵ�ϵ�ⱥ��ʳ��ˮ����������ơ�������������C��ȷ��1.12LCl2���ʵ�����һ����0.05mol��D����
������ͬ��Ԫ�صIJ�ͬ���ػ�ѧ������ȫ��ͬ���������ʿ��ܲ�ͬ��
�����Ѷȣ�һ��
4������� ��6�֣���ˮ�к��ж��ֳɷ֣�������ж�����ʣ�������ˮ�ֱ�����ͼ�������ʷ����ķ�Ӧ��գ�a��b��c��d�غϲ��ִ������ʼ䷴Ӧ������ˮ����������֤����ˮ����Ư���Ե���??(�a������b������c����d��)��C�����е������� ?��b�����е����ӷ���ʽΪ??��a�����еĻ�ѧ����ʽΪ ?��

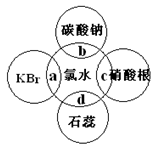
�ο��𰸣�d�� �а�ɫ�������� 2H����CO32����H2O��CO2��2Br����Cl 2��2Cl�� �� Br2
�����������ˮ�е�HClO��ǿ�����ԣ�һ����Ӧ����Ư��ʱ��HClO��ǿ�����Խ���ɫ������������ɫ���ʣ���������ˮ��ʹʯ����Һ�ȱ�죬����ɫ���ʴ�Ϊ��d����ˮ����Cl-������AgNO3��Һ�а�ɫ�������ɣ�����AgCl�������ʴ�Ϊ���а�ɫ�������ɣ���ˮ�к���HCl��HClO���������ԣ���CO32-��Ӧ���ɶ�����̼���壬��Ӧ�����ӷ���ʽΪCO32-+2H+=CO2��+H2O��Cl2��������ˮ����Ҫ�ɷ֣�����ǿ�����ԣ���KBr����������ԭ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ2KBr+Cl2 �T2KCl+Br2���ʴ�Ϊ��CO32-+2H+=CO2��+H2O�� 2KBr+Cl2 �T2KCl+Br2��
���������⿼�����������ʣ���Ŀ�ѶȲ���ע����ˮ�ijɷֺ����ʣ�ע�ػ���֪ʶ�Ļ��ۡ�
�����Ѷȣ�һ��
5��ѡ���� ����a mol FeBr2����Һ�У�ͨ��xmol Cl2�����и���ΪͨCl2�����У���Һ�ڷ�����Ӧ�����ӷ���ʽ�����в���ȷ����
[? ]
A��x��0.4a��2Fe2++Cl2��2Fe3++2Cl-
B��x��0.6a��2Br-+ Cl2��Br2+2Cl-
C��x=a��2Fe2++2Br-+2Cl2��Br2+2Fe3++4Cl-
D��x=1.5a��2Fe2++4Br-+3Cl2��2Br2+2Fe3++6Cl-
�ο��𰸣�B
���������
�����Ѷȣ�һ��