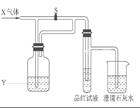
1、选择题 如图是一套检验气体性质的实验装置,向装置中缓慢通入气体X,若关闭活塞S,则品红试液无变化,而澄清石灰水变浑浊;若打开活塞S,则品红试液褪色。据此判断气体X和洗瓶内的液体Y可能是
?
| A
| B
| C
| D
|
X
| Cl2
| SO2
| CO2
| NH3
|
Y
| 饱和NaHSO3溶液
| 饱和NaHCO3溶液
| Na2SO3溶液
| 浓H2SO4
|
?
参考答案:B
本题解析:根据题意气体X能使品红试液褪色,CO2、NH3不能使品红试液褪色,排除C、D;液体Y 能吸收气体X且产生使澄清石灰水变浑浊的气体,排除A;SO2与饱和NaHCO3溶液反应生成CO2,能使澄清石灰水变浑浊,选B.
本题难度:一般
2、选择题 某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O),经测定ClO-与ClO3-的物质的量之比为1:3,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
A.21:5
B.11:3
C.3:1
D.4:1
参考答案:根据ClO-与ClO3-的浓度之比1:3,由Cl到ClO-,失去1个电子,由Cl到ClO3-,失去5个电子,一共失去1+3×5=16个电子;由Cl到Cl-,得到1个电子,需要16个原子才能得到16个电子,所以,被还原的氯元素与被氧化的氯元素的物质的量之比=16:(1+3)=4:1.
故选:D.
本题解析:
本题难度:一般
3、选择题 下列叙述不正确的是
[? ]
A.漂白粉的有效成分是Ca(ClO)2
B.胆矾的成分是CuSO4・5H2O
C.医疗上用的“钡餐”成分是BaSO4
D.光导纤维主要成分是Si
参考答案:D
本题解析:
本题难度:简单
4、选择题 除去氯气中含有的少量水蒸气,所用试剂正确的是
A.固体氢氧化钠
B.生石灰
C.浓盐酸
D.浓硫酸
参考答案:D
本题解析:碱性干燥剂不能选用,会跟Cl2发生反应.浓盐酸无吸收性,只有浓硫酸可吸水又不与Cl2反应,故D对.
本题难度:简单
5、计算题 把6.1g干燥纯净的氯酸钾和二氧化锰的混合物放在试管里加热,当完全分解、冷却后称得剩余固体质量为4.2g,求原混合物里氯酸钾有多少克?
参考答案:4.8g
本题解析:根据质量守恒定律,混合物加热后减轻的质量即为生成的氧气质量(W混-W剩=WO2),
本题难度:简单