1、填空题 (4分)写出(1)乙炔的电子式:?;(2)聚氯乙烯的结构 简式:?
简式:?
(3)苯和液溴反应生成溴苯的化学方程式:?
参考答案:(4分,(,1)(2)各1分)
(1)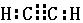 ?(2)?
?(2)?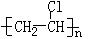 (3)
(3)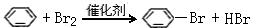
本题解析:略
本题难度:一般
2、选择题 下列工业生产的主要反应原理不涉及氧化还原反应的是
A.硝酸工业
B.接触法制硫酸
C.合成氨工业
D.氨碱法制纯碱
参考答案:D
本题解析:A、硝酸工业是利用氨气的催化氧化生成一氧化氮,一氧化氮被氧气氧化为二氧化氮,二氧化氮和水发生氧化还原反应生成硝酸,因此过程中的反应都是氧化还原反应,故A不符合题意;B、接触法制硫酸是利用黄铁矿燃烧生成二氧化硫,二氧化硫催化氧化生成三氧化硫,三氧化硫溶于水生成硫酸;前两步都是氧化还原反应,故B不符合题意;C、合成氨工业是利用分离空气得到的氮气和水煤气中生成的氢气的反应是氧化还原反应。氢气和氮气发生氧化还原反应生成氨气,故C不符合题意;D、氨碱法制纯碱,是向氨化的饱和食盐水中通入二氧化碳反应生成碳酸氢钠;反应过程中无元素化合价变化,不是氧化还原反应,故D符合,答案选D。
本题难度:一般
3、选择题 将1.92g铜粉与一定量浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况),则所消耗硝酸物质的量是( )
A.0.12mol
B.0.11mol
C.0.09mol
D.0.08mol
参考答案:B
本题解析:
本题难度:简单
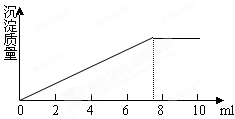
4、选择题 在5ml0.05mol/L的某金属氯化物的溶液中,滴加
0.1mol/LAgNO3溶液,生成沉淀的质量与加入AgNO3溶液的体积关系如图所示,则该氯化物中金属元素的化合价为
A.+1
B.+2
C.+3
D.+4
参考答案:C
本题解析:
分析:根据氯离子和银离子之间反应生成氯化银沉淀的实质以及氯化物的化学式进行计算.
解答:解:氯化物种的Cl-和Ag+1:1反应,因此消耗掉的硝酸银的物质的量为这些溶液中Cl-离子的物质的量,n(Cl-)=n(Ag+)=7.5×10-3L×0.1mol/L=7.5×10-4mol.
设该金属的化合价为X其化学式为A(Cl)x,n(Ax+)=5×10-3L×0.05mol/L=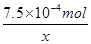 ,解得x=3.
,解得x=3.
故选C.
点评:本题考查学生分析和解决问题的能力,是一道有关离子反应的计算题,难度不大.
本题难度:简单
5、选择题 等物质的量的下列烃完全燃烧,消耗氧气最多的是( )
A.CH4
B.C5H12
C.C3H8
D.C2H6
参考答案:B
本题解析:
本题难度:一般