1、选择题 下列表述中正确的是
[? ]
A.任何能使熵值增大的过程都能自发进行
B.增大反应物的量,一定会加快正反应速率,使平衡向正反应方向进行
C.化学平衡发生移动,平衡常数不一定发生变化
D.反应物的转化率减少,平衡一定向逆反应方向移动
2、填空题 在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内分压与反应温度的关系如下图所示(已知气体的分压之比等于物质的量之比)。
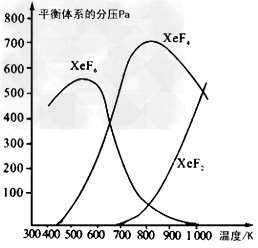
(1)420K时,发生反应的化学方程式为_______________________。若反应中消耗1?mol Xe,则转移电子_______mol。
(2)600K~800K时,会发生反应:XeF6(g) XeF4(g)+?F2(g),其反应热△H ____(填“>”“=”或“<”)0。理由是______________________。
XeF4(g)+?F2(g),其反应热△H ____(填“>”“=”或“<”)0。理由是______________________。
(3)900K时,容器中存在的组分有__________。
3、选择题 下图是温度和压强对X+Y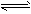 2Z反应影响的示意图。 图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。 图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
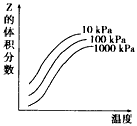
[? ]
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中只有一种为气态,Z为气态
D.上述反应的逆反应的△H>0
4、填空题 为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。
已知:
2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ・moL-1
2H2(g)+O2(g)=2H2O(g);ΔH=-483.6KJ・moL-1
H2O (g)=H2O(l);ΔH=-44.0KJ・moL-1
(1)氢气的燃烧热△H=__________kJ・moL-1
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式__________________________
(3)往1L体积不变的容器中加入1.00mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为__________;反应达到平衡后,升高温度,此时平衡常数将
__________(填“变大”、“不变”或“变小”),平衡将向__________(填“正”或“逆”)方向移动
(4)为了提高CO的转化率,可采取的措施是__________。
A.增大的CO浓度 B.增大的H2O(g)浓度 C.使用催化剂 D.降低温度
(5)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是____________________
5、选择题 如图是关于反应A2(g)+3B2(g)?2C(g)△H<0的平衡移动图形,影响平衡移动的原因是( )
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用催化剂
