1������� ��1�������ʵ�����SO2��SO3���ߵ�����֮��Ϊ______��������ԭ����֮��Ϊ______��
��2���ڱ�״���£�CO��CO2������������Ϊ36g�����Ϊ______��������CO2��ռ�����Ϊ 11.2L��CO��ռ������Ϊ______��
�ο��𰸣���1�������ʵ�����Ϊn�������ʵ�����SO2��SO3���ߵ�����֮��Ϊn��64g/mol��n��80g/mol=4��5����ԭ�Ӹ���֮�ȵ������ʵ���֮�ȣ�Ϊn��2��n��3=2��3��
�ʴ�Ϊ��4��5��2��3��
��2����״���£�CO��CO2������������Ϊ36g��CO2��ռ�����Ϊ 11.2L�������ʵ���Ϊ11.2L22.4L/mol=0.5mol��
����COΪxmol������x��28g/mol+0.5mol��44g/mol=36g�����x=0.5mol��
���������Ϊ0.5mol+0.5mol-1mol������µ����Ϊ1mol��22.4L/mol=22.4L��
CO������Ϊ0.5mol��28g/mol=14g��
�ʴ�Ϊ��2.24L��14g��
���������
�����Ѷȣ�һ��
2��ѡ���� 448 mL ij�����ڱ�״���µ�����Ϊ1.28 g���������Ħ������ԼΪ
A��64 g
B��64
C��64 g/mol
D��32 g/mol
�ο��𰸣�C
�������������£�448mlΪ0.02mol��M===64g/mol����ѡC��
�����Ѷȣ���
3��ѡ���� ��NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A����״���£�5.6L NO��5.6L O2��Ϻ�ķ�������Ϊ0.5NA
B��1mol Na2O2�����к���������Ϊ4NA
C��7.1gCl2������NaOH��Һ��Ӧת�Ƶĵ�����Ϊ0.2NA
D���ڱ�״���£�22.4LCH4��18gH2O�����еĵ�������Ϊ10NA
�ο��𰸣�D
���������
��ȷ�𰸣�D
A.����ȷ��2NO��O2=2NO2? 2NO2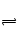 N2O4��Ϻ�ķ�����������0.5NA
N2O4��Ϻ�ķ�����������0.5NA
B.����ȷ��1mol Na2O2�����к����ӣ�Na��? O22�D������Ϊ3NA
C.����ȷ��Cl2��2NaOH=NaCl��NaClO��H2O,7.1gCl2������NaOH��Һ��Ӧת�Ƶĵ�����Ϊ0.1NA
�����Ѷȣ�һ��
4��ѡ���� ��֪�з�Ӧ2NO��O2��2NO2���������ΪVL���ܱ�������ͨ��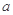 molNO��
molNO��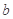 molO2����Ӧ�������еĵ�ԭ�Ӻ���ԭ�ӵ�ԭ�Ӹ���֮����(? )
molO2����Ӧ�������еĵ�ԭ�Ӻ���ԭ�ӵ�ԭ�Ӹ���֮����(? )
A��a/b
B��a/2b
C��a/��a��2b��
D��a/��2a��2b��
�ο��𰸣�C
�������������ԭ���غ��֪�������еĵ�ԭ�Ӻ���ԭ�ӵ�ԭ�Ӹ���֮����a/(a��2b)����ѡC��
�����Ѷȣ�һ��
5��ѡ���� ���������ʵ���Ũ����Һ��ʵ���У�����ý�ͷ�ιܶ��ݺ�Һ����ȷ���ǣ�������
A��

B��

C��
D��

�ο��𰸣�B
���������
�����Ѷȣ�һ��