1��ѡ���� ���й���������˵���У���ȷ���ǣ�?��
A����һ����ɫ��ζ������
B������ˮ�γ�Һ��
C����ˮ��Ӧ����������
D����ҵ���ɶ������̺�Ũ���ᷴӦ����������
�ο��𰸣�C
���������������һ�ֻ���ɫ���壬����ˮ���γ���ˮ��������ˮ��Ӧ��������ʹ����ᣬʵ�����ö������̺�Ũ��������ȡ����������C����ȷ����ѡC��
����������ܼ�������Ҫ���������Ļ������ʡ�
�����Ѷȣ���
2��ѡ���� ���е����У����������ǿ����Һ���ܷų���������
A��Cu
B��Fe
C��Al
D��Si
�ο��𰸣�C
���������
�𰸣�C
C���������ԣ�2Al��6H��=2Al3����3H2��,2Al��2OH�D��2H2O=2AlO2�D��3H2��;
A���ᡢ�������Ӧ��Bֻ����Dֻ������H2
�����Ѷȣ���
3������� ��ˮ���ʾ��ж����ԣ���ָ�����и�������Ҫ�Ǻ����������ֳ��������ʣ�
��1����ˮ��dz����ɫ______���û�ѧʽ�����ӷ�����д����ͬ����
��2��ʹʪ�����ɫʯ����ֽ�ȱ�����ɫ______��
��3���μ�AgNO3��Һ�����ɰ�ɫ����______��
��4������ʯ��ʯ��ĩ���ܽ⣬���ų�����______��
��5��������Fe2+��Һ�еμ�KSCN��Һ�����������ٵμ���ˮ��ʺ�ɫ______��
�ο��𰸣���1�������ǻ���ɫ���壬��ˮ�д��ڻ�ѧƽ�⣬CL2+H2O=HCl+HClO����Һ�д����������ӳʻ���ɫ���ʴ�Ϊ��Cl2��
��2����ˮ�д��ڻ�ѧƽ�⣬CL2+H2O=HCl+HClO��ʹʪ�����ɫʯ����ֽ�ȱ����ƽ��״̬�����������������ӵ����ã������ɫ�Ǵ������Ư�����ã��ʴ�Ϊ��H+��HClO��
��3���μ�AgNO3��Һ�����ɰ�ɫ���������������������Ӻ������ӷ�Ӧ�����Ȼ���������Ag++Cl-=AgCl�����ʴ�Ϊ��Cl-��
��4������ʯ��ʯ��ĩ���ܽ⣬���ų������������̼��Ʒ�Ӧ���ɶ�����̼���壬CaCO3+2H+=Ca2++CO2��+H2O���ʴ�Ϊ��H+��
��5��������Fe2+��Һ�еμ�KSCN��Һ�����������ٵμ���ˮ��ʺ�ɫ������Ϊ�������������ӷ�Ӧ���������ӵķ�Ӧ2Fe2++Cl2=2Fe3++2Cl-���ʴ�Ϊ��Cl2��
���������
�����Ѷȣ�һ��
4��ѡ���� ���и����������ͬһ����װ����ȡ����
A��Cl2��O2
B��H2��O2
C��H2��CO2
D��Cl2��HCl
�ο��𰸣�CD
���������Cl2��HCl���Ϲ�+Һ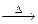 ����ģʽ��H2��CO2���Ϲ�+Һ
����ģʽ��H2��CO2���Ϲ�+Һ ����O2Ϊ��
����O2Ϊ��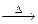 ��,����C��D����ȷ��
��,����C��D����ȷ��
�����Ѷȣ���
5��ʵ���� ��16�֣�ij����С����MnO2��Ũ�����Ʊ�Cl2ʱ�����ø����չ�����SO2��NaOH��Һ����β ���������մ�����
���������մ�����
��1����д��MnO2��Ũ�����Ʊ�Cl2�����ӷ���ʽ________________��
��2����ӦCl2+Na2SO3+2 NaOH===2NaCl+Na2SO 4+H2O�еĻ�ԭ��Ϊ_______________
4+H2O�еĻ�ԭ��Ϊ_______________ _��
_��
��3������β��һ��ʱ�������Һ��ǿ���ԣ��п϶�����Cl ��OH
��OH ��SO
��SO �������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
�������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
��?����������裮
����1��ֻ����SO32-������2���Ȳ�����SO3 2-Ҳ������ClO
2-Ҳ������ClO ��
��
����3��_____________������4��?
��?���ʵ�鷽��������ʵ�顣���ڴ����д��ʵ�鲽���Լ�Ԥ������ͽ��ۡ���ѡʵ���Լ���3moL L-1H2SO4��1moL
L-1H2SO4��1moL L-1NaOH��0.01mol
L-1NaOH��0.01mol L-1KMnO4������-KI��Һ����ɫʯ����Һ��
L-1KMnO4������-KI��Һ����ɫʯ����Һ��