1、填空题 在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内分压与反应温度的关系如下图所示(已知气体的分压之比等于物质的量之比)。
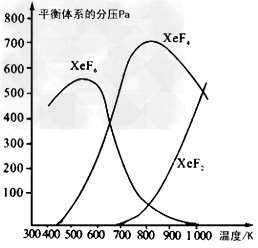
(1)420K时,发生反应的化学方程式为_______________________。若反应中消耗1?mol Xe,则转移电子_______mol。
(2)600K~800K时,会发生反应:XeF6(g) XeF4(g)+?F2(g),其反应热△H ____(填“>”“=”或“<”)0。理由是______________________。
XeF4(g)+?F2(g),其反应热△H ____(填“>”“=”或“<”)0。理由是______________________。
(3)900K时,容器中存在的组分有__________。
2、选择题 某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是
物质
| X
| Y
| Z
| W
|
初始浓度/mol・L-1
| 0.5
| 0.6
| 0
| 0
|
平衡浓度/mol・L-1
| 0.1
| 0.1
| 0.4
| 0.6
|
?
A.反应达到平衡时,X的转化率为80%?
B.该反应的平衡常数表达式为K=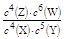
C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动
D.改变温度可以改变此反应的平衡常数
3、选择题 在密闭容器中达到平衡的化学反应N2O4(g)  2NO2(g) △H>0,改变条件,下列说法不正确的是?
2NO2(g) △H>0,改变条件,下列说法不正确的是?
[? ]
A.温度不变体积减小,反应速率增大,再次平衡时混合气颜色变浅
B.温度和体积不变,加入少许NO2,再次平衡时混合气中NO2的百分含量减少
C.体积不变时加入少许N2O4,再度平衡时颜色变深
D.体积不变时升高温度,再次平衡时混合气颜色变深
4、选择题 室温下浓度为0.1 mol / L的三种一元碱溶液:AOH、BOH、COH,其中AOH中的c(OH―)=0.01 mol / L,BOH的电离度为1%,COH的c(H+)=1×10-13mol / L,则室温下三种碱所形成的氯化物:ACl、BCl、CCl的溶液在物质的量浓度相同的情况下,其pH由大到小的顺序是?
A.ACl>BCl>CCl
B.CCl>ACl>BCl
C.CCl>BCl>ACl
D.BCl>ACl>CCl
5、选择题 可逆反应aA(g)+bB(s)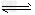 cC(g)+dD(g).在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是
cC(g)+dD(g).在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是

[? ]
A.温度降低,化学平衡向逆反应方向移动?
B.使用催化剂,C的物质的量分数增加
C.化学方程式系数a<c+d
D.无法根据图像确定改变温度后化学平衡移动方向