1、推断题 A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如下反应关系
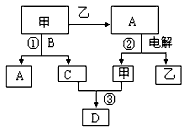
(1)上述转化过程中包含的反应类型为____________。
a.置换反应 b.化合反应 c.分解反应 d.复分解反应
(2)乙在甲中燃烧,当有1 mol e-转移,生成液态A时,放出 142.9 kJ的热量,写出该反应的热化学方程式:_____________________。
(3)反应③在一定条件下为可逆反应,经过一段时间该反应达到平衡,写出该反应的化学方程式:
____________________。若将3 mol甲和4 mol C混合充入容积为2 L的密闭容器中,2分钟后,达到平衡。平衡后混合气总物质的量为6 mol,甲的化学反应速率为____________。将该平衡混和物缓慢通入水中得到1L溶液,所得溶液物质的量浓度是____________。
参考答案:(1)bc
(2)H2(g) + 1/2O2(g) = H2O(l) △H=-285.8 kJ/mol
(3)2NO + O2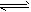 2NO2;0.25 mol/(L・min);4mol/L
2NO2;0.25 mol/(L・min);4mol/L
本题解析:
本题难度:一般
2、简答题 下面图表示制备无水盐E的主要步骤:
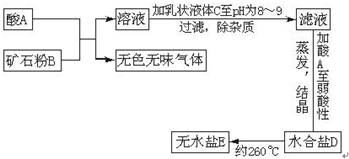
已知B是石灰石,D盐含有约49%的结晶水,无水盐E可用作干燥剂.取少量E溶于水,向其中滴加硝酸后,再滴加硝酸银溶液,有白色沉淀F生成.
填写以下空白(写出化学式或名称):
A______,C______,D______,E______,F______.
参考答案:这是一例典型的定性分析和定量分析相结合的推断题.
(一)定性分析:因为B是石灰石,和酸A反应,放出的无色无味气体应是CO2,生成可溶性钙盐,由此判定最终形成的无水盐E也是钙盐溶液,因为E溶于水后向其中滴加硝酸后,再滴加硝酸银溶液,有白色沉淀F生成,知F是AgCl,E是CaCl2,吻合了E可作干燥剂这条件,D是CaCl2的结晶水合物.
(二)定量分析:设无水盐为CaCl2?xH2O
? CaCl2?xH2O~xH2O
101+18x?18x ?
100?49
解之:x=6
则D盐化学式 CaCl2?6H2O酸A是盐酸,乳状液体C应是石灰乳,
故答案为:HCl(盐酸);Ca(OH)2(石灰乳);CaCl2?6H2O;CaCl2;AgCl.
本题解析:
本题难度:一般
3、填空题 主族元素A、B、C、D都是短周期元素,A、D同主族,B、C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体。它们在一定条 件下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能剧烈反应生成A的单质。所得溶液中含有与氖原子的电子层结构相同的阳离子。
件下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能剧烈反应生成A的单质。所得溶液中含有与氖原子的电子层结构相同的阳离子。
回答下列问题:(1)写出元素符号A____,B____,C____,D____。
(2)写出B单质与D在加热反应后生成物质的化学式___________ ___________。
___________。
参考答案:(1)H, O,C,Na(2分)?(2) Na2O2(2分)
本题解析:略
本题难度:一般
4、简答题 如图各物质是中学化学中常见的物质,甲和A的焰色反应为黄色,常温常压下B为无色无味气体,丁可使带火星的木条复燃.请回答下列问题:
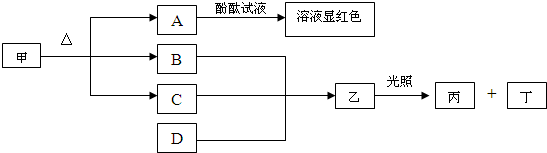
(1)写出B的电子式______.
(2)工业上生产D采用石灰乳与某种气体反应.D常用作______剂
(3)写出由A变甲的化学方程式______.
(4)B与甲烷在一定条件下生成氢气和CO的化学方程式______.
参考答案:丁可使带火星的木条复燃,应为O2,结合乙在光照条件下分解的性质可知乙为HClO,丙为HCl,甲和A的焰色反应为黄色,说明都含有Na元素,且A的水溶液呈碱性,可说明甲为NaHCO3,A为Na2CO3,则B为CO2,C为H2O,工业上生产D采用石灰乳与某种气体反应,结合题给转化关系可知D应为Ca(ClO)2,
(1)由以上分析可知B为CO2,电子式为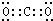 ,故答案为:
,故答案为: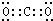 ;
;
(2)D为Ca(ClO)2,具有氧化性,可与酸反应生成具有漂白性的次氯酸,常用于漂白或消毒,
故答案为:漂白或消毒;
(3)Na2CO3可与CO2和水反应生成NaHCO3,反应的方程式为CO2+Na2CO3+H2O=2NaHCO3,
故答案为:CO2+Na2CO3+H2O=2NaHCO3;
(4)CO2与甲烷在一定条件下生成氢气和CO,二者发生氧化还原反应,反应的方程式为CO2+CH4=2CO+2H2,
故答案为:CO2+CH4=2CO+2H2.
本题解析:
本题难度:一般
5、简答题 A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素.
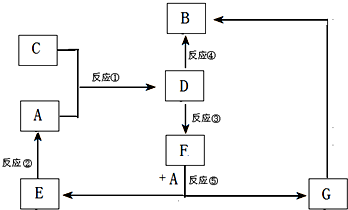
已知:(Ⅰ)A为金属单质;?B为红褐色固体;E为密度最小的气体;G为浅绿色溶液.
(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物.
请回答下列问题:
(1)上述反应中属于置换反应的是?(填序号).
(2)G生成B有多种途径.若在G的溶液中加入与G等物质的量的Na2O2,恰好使G转化为B,写出该反应的离子方程式:?
反应③(即D将某种氧化物氧化为F)的离子方程式?
(3)D的水溶液显酸性,请用离子方程式解释原因?
(4)实验室制取C的化学方程式为?
对气体C进行如下实验.已知整个反应过程中,每消耗0.1mol?KI,转移的电子数约为3.612×1023个.请按照要求填空:
| 实验步骤 | 实验现象 | 用化学用语解释
将少量气体通入淀粉KI溶液
溶液最初变成?色
?
(用离子方程式表示)
继续通入气体
溶液逐渐变成无色
?
(用化学方程式表示)
参考答案:
本题解析:
本题难度:一般
|