1、选择题 25℃时,向10mL?0.01mol/L?KOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的是( ? )
A.pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-)
B.pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-)
C.V[C6H5OH(aq)]=10mL时,c(K+)=c(C6H5O-)>c(OH-)=c(H+)
D.V[C6H5OH(aq)]=20mL时,c(C6H5O-)+c(C6H5OH)=2c(K+)
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列溶液中微粒的物质的量浓度关系一定正确的是
[? ]
A.某二元弱酸的酸式盐NaHA溶液中:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
B.0.2 mol/L NH4Cl溶液和0.1 mol/L NaOH溶液等体积混合:c( NH4+)>c(Cl-)>c(Na+)>c(OH-) >c(H+)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+)
D.25℃时,pH=8的CH3COONa稀溶液中:c(CH3COOH) =9.9×10-7mol/L
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列关系的表述中,正确的是
[? ]
A.0.1mol/LNaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)
B.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1:1
C.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)不相等
D.0.1mol/LNaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
参考答案:C
本题解析:
本题难度:一般
4、选择题 向三份0.1mol/L醋酸钠溶液中分别加入少量硝酸铵、亚硫酸钠、氯化铁固体(忽略溶液体积变化),则CH3COO-浓度的变化依次是( )
A.增大、减小、减小
B.增大、减小、增大
C.减小、增大、增大
D.减小、增大、减小
参考答案:醋酸钠是强碱弱酸盐其水溶液呈碱性,硝酸铵是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加硝酸铵会促进醋酸根离子水解,导致醋酸根离子浓度减小;
亚硫酸钠是强碱弱酸盐其水溶液呈碱性,所以向醋酸钠溶液中加亚硫酸钠会抑制醋酸根离子的水解,导致醋酸根离子浓度增大;
氯化铁是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加氯化铁会促进醋酸根离子水解,导致醋酸根离子浓度减小,
故选D.
本题解析:
本题难度:简单
5、选择题 温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、⑤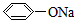 、
、
⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
[? ]
A. ③①④②⑥⑤
B. ①③⑥④②⑤
C. ③②①⑥④⑤
D. ⑤⑥②④①③
参考答案:A
本题解析:
本题难度:一般