1、填空题 稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解。
(1)无水CeCl3可用加热CeCl3・6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是______________。
(2)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:?
___Ce3++?___H2O2+?___H2O?→?___Ce(OH)4↓+?______
(3)在溶液中,反应A+2B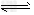 C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为
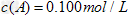 、
、 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。
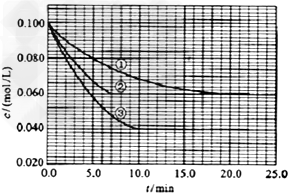
请回答下列问题:
与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②______________;③_______________;?实验②平衡时B的转化率为_________;实验③平衡时C的浓度为____________;该反应是________热反应,判断其理由是____________________________;该反应进行到4.0min时的平均反应速度率:实验②: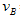 =__________________________________;
=__________________________________;
参考答案:(1)分解出HCl气体,抑制CeCl3的水解
(2)2Ce3++H2O2+6H2O→ 2Ce(OH)4↓+6H+?
(3 )②加催化剂,达到平衡的时间缩短,平衡时A的浓度未变;③温度升高,达到平衡的时间缩短,平衡时A的浓度减小;40%(或0.4);0.06mol/L; 吸热;升高温度平衡向正反应方向移动,故该反应是吸热反应;0.014mol(L・min)-1
本题解析:
本题难度:一般
2、选择题 已知常温下反应①、②、③的平衡常数关系为K1> K3> K2,据此所做以下推测合理的是
①NH3+H+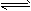 NH4+ (平衡常数为K1)②Ag++Cl-
NH4+ (平衡常数为K1)②Ag++Cl-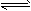 AgCl(平衡常数为K2)
AgCl(平衡常数为K2)
③Ag++2NH3 Ag(NH3)2+(平衡常数为K3)
Ag(NH3)2+(平衡常数为K3)
[? ]
A.氯化银可溶于氨水
B.银氨溶液中加入少量氯化钠有白色沉淀
C.银氨溶液中加入盐酸无明显现象
D.银氨溶液可在酸性条件下稳定存在
参考答案:A
本题解析:
本题难度:一般
3、填空题 工业生产中产生的含SO2废气经石灰吸收和氧化后制成硫酸钙,硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、水泥等,以下是工业利用硫酸钙的部分流程
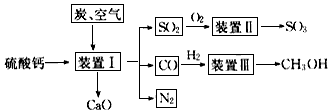
(1)生产中常在装置I里加入SiO2,其主要作用:①生产水泥;②还可___________________。
(2)装置Ⅱ中,为了提高SO2的转化率,可采用的措施是__________。
A.加入V2O5作催化剂
B.采用过量SO2
C.低温
D.通入过量空气
(3)装置Ⅲ中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO)。已知:
2CO(g)+O2(g)=2CO2(g) △H =-566 kJ/mol
2H2O(g)=2H2(g)+O2(g) △H =+484 kJ/mol
CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol
试写出CO与H2在一定条件下反应生成CH3OH(g)的热化学方程式________________________;若将生成的CH3OH与氢氧化钾溶液、氧气构成燃料电池,则燃料电池的负极反应式为___________。
(4)已知25℃时,Ksp(CaSO4)=7.10×10-5,在0.100 L 0.200 mol/L CaCl2溶液中加入2. 72 g CaSO4粉末充分搅拌后,假设溶液的体积变化忽略不计,则溶液中SO42-物质的量浓度为_______mol/L。
参考答案:(1)降低反应所需温度或降低能耗
(2)D
(3)CO(g)+2H2(g)=CH3OH(g) △H=-90.1 kJ/mol;CH3OH+8OH--6e-=CO32-+6H2O
(4)3. 55×10-4
本题解析:
本题难度:一般
4、选择题 现有3个体积相等的密闭容器,都进行下列反应:CO2(g)+H2(g)?H2O(g)+CO(g),反应所处的温度相同,但起始浓度不同,其中甲:n(CO2)=n(H2)=1mol;乙:n(CO2)=1mol,n(H2)=2mol;丙:n(CO2)=n(H2)=1mol,n[H2,O(g)]=1mol.达到平衡时CO的物质的量由大到小的顺序是( )
A.乙>甲>丙
B.甲>丙>乙
C.乙>丙>甲
D.甲>乙>丙
参考答案:对于乙到达平衡状态,可以等效为在甲到达平衡的基础上再加入1mol氢气,平衡向正反应移动,二氧化碳的转化率增大,平衡时乙中CO的物质的量比甲中CO的物质的量大,
对于丙到达平衡状态,可以等效为在甲到达平衡的基础上再加入1molH2O(g),平衡向逆反应移动,二氧化碳的转化率降低,平衡时丙中CO的物质的量比甲中CO的物质的量小,
即平衡时CO的物质的量乙>甲>丙,
故选A.
本题解析:
本题难度:一般
5、选择题 可逆反应:2HI(g)?H2(g)+I2(g);△H>0.在密闭容器中进行,当达到平衡时欲使混合气体的颜色加深,应采取的措施( )
A.减小容器体积
B.降低温度
C.加入催化剂
D.充入H2气体
参考答案:A.减小容器的体积,碘蒸气浓度增大,则混合气体颜色加深,故A选;
B.降低温度,平衡向逆反应方向移动,碘蒸气浓度减小,则混合气体颜色变浅,故B不选;
C.加入催化剂对平衡无影响,则碘蒸气浓度不改变,所以混合气体颜色不变,故C不选;
D.充入氢气,平衡向逆反应方向移动,碘蒸气浓度减小,则混合气体颜色变浅,故D不选;
故选A.
本题解析:
本题难度:一般