1、实验题 某同学欲探究食品添加剂铵明矾NH4Al(SO4)2・12H2O高温分解的情况。
(1)预测产物:下列关于气体产物的预测不合理的是?。
A.NH3、N2、SO2、H2O? B.NH3、SO3、H2O
C.NH3、SO2、H2O? D.NH3、N2、SO3、SO2、H2O
(2)定性检验:取一定量铵明矾,设计下列实验探究产物。
①按图示组装仪器后,首先检查整套装置的气密性,操作是?。
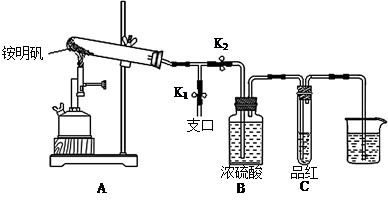
②夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是?;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是?(任填一种物质的化学式)。
③分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式?。
④为了防止倒吸,实验结束时必须先?(填字母序号),然后熄灭酒精喷灯。
A.取出烧杯中的导管? B.打开止水夹K1? C.关闭止水夹K2
(3)分析和结论:实验证明气体产物是(1)D中的5种气体。相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=?。
参考答案:(1)C(2分)
(2)①关闭支口开关K1并打开K2(1分),将最后的导管通入水中,微热大试管(1分),若看到从导管中出现气泡(1分),且停止加热后在导管中上升一段水柱,(1分)则证明气密性好。(共4分)
②打开K1,用蘸有浓盐酸的玻璃棒靠近支口,若出现白烟(或者不加试剂看到白烟也给分)(2分)(用润湿的紫色石蕊试纸检验不得分);(NH4)2SO4或者(NH4)2SO3或者SO3(酸式盐及以上物质的混合物也给分)(2分)
③Al2O3 +2OH-=2AlO2-+H2O或Al2O3 +3H2O +2OH-=2Al(OH)4-(2分,配平错误得0分)
④B或C,或BC(2分)
(3)1:3(2分)
本题解析:(1)A、生成N2,N元素化合价升高,生成SO2,S元素化合价降低,符合氧化还原反应原理,预测合理;B、生成NH3、SO3、H2O,为非氧化还原反应,预测合理;C、生成SO2,S元素化合价降低,无元素化合价升高,不符合氧化还原反应原理,预测不合理;D、既有元素化合价升高,也有元素化合价降低,预测合理。
(2)①利用加热气体膨胀的原理检验装置的气密性,首先要关闭支口开关K1并打开K2,然后将最后的导管通入水中,微热大试管,若看到从导管中出现气泡,且停止加热后在导管中上升一段水柱,则证明气密性好。
②用浓盐酸检验NH3,打开K1,用蘸有浓盐酸的玻璃棒靠近支口,若出现白烟,证明含有NH3,但不能用润湿的石蕊试纸,因为混合气体中含有SO2,SO3,试纸不可能变蓝;装置A与B之间的T型导管中出现白色固体可能是SO2与NH3反应生成的(NH4)2SO3,或SO3与NH3反应生成的(NH4)2SO4,或SO3固体,或酸式盐及以上物质的混合物。
③A试管中残留的白色固体是两性氧化物,则A为Al2O3,与NaOH溶液反应的离子方程式为:Al2O3 +2OH-=2AlO2-+H2O或Al2O3 +3H2O +2OH-=2Al(OH)4-。
④打开止水夹K1 倒吸的液体由支口出流出,关闭止水夹K2,导管被关闭,所以防止倒吸的方法为:B或C,或BC。
(3)根据氧化还原反应中化合价升高的总价数与降低的总价数相等,可得:6n(N2)=2n(SO2),可得n(N2):n(SO2)=1:3,相同条件下气体物质的量之比等于体积之比,所以V(N2):V(SO2)=1:3。
本题难度:困难
2、选择题 下列方案能够达到实验目的的是?
A.用浓溴水除去苯中的苯酚
B.用新制Cu(OH)2悬浊液鉴别苯、乙醛、乙酸
C.在加热条件下,用乙醇除去乙酸乙酯中的乙酸
D.将溴乙烷和NaOH溶液混合加热后,再加入硝酸银溶液,检验溴元素
参考答案:B
本题解析:A、溴单质和生成的三溴苯酚都会溶解在苯中,不能除去,错误;B、新制Cu(OH)2悬浊液与苯不反应、与乙醛加热有红色沉淀、与乙酸发生酸碱中和而溶解,现象不同可以鉴别,正确;C、乙醇和乙酸的酯化反应是可逆反应,不能彻底进行,错误;D、检测溴离子应该先用硝酸酸化,再加入硝酸银溶液,错误。
本题难度:一般
3、选择题 下列物质的分离方法不正确的是(?)
A.用结晶的方法分离汽油和水;
B.用过滤的方法除去氯化钠溶液中的泥沙;
C.用重结晶的方法从含有少量氯化钠的硝酸钾溶液中提取硝酸钾;
D.蒸馏法分离乙酸(沸点118。)和乙酸乙酯(沸点77.1。);
参考答案:A
本题解析:汽油不溶于水,采用分液分离,A不正确,其余都是正确的,答案选A。
本题难度:一般
4、选择题 相同质量的下列物质,所含分子数目最多的是
A.CH4
B.NH3
C.H2O
D.HF
参考答案:A
本题解析:分析:相同质量时,分子个数最多即相对分子质量最小的物质,由于分子的质量与其相对分子质量成正比,故只要找到相对分子质量最小的物质即可.
解答:相同质量时,分子个数最多即相对分子质量最小的物质,由于分子的质量与其相对分子质量成正比,故只要找到相对分子质量最小的物质即可,
四个选项中CH4相对分子质量最小是16.而NH3是17;H2O是18;HF是20.
故选A.
点评:本题考查分子个数的计算,难度不大,解题的关键是利用相对分子质量与分子质量成正比,分析出质量相同的物质分子个数的多少,属基础性知识考查题.
本题难度:简单
5、选择题 只用一种试剂就能将苯酚、乙醇、NaOH、KSCN、Na2CO3、KI六种溶液鉴别开的是
A.FeCl3溶液
B.KMnO4溶液
C.溴水
D.CCl4
参考答案:A
本题解析:A.苯酚中加入FeCl3溶液,溶液变为紫色;乙醇加入FeCl3溶液无现象; NaOH加入FeCl3溶液产生红褐色沉淀; KSCN加入FeCl3溶液,溶液变为血红色; Na2CO3加入FeCl3溶液发生的现象是既有红褐色沉淀产生又有无色气体逸出;KI加入FeCl3溶液,溶液变为棕黄色。现象个不相同,可以区分。正确。B.试剂KMnO4溶液能把苯酚氧化为对苯醌,不溶解于水,把乙醇氧化为乙酸,溶液为无色,把KI氧化为I2,溶液变为黄色,但与NaOH、KSCN、Na2CO3都不反应,溶液无明显的颜色变化,无法区分。错误。C. 溴水遇苯酚产生三溴苯酚白色沉淀,遇乙醇无明显变化,Br2+2NaOH="NaBr+NaBrO+" H2O。溶液我明显的变化。与KSCN不反应,2HBr+ Na2CO3=NaBr+H2O+ CO2↑。Br2+2KI=KBr+I2。溶液的颜色变为黄色。无法区分。错误。D.CCl4能溶解苯酚,不分层,与乙醇混溶,不分层,而与NaOH、KSCN、Na2CO3、KI不能溶解,也不能发生反应。无法区分。错误。
本题难度:一般