1、选择题 北京2008奥运会金牌直径为70mm,厚6mm。某化学兴趣小组对金牌成分提出猜想:甲认为金牌是由纯金制造;乙认为金牌是由金银合金制成;丙认为金牌是由黄铜(铜锌合金)。为了验证他们的猜想,请你选择一种试剂证明甲、乙、丙猜想的正误
A.硫酸铜溶液
B.盐酸
C.稀硝酸
D.硝酸银溶液
参考答案:C
本题解析:在金属活动性顺序表中,Au与任何酸都不会发生反应,Ag能与硝酸发生反应,得到的AgNO3是无色溶液;而Zn与与硝酸反应得到Zn(NO3)2溶液是无色溶液;Cu与硝酸反应得到的是蓝色Cu(NO3)2溶液。因此用稀硝酸就可以证明甲、乙、丙猜想的正误.选项为C。
本题难度:一般
2、选择题 除去下列各组物质中的杂质(括号内为杂质),采用的方法不正确的是( )
A.NaCl(NH4Cl)加热
B.FeCl2溶液(FeCl3)加铁粉
C.AlCl3溶液(MgCl2)加氨水
D.Na2CO3(NaHCO3)加热
参考答案:A.氯化铵不稳定,在加热条件下易分解生成氨气和氯化氢,氯化钠较稳定,在加热条件下不变化,所以可以采用加热的方法除去氯化铵,故A正确;
B.氯化铁和铁反应生成氯化亚铁,且过量的铁和水不反应,不引进新的杂质,故B正确;
C.氯化铝和氯化镁与氨水反应都生成沉淀,所以不能用氨气除去氯化铝中的氯化镁,故C错误;
D.在加热条件下,碳酸氢钠分解生成碳酸钠、二氧化碳和水,碳酸钠较稳定,在加热条件下不分解,所以可以采用加热的方法除去碳酸钠中的碳酸氢钠,故D正确;
故选C.
本题解析:
本题难度:一般
3、填空题 (14分)废旧碱性锌锰干电池内部的黑色物质A主要含有MnO2、NH4CI、ZnCI2,还有少量的FeCI2和炭粉,用A制备高纯MnCO3,的流程图如下。
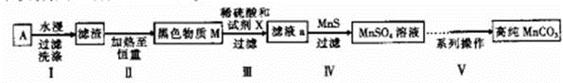
(1)碱性锌锰干电池的负极材料是_________(填化学式)。
(2)第Ⅱ步操作的目的是________________________。
(3)第Ⅳ步操作是对滤液a进行深度除杂,除去Zn2+的离子方程式为____________________。
(已知:Ksp(MnS)=2.5×10-13,Ksp(ZnS)=1.6×10-24)?
(4)为选择试剂X,在相同条件下,分别用5 g黑色物质M进行制备MnSO3的实验,得到数据如右表:

①试剂x的最佳选择是_________。
②第Ⅲ步中用选出的最佳试剂X与M的主要成分反应的化学方程式为_________。
(5)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH为7.7。请补充完成以下操作:
第Ⅴ步系列操作可按一下流程进行:请补充完成操作:(第Ⅴ步系列操作中可供选用的试剂: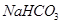 、乙醇)
、乙醇)
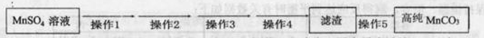
操作1:___________________;操作2:过滤,用少量水洗涤2~3次
操作3:检测滤液,表明SO42-已除干净; 操作4:___________________;
操作5:低温烘干。
(6)操作1可能发生反应的离子方程式?
参考答案:(14分,每空2分)
(1)Zn
(2)除去碳粉
(3)Zn2++MnS=ZnS+Mn2+
(4)①30%的过氧化氢?②H2O2+MnO2+H2SO4=MnSO4+2H2O+O2↑
(5)加入NaHCO3,控制pH<7.7;?用少量无水乙醇洗涤2~3次
(6)Mn2++2 HCO3-= MnCO3↓+H2O+CO2↑
本题解析:(1) 碱性锌锰干电池中,锌比锰活泼,所以负极材料是Zn;
(2)第I步操作水浸后,溶于水的NH4CI、ZnCI2可除去,而碳粉不溶于水,所以第Ⅱ步操作的目的是除去碳粉;
(3)第Ⅳ步操作中加入MnS目的是利用沉淀的转化除去Zn2+,使MnS转化为更难溶的ZnS,离子方程式为Zn2++MnS=ZnS+Mn2+
(4)①根据表中数据选择30%的过氧化氢得到的MnSO4的质量最多,所以选择30%的过氧化氢;
②根据表可知,过氧化氢是把二氧化锰转化为硫酸锰,本身被氧化为氧气,化学方程式为H2O2+MnO2+H2SO4=MnSO4+2H2O+O2↑
(5)最终产物是碳酸锰,所以第一步应加入NaHCO3,调节pH值使之小于7.7,防止氢氧化锰生成;MnCO3潮湿时易被空气氧化,所以水洗完后再用用少量无水乙醇洗涤2~3次以除去碳酸锰表面的水分;
(6)操作1目的是生成碳酸锰的沉淀,所以可能发生反应的离子方程式Mn2++2 HCO3-= MnCO3↓+H2O+CO2↑
本题难度:困难
4、选择题 下列实验能达到预期目的是( )
A.可用过滤法分离氢氧化铁胶体和三氯化铁溶液的混合物
B.实验室制取乙烯时,常含有少量的CO2、SO2及H2O(g)杂质,可依次通过高锰酸钾溶液和碱石灰得较纯净的乙烯气体
C.鉴别氯化铝和氯化镁溶液:分别滴加过量的氢氧化钠溶液
D.银镜反应实验后试管内壁附有银,可用氨水清洗
参考答案:A、过滤法可以实现固体和液体物质的分离,氢氧化铁胶体和三氯化铁溶液均可以透过滤纸,它们的混合物可以采用渗析法,故A错误;
B、乙烯具有还原性,能被高锰酸钾氧化为二氧化碳,所以乙烯中的杂质不能用高锰酸钾来除去,故B错误;
C、氯化铝中滴加过量的氢氧化钠溶液,会得到无色的偏铝酸钠溶液,但是氯化镁中加入过量的氢氧化钠,会得到氢氧化镁白色沉淀,现象不一样,可以进行鉴别,故C正确;
D、金属银和氨水是不反应的,试管壁上的金属银可以用硝酸洗去,故D错误.
故选C.
本题解析:
本题难度:一般
5、选择题 从氯酸钾分解制氧气后的剩余物中回收二氧化锰的操作顺序正确的是
[? ]
A.溶解、过滤、蒸发、加热
B.溶解、过滤、洗涤、加热
C.溶解、蒸发、洗涤、过滤
D.溶解、洗涤、过滤、加热
参考答案:B
本题解析:
本题难度:一般