1、选择题 随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。下列有关说法中不正确的是

[? ]
A.电解法合成氨的电解池中能用水作电解质溶液的溶剂
B.钯电极A的电极反应式为:N2+6e-+6H+==2NH3
C.钯电极B连接的是电源的正极
D.当有0.3mol电子转移时,有0.12mol?NH3生成
2、填空题 (12分)如图装置闭合电键时,电流计A的指针将发生偏转。试回答下列问题。
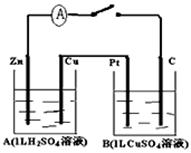
(1)A池是____________;Zn的电极名称是____________;B池是____________;
Pt的电极名称是____________(填电解池、原电池、阴、阳、正、负极等)
(2)写出下列有关反应:C极上电极反应:_________________
(3)B池中的总反应的化学方程式为________________________
3、填空题 下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g
10.00%的K2SO4溶液,电极均为石墨电极。

(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。
据此回答问题:
① 电源的N端为___________极;
② 电极b上发生的电极反应为___________;
③ 列式计算电极b上生成的气体在标准状况下的体积:___________;
④ 电极c的质量变化是___________g;
⑤ 电解前后个溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液____________________;乙溶液___________________;丙溶液______________________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?____________________________________________。
4、选择题 NH4Cl溶液中水的电离程度比盐酸中水的电离程度(? )
A.大
B.小
C.相等
D.不能确定
5、填空题 (10分)化工厂的联合生产可以提高资源的利用率,有效减少环境污染,某化工集团将钛的生产和氯碱工业及甲醇生产联合起来,其主要工艺如下:
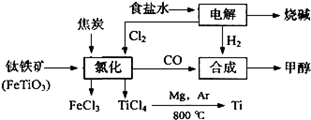
(1)工业电解饱和食盐水的化学方程式为________,其阳极产物为________(填化学式)。
(2)上述工艺流程中钛铁矿在高温条件下经过氯化法得到四氯化钛的化学方程式为________。
(3)已知:① Mg(s) + Cl2(g) = MgCl2(s) △H =" -641" kJ・mol-1
② Ti(s) + 2Cl2(g) = TiCl4(s) △H =" -770" kJ・mol-1
则 2Mg(s) + TiCl4(g) = MgCl2(s) + Ti(s) △H = ________。
(4)在25℃、101kPa条件下,1 g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.7 kJ,则表示甲醇燃烧的热化学方程式为:________________________________________。