1、填空题 (14分)运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)某硝酸厂处理尾气中NO的方法是:催化剂存在时用H2将NO还原为N2。已知:

则氮气和水蒸气反应生成氢气和一氧化氮的热化学方程式是 。
(2)在压强为0.1 Mpa条件,将a mol CO和3a mol H2的混合气体在催化剂作用下转化为甲醇的反应如下:CO(g)+2H2(g) CH3OH(g) ΔH<0。
CH3OH(g) ΔH<0。
①该反应的平衡常数表达式为________________。
②若容器容积不变,下列措施可增大甲醇产率的是________。
A.升高温度
B.将CH3OH从体系中分离
C.充入He,使体系总压强增大
(3)某研究小组在实验室研究某催化剂效果时,测得NO转化为N2的转化率随温度变化情况如图。

①若不使用CO,温度超过775 ℃,发现NO的分解率降低,其可能的原因为________;在n(NO)/n(CO)=1的条件下,应控制最佳温度在________左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染。

写出C2H6与NO2发生反应的化学方程式________________。
(4)以NO2、O2、熔融NaNO3组成的燃料电池装置如右图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电极反应式为________________________。
参考答案:(1)N2(g)+2H2O(g)===2NO(g)+2H2(g) ΔH=+665 kJ・mol-1
(2)c(CH3OH)/c(CO)・c2(H2);B
(3)①该反应是放热反应,升高温度反应更有利于向逆反应方向进行;870℃
②4C2H6+14NO2 8CO2+7N2+12H2O
8CO2+7N2+12H2O
(4)NO2+NO3--e-===N2O5
本题解析:(1)化学反应方程式为N2+2H2O===2NO+2H2,由图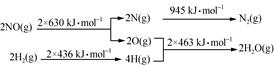 可知,ΔH=945+4×463-2×630-2×436=+665 kJ・mol-1,故热化学方程式为N2(g)+2H2O(g)===2NO(g)+2H2(g) ΔH=+665 kJ・mol-1;
可知,ΔH=945+4×463-2×630-2×436=+665 kJ・mol-1,故热化学方程式为N2(g)+2H2O(g)===2NO(g)+2H2(g) ΔH=+665 kJ・mol-1;
(2)由热化学方程式CO(g )+2H2(g) CH3OH(g) ΔH<0可知,平衡常数K=
CH3OH(g) ΔH<0可知,平衡常数K=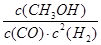 ;欲增大甲醇产率,则应使该平衡正向移动,升高温度,平衡向着吸热的方向移动,该平衡逆移, 将CH3OH从体系中分离,可使平衡正移,充入He,使体系总压强增大,该平衡不移动,故选择B;
;欲增大甲醇产率,则应使该平衡正向移动,升高温度,平衡向着吸热的方向移动,该平衡逆移, 将CH3OH从体系中分离,可使平衡正移,充入He,使体系总压强增大,该平衡不移动,故选择B;
(3)①由图可知,若不使用CO,温度超过775 ℃,发现NO的分解率降低,则该反应是放热反应,升高温度反应更有利于向逆反应方向进行;在n(NO)/n(CO)=1的条件下,应控制最佳温度在850-900℃之间;
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染,C2H6与NO2反应,生成无污染的N2和CO2,反应方程式为4C2H6+14NO2 8CO2+7N2+12H2O;
8CO2+7N2+12H2O;
(4)以NO2、O2、熔融NaNO3组成的燃料电池,由图可知,石墨Ⅰ为燃料电池的负极,负极失电子,生成一种氧化物Y,电极反应为NO2+NO3--e-===N2O5。
考点:热化学方程式的书写,平衡常数的计算,化学平衡的移动,图像的描述,化学反应方程式的书写,电极反应的书写
本题难度:困难
2、填空题 工业生产硝酸铵的流程图如下:?
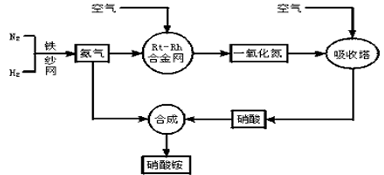
请回答下列问题:
(1)写出硝酸铵在工农业生产中的主要用途____________(任写一条)。
(2)已知N2 (g) +3H2(g) 2NH3(g) △H = -92kJ . mol-1。请回答:
2NH3(g) △H = -92kJ . mol-1。请回答:
①在500℃、200atm和铁催化条件下向一密闭容器中充入 1mol N2和3 mol H2,充分反应后,放出的热量_________(填 “<”“>”或“=”)92.4kJ,理由是_____________。
②为有效提高氢气的转化率,实际生产中宜采取的措施有___________
A.降低温度
B.最适合催化剂活性的适当高温
C.增大压强
D.降低压强
E.循环利用和不断补充氮气
F.及时移出氨
(3)写出氨在铂铑合金网催化氧化下的化学方程式:_________。
(4)在一定温度和压强的密闭容器中,将物质的量之比为 3:2的H2和N2混合,当该反应达到平衡时,测出平衡混合气中氨的体积分数为15%,此时H2的转化率为___________。
参考答案:(1)可做氮肥
(2)①<? ;在latm和298K条件下. 1mol氮气和3mol氢气完全反应生成2mol氨气,放出92.4kJ热量,而该反应为可逆反应,不可能进行完全,且题给条件为500℃、200 atm,故放出的热量肯定小于92.4 kJ
②CEF
(3)4NH3 +5O2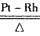 4NO +6H2O
4NO +6H2O
(4)32.6%
本题解析:
本题难度:一般
3、选择题 在恒温的密闭容器中,放入A和B两种物质,当反应A(g)+2B(g)?2C(g)达平衡时,下列说法正确的是( )
A.平衡混合气的总质量不变
B.平衡混合气与原混合气的相对平均分子质量相等
C.容器内压强在温度不变时,反应前后没有改变
D.平衡时,混合气体的物质的量比反应前少
参考答案:A、该反应两边都是气体,一定满足平衡混合气的总质量不变,故A正确;
B、因反应前计量数之和大于反应后的计量数,即该反应中气体的物质的量减小,而气体的质量不变,所以.M增大,故B错误;
C、在恒温恒容条件下,该反应中气体的体积减小,混合气体的压强减小,故C错误;
D、该反应是体积减小的反应,达到平衡时混合气体的物质的量减小,故D正确;
故选AD.
本题解析:
本题难度:一般
4、选择题 下列事实中不能用勒夏特列原理来解释的是( )
A.向H2S水溶液中加入NaOH固体有利于S2-增多
B.鼓入过量空气有利于SO2转化为SO3
C.高压对合成氨有利
D.500℃左右比室温更有利于氨的合成
参考答案:A、硫化氢溶液中存在电离平衡H2S?HS-+H+,HS-?S2-+H+,加入碱中和氢离子,平衡正向进行有利于S2-的生成,能用勒夏特列原理解释,故A不符合;
B、存在平衡2SO2+O2(g)?2SO3(g),加入过量的空气,平衡向正反应方向移动,提高二氧化硫的转化率,能用勒夏特利原理解释,故B不符合;
C、合成氨反应N2+3H2=2NH3,反应前后气体体积减小,高压有利于合成氨反正向进行,能用勒夏特列原理解释,故C不符合;
D、合成氨反应N2+3H2=2NH3,反应是放热反应,温度升高平衡逆向进行,500℃左右比室温更利于合成氨反应,是因为此时反应速率增大,催化剂活性最大,不能用勒夏特列原理解释,故D符合;
故选D.
本题解析:
本题难度:简单
5、填空题 在一小烧杯里混合10ml0.01mol/LFeCl3溶液和10ml0.01mol/LKSCN溶液,溶液立即变为红色.
(1)再向溶液中滴入1mol/LFeCl3溶液,现象______,平衡向______反应方向移动,KSCN浓度会______.
(2)在烧杯中加入KCl固体,颜色______,平衡______移动.
参考答案:(1)发生反应FeCl3+3KSCN?Fe(SCN)3+3KCl反应,存在平衡:Fe3++3SCN-=Fe(SCN)3,滴入1mol/LFeC13溶液,铁离子浓度增大,平衡正向进行溶液颜色加深,平衡移动后KSCN浓度会减小,
故答案为:溶液红色加深,正;降低;
(3)平衡为Fe3++3SCN-=Fe(SCN)3,加入KC1固体,对存在平衡的离子浓度不影响,平衡不动,溶液颜色不变;
故答案为:无变化,不.
本题解析:
本题难度:一般